Clear Sky Science · de
Forschungsfortschritte zur Heterogenität dentaler mesenchymaler Stammzellen
Warum winzige Zahn-Stammzellen wichtig sind
Zähne wirken an der Oberfläche einfach, doch im Inneren verbirgt sich eine geschäftige Welt von Stammzellen, die stillschweigend unseren Zahnbestand aufbauen, erhalten und reparieren. Dieser Übersichtsartikel behandelt eine spezielle Zellfamilie in und um die Zähne — dentale mesenchymale Stammzellen — und erklärt, wie ihre verborgene Vielfalt den Weg zu besseren Behandlungen von Karies, Zahnfleischerkrankungen, Knochverlust im Kiefer und sogar Nervenverletzungen öffnen könnte. Wenn Forscher die „Besetzung“ hinter Zahnentwicklung und Heilung verstehen, hoffen sie, intelligentere, zuverlässigere regenerative Therapien zu entwickeln, statt sich allein auf Bohren, Füllungen und Implantate zu verlassen.
Von frühen Zahnknospen bis zu ausgewachsenen Zähnen
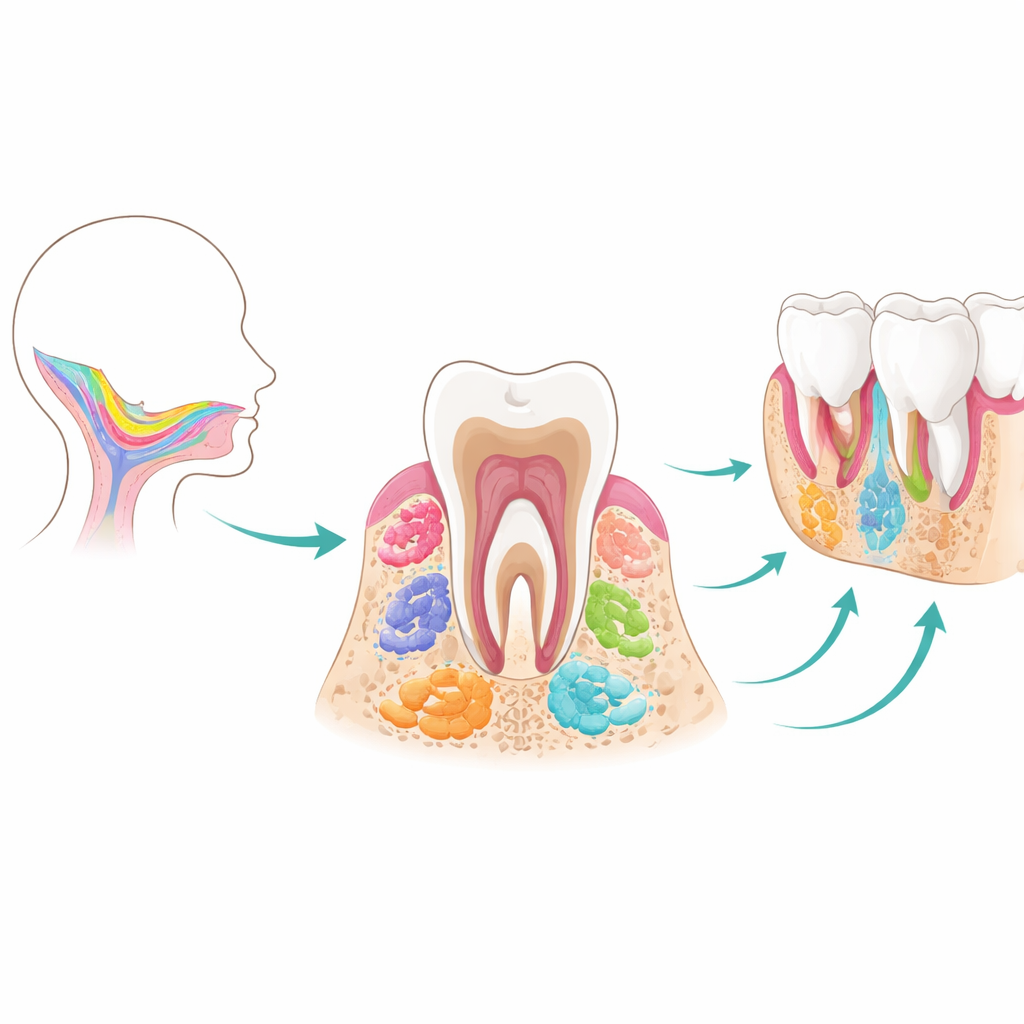
Zähne und ihre stützenden Gewebe entstehen durch eine eng abgestimmte Partnerschaft zwischen zwei Hauptschichten: einer äußeren Hülle, die später den Zahnschmelz bildet, und inneren Zellen, die Dentin, Pulpa, Bandapparat und Kieferknochen hervorbringen. Die mesenchymalen Stammzellen im Mittelpunkt dieses Reviews stammen alle von wandernden Zellen des frühen Embryos, den kranialen Neuralleistenzellen. Wenn sie sich im sich bildenden Kiefer ansiedeln, bilden diese Zellen zunächst Zahnkeime — winzige „Knospen“, die die Stadien Knospe, Kappe und Glocke durchlaufen. Im Laufe dieser Entwicklung treten nacheinander mehrere vorübergehende Stammzellpopulationen auf. Zahnkeim-Progenitorzellen fungieren als frühe, vielseitige Baumeister; Zellen des dentalen Follikels helfen bei der Montage der Gewebe, die den Zahn an seinem Platz halten; und Stammzellen in der apikalen Papille an der Wurzelspitze steuern die Wurzelbildung und zeigen überraschendes Potenzial, nervenähnliche Zellen zu bilden. Sobald Zahnwurzeln ausgereift sind, verschwinden viele dieser frühen Akteure, was ihre Untersuchung oder spätere Nutzung erschwert.
Viele Stammzelltypen, ein integriertes Zahnsystem
Auch nachdem Zähne vollständig gebildet sind, verbleiben mehrere Arten von Stammzellen in geschützten Nischen und unterstützen weiterhin den Gewebeerhalt. Dentale Pulpa-Stammzellen leben im Inneren des Zahns, wo Blutgefäße und Nerven einmünden; Stammzellen des Parodontalspalts sitzen zwischen Zahnwurzel und Knochen; gingivale Stammzellen kleiden das Zahnfleisch aus; und mesenchymale Stammzellen im Alveolarknochen bilden den „Boden“, der die Zähne verankert. Jede Population teilt grundlegende Eigenschaften wie Selbsterneuerung und die Fähigkeit, sich in knochen- oder dentinbildende Zellen zu differenzieren, ist aber nicht austauschbar. Pulpa-Stammzellen neigen beispielsweise dazu, Dentin- und nervenähnliche Schicksale zu bevorzugen, parodontale Zellen sind besonders gut im Wiederaufbau der faserigen Verankerung und des Zementums an der Wurzeloberfläche, und Kieferknochenstammzellen sind auf schnelle, direkte Knochenbildung im Gesichtsbereich spezialisiert. Diese eingebaute Arbeitsteilung erklärt, warum die Mundhöhle unterschiedlich auf Verletzungen von Pulpa, Bandapparat oder Knochen reagiert.
Verborgene Unterschiede innerhalb jeder Stammzell-Gruppe
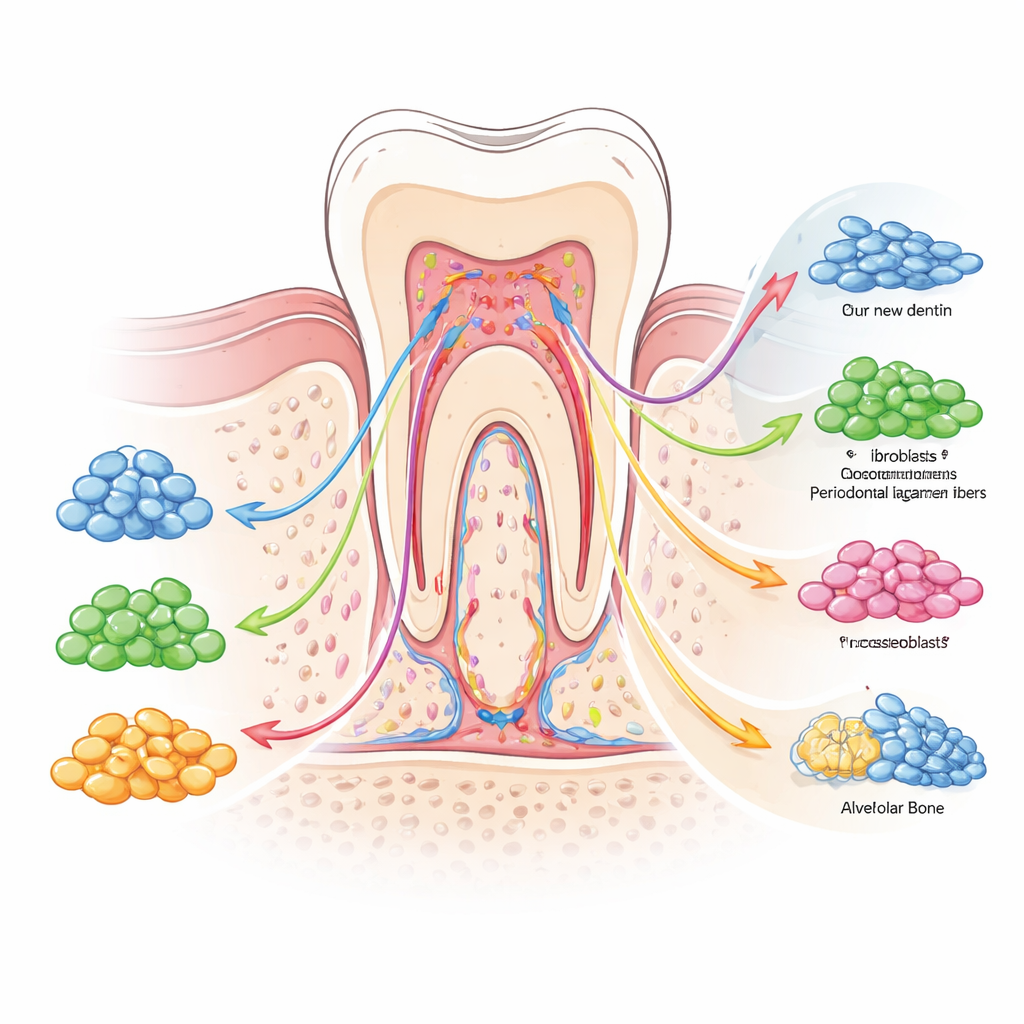
Eine zentrale Botschaft des Reviews ist, dass Heterogenität nicht nur zwischen verschiedenen Stammzelltypen besteht, sondern auch innerhalb jeder einzelnen Gruppe. Neue Methoden wie die Einzelzell-RNA-Sequenzierung erlauben es, Tausende einzelner Zellen gleichzeitig zu profilieren und Untergruppen mit unterschiedlicher Genaktivität und unterschiedlichem Verhalten zu identifizieren. In der dentalen Pulpa haben Forscher beispielsweise mehrere Cluster kartiert: einige erhalten den Reservestamm und treiben Proliferation an, andere sind auf Dentinproduktion vorbereitet, und wieder andere sind zugunsten der Bildung von Blutgefäßen oder nervenähnlichen Zellen voreingenommen. Ähnliche Subgruppen wurden in parodontalen Ligamentstammzellen, Kieferknochenstammzellen, Stammzellen aus Milchzähnen und gingivalen Stammzellen gefunden. Markermoleküle an der Zelloberfläche und im Zellkern helfen, diese Subpopulationen zu unterscheiden, die sich in Wachstumsfähigkeit, Alterungsverlauf und Reagibilität auf mechanische Kräfte, Entzündung oder bakterielle Angriffe unterscheiden.
Signale und Schalter, die das Stammzellverhalten formen
Die Autoren betonen, dass diese Vielfalt nicht zufällig ist. Sie wird von einem Netzwerk biochemischer Signale und „epigenetischer“ Schalter organisiert, die wie Ampeln und Wegweiser für das Zellschicksal wirken. Signalwege, die durch bone morphogenetic proteins, Wnt-Signale und transforming growth factor beta gesteuert werden, treiben Zellen in Richtung Aufbau harter Gewebe wie Dentin und Knochen, während andere, darunter Notch und PI3K/AKT, helfen, ein ausgewogenes Reservoir von Stamm- und Vorläuferzellen zu erhalten. Gleichzeitig passen chemische Markierungen an DNA und Verpackungsproteinen an, welche Gene zugänglich sind, und stellen bestimmte Zellen darauf ein, bei Schäden schnell zu reagieren. Mechanische Kräfte durch Kauen, entzündliche Moleküle bei Infektionen und Signale von nahen Blutgefäßen oder Nerven verschieben das Gleichgewicht weiter in Richtung Reparatur, Narbenbildung oder Abbau. Zusammen schaffen diese Ebenen der Kontrolle ein flexibles, aber manchmal unvorhersehbares Heilsystem.
Was das für die zahnmedizinische Versorgung der Zukunft bedeutet
Für Nicht‑Spezialisten ist die wichtigste Erkenntnis, dass Zahn‑ und Zahnfleischregeneration keine Science‑Fiction mehr ist, ihr Erfolg aber davon abhängen wird, die Stammzellvielfalt zu steuern, statt sie zu ignorieren. Das Review argumentiert, dass die Kenntnis, welche spezifischen Subpopulationen Dentin, Bandapparat, Knochen oder Nerven aufbauen — und welche Signale sie steuern — Forschern helfen wird, Zellselektion, Biomaterialien und pharmakologische Signale für vorhersehbare Ergebnisse zu verfeinern. Gleichzeitig mahnen die Autoren, dass die meisten detaillierten Karten aus Tierstudien und Zellkulturen stammen und technische Störungen das Bild verwischen können. Sie fordern integrierte „Multi‑Omics“‑Ansätze an menschlichem Gewebe, bessere Standardisierung und rigorose Tests in lebenden Systemen. Letztlich könnte das Entschlüsseln der Heterogenität dentaler mesenchymaler Stammzellen Zahnärzten erlauben, beschädigte Strukturen nicht nur durch inert Materialien zu ersetzen, sondern lebende, funktionelle Zähne und ihre Stützgewebe wirklich zu regenerieren.
Zitation: Fu, H., Chen, P., Wu, Z. et al. Research progress in heterogeneity of dental mesenchymal stem cells. Int J Oral Sci 18, 31 (2026). https://doi.org/10.1038/s41368-026-00433-8
Schlüsselwörter: dentale Stammzellen, Zahnerneuerung, parodontale Rekonstruktion, Einzelzellsequenzierung, orale Gewebetechnik