Clear Sky Science · sv
Forskningens framsteg om heterogenitet hos dentala mesenkymala stamceller
Varför små tandstamceller spelar roll
Tänder kan se enkla ut på ytan, men inuti finns en livlig värld av stamceller som tyst bygger, underhåller och reparerar våra leenden. Denna översiktsartikel undersöker en särskild familj av celler i och runt tänderna — dentala mesenkymala stamceller — och förklarar hur deras dolda mångfald kan öppna dörrar till bättre behandlingar för karies, tandköttssjukdomar, käkbenförlust och till och med nervskador. Genom att förstå vilka “personer” som ligger bakom tandutveckling och läkning hoppas forskare kunna utforma smartare, mer pålitliga regenerativa terapier istället för att förlita sig enbart på borrar, fyllningar och implantat.
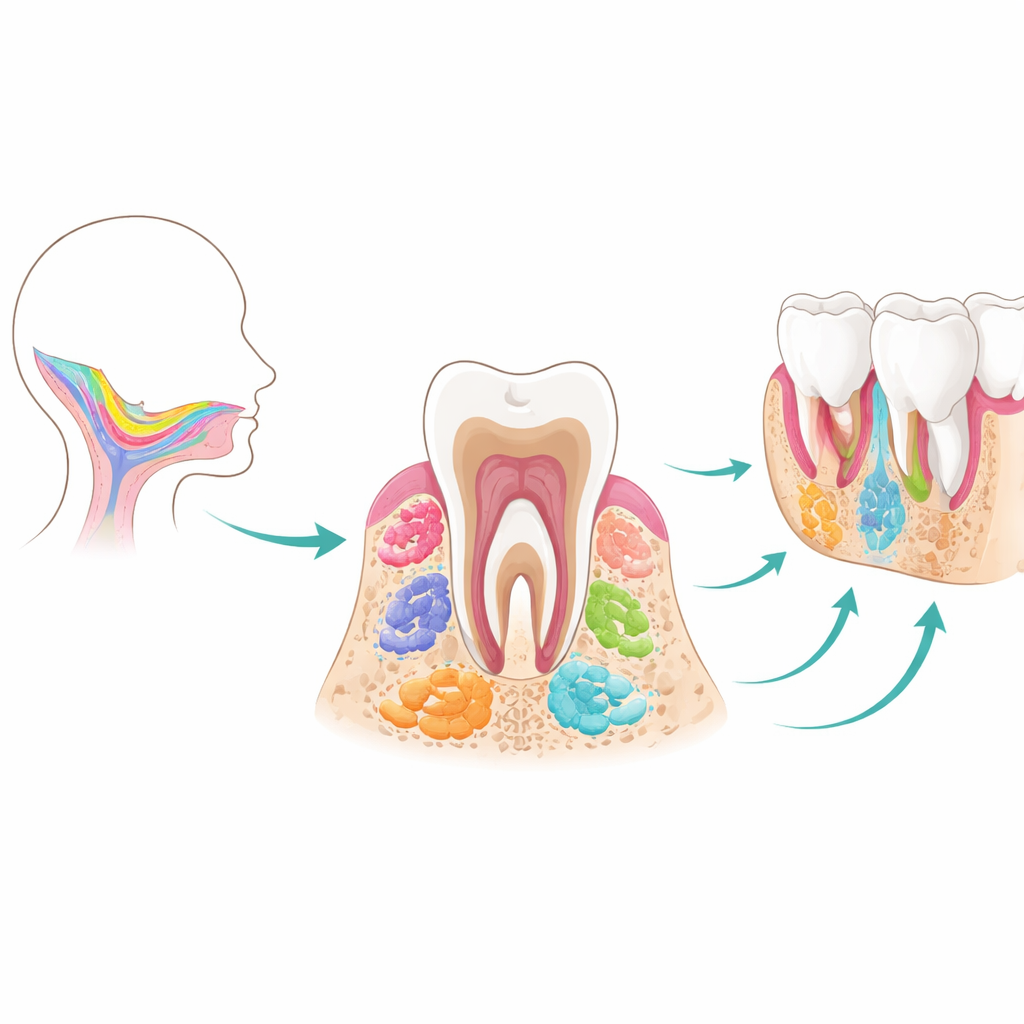
Från tidiga tandknoppar till fullvuxna tänder
Tänder och deras stödjande vävnader bildas genom ett tätt koreograferat samspel mellan två huvudlager: ett yttre täcke som senare bildar emalj, och inre celler som ger upphov till dentin, pulpa, ligament och käkben. De mesenkymala stamcellerna i centrum för denna översikt härstammar alla från migrerande celler i det tidiga embryot som kallas kraniell neuralfåra. När de bosätter sig i den formande käken bildar dessa celler först tandgerminaler — små ”knoppar” som går igenom knop-, hatt- och klockstadier. Längs denna tidslinje uppträder flera temporära stamcellspopulationer i följd. Progenitorceller i tandgermen fungerar som tidiga, mångsidiga byggare; tandfollikelns stamceller hjälper till att montera de vävnader som håller tänderna på plats; och stamceller i apikal papilla vid rotspetsen styr rotbildning och visar överraskande potential att bli nervliknande celler. När tandrötterna mognar försvinner många av dessa tidiga aktörer, vilket gör dem svåra att studera eller återanvända senare i livet.
Många stamcellstyper, ett integrerat tandssystem
Även efter att tänderna är fullbildade kvarstår flera typer av stamceller i skyddade nischer och fortsätter stödja vävnadsunderhållet. Dentala pulpastamceller lever inne i tanden där blodkärl och nerver går in; parodontalligamentstamceller sitter mellan tandrot och ben; gingivala stamceller bekläder tandköttet; och mesenkymala stamceller i det alveolära (käk)benet bildar ”jorden” som förankrar tänderna. Varje population delar grundläggande egenskaper som förmågan att förnya sig och differentiera till ben- eller dentinbildande celler, men de är inte utbytbara. Till exempel tenderar pulpaceller att favorisera dentin- och nervlika öden, parodontalceller utmärker sig vid att återuppbygga fibrösa fästen och cementum på rotytan, och käkbenets stamceller är specialiserade för snabb, direkt benbildning i ansiktet. Denna inbyggda arbetsfördelning hjälper till att förklara varför munnen kan reagera olika vid skada i pulpa, ligament eller ben.
Dolda skillnader inom varje stamcellspool
En huvudpoäng i översikten är att heterogenitet inte bara existerar mellan olika stamcellstyper utan även inom varje enskild typ. Nya tekniker som single-cell RNA-sekvensering kan profilera tusentals individuella celler samtidigt och avslöja undergrupper med skild genaktivitet och beteende. I dentala pulpan har forskare till exempel kartlagt flera kluster: vissa upprätthåller reservpoolen och driver proliferation, andra är förberedda för dentinproduktion, och ytterligare andra är benägna att bilda blodkärl eller nervliknande celler. Liknande undergrupper har identifierats i parodontalligamentets stamceller, käkbenets stamceller, stamceller från mjölktänder och gingivala stamceller. Markörmolekyler på cellytan och inne i kärnan hjälper till att skilja dessa subpopulationer åt, som skiljer sig i tillväxtkapacitet, åldringsmönster och respons på mekaniska krafter, inflammation eller bakteriella angrepp.
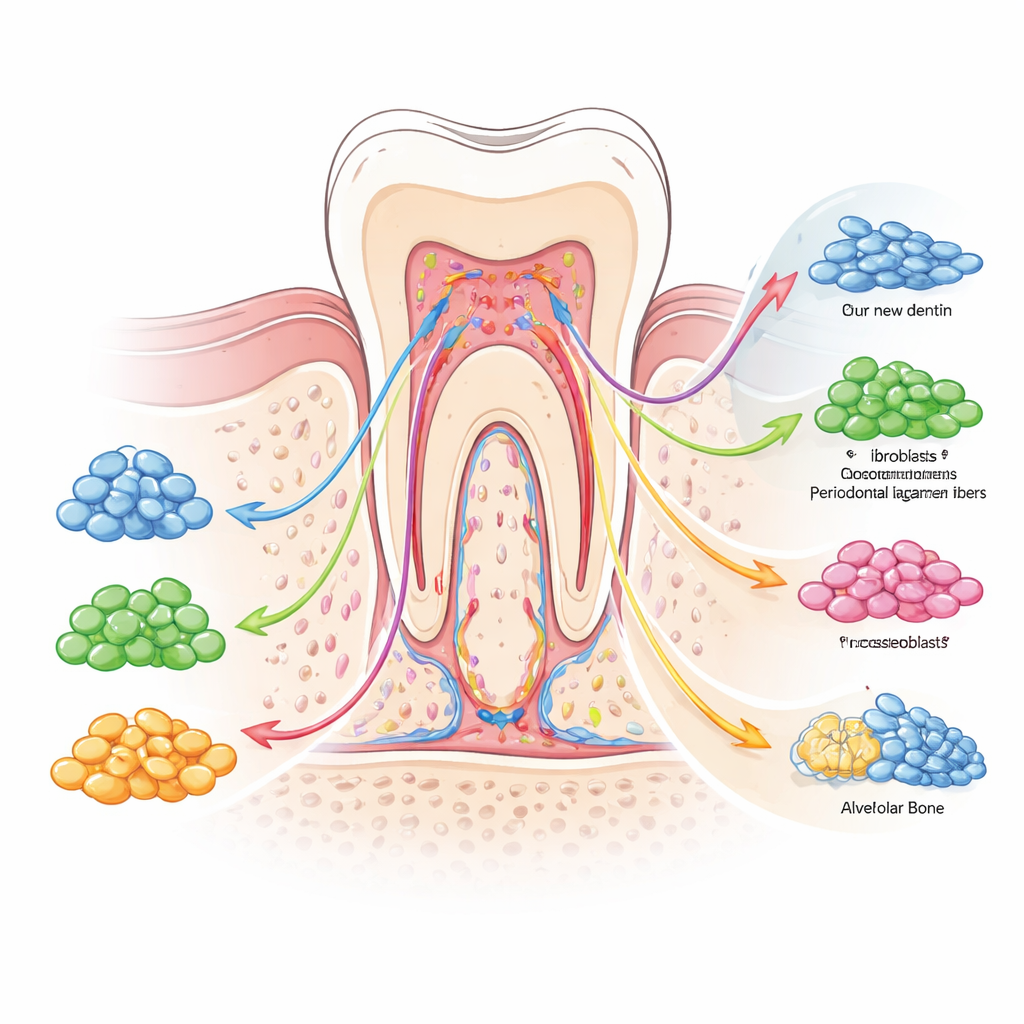
Signaler och strömbrytare som formar stamcellsbeteende
Författarna framhåller att denna mångfald inte är slumpmässig. Den organiseras av ett nätverk av biokemiska signaler och ”epigenetiska” strömbrytare som fungerar som trafikljus och vägskyltar för cellödet. Banor drivna av benmorfogenetiska proteiner, Wnt‑signaler och transformande tillväxtfaktor beta skjuter celler mot att bygga hårda vävnader såsom dentin och ben, medan andra, inklusive Notch och PI3K/AKT, hjälper till att upprätthålla en balanserad pool av stam- och progenitorceller. Samtidigt justerar kemiska märken på DNA och paketeringsproteiner vilka gener som är tillgängliga och förinställer vissa celler för snabb respons vid skada. Mekaniska krafter från tuggning, inflammatoriska molekyler vid infektion och signaler från närliggande blodkärl eller nerver skjuter alla balansen mot reparation, ärrbildning eller nedbrytning. Tillsammans skapar dessa kontrollager ett flexibelt, men ibland oförutsägbart, läkningssystem.
Vad detta betyder för framtida tandvård
För en icke‑specialist är huvudbudskapet att tand- och tandköttsregenerering inte längre är science fiction, men dess framgång kommer att bero på att hantera stamcellsmångfald snarare än att ignorera den. Översikten hävdar att kunskap om vilka specifika subpopulationer som bygger dentin, ligament, ben eller nerver — och vilka signaler som styr dem — kommer att hjälpa forskare att förfina cellval, biomaterial och läkemedelssignaler för förutsägbara resultat. Samtidigt varnar författarna för att de flesta detaljerade kartor kommer från djurstudier och laboratoriekulturer, och att tekniskt brus kan sudda bilden. De efterlyser integrerade ”multi-omics”-metoder i mänsklig vävnad, bättre standardisering och rigorösa tester i levande system. I slutändan kan avkodningen av heterogeniteten hos dentala mesenkymala stamceller möjliggöra för tandläkare att gå från att ersätta skadade strukturer med inerta material till att verkligen regenerera levande, funktionella tänder och deras stödjevävnader.
Citering: Fu, H., Chen, P., Wu, Z. et al. Research progress in heterogeneity of dental mesenchymal stem cells. Int J Oral Sci 18, 31 (2026). https://doi.org/10.1038/s41368-026-00433-8
Nyckelord: dentala stamceller, tandregenerering, parodontal reparation, single-cell-sekvensering, oral vävnadsteknik