Clear Sky Science · fr
Progrès de la recherche sur l'hétérogénéité des cellules souches mésenchymateuses dentaires
Pourquoi les petites cellules souches dentaires comptent
Les dents paraissent simples à première vue, mais en leur sein se cache un monde animé de cellules souches qui construisent, entretiennent et réparent discrètement notre sourire. Cet article de synthèse examine une famille particulière de cellules situées dans et autour des dents — les cellules souches mésenchymateuses dentaires — et explique comment leur diversité cachée pourrait ouvrir la voie à de meilleurs traitements contre la carie, les maladies des gencives, la perte osseuse de la mâchoire et même les lésions nerveuses. En comprenant la « distribution des rôles » à l’œuvre dans le développement et la réparation des dents, les chercheurs espèrent concevoir des thérapies régénératives plus intelligentes et plus fiables, plutôt que de se contenter de forages, d’obturations et d’implants.
Des bourgeons dentaires précoces aux dents adultes
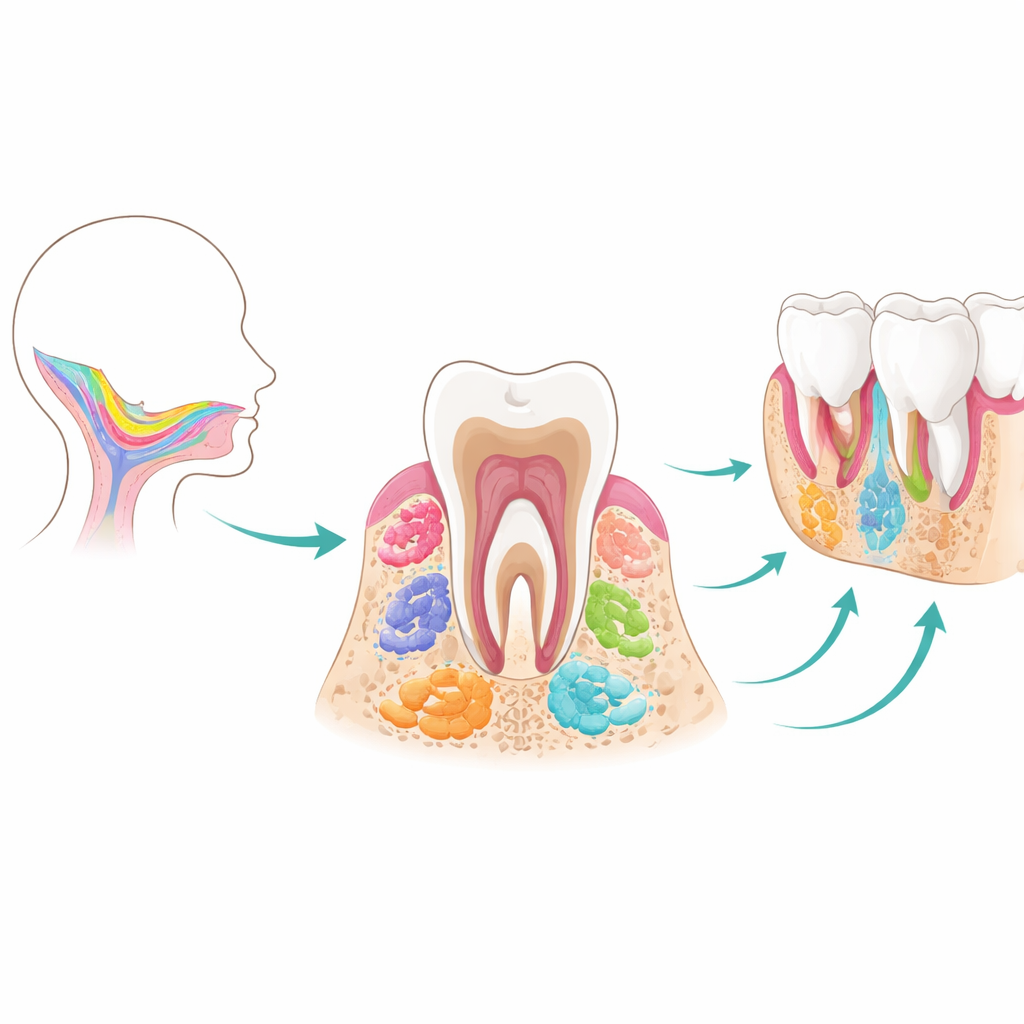
Les dents et leurs tissus de soutien se forment grâce à une coopération étroitement orchestrée entre deux couches principales : une enveloppe externe qui donnera ensuite l’émail, et des cellules internes qui produiront la dentine, la pulpe, le ligament et l’os de la mâchoire. Les cellules souches mésenchymateuses au cœur de cette revue proviennent toutes de cellules migratrices de l’embryon précoce appelées crêtes neurales crâniennes. En s’installant dans la mâchoire en formation, ces cellules génèrent d’abord des bourgeons dentaires — de petits « boutons » qui traversent les stades de bourgeon, de capuchon et de cloche. Au cours de ce développement, plusieurs populations temporaires de cellules souches apparaissent séquentiellement. Les cellules progénitrices du germe dentaire agissent comme des bâtisseurs précoces et polyvalents ; les cellules souches du follicule dentaire contribuent à assembler les tissus qui maintiennent les dents en place ; et les cellules souches de la papille apicale, situées à l’extrémité de la racine, guident la formation radiculaire et montrent un potentiel surprenant à devenir des cellules de type nerveux. Une fois les racines dentaires matures, nombre de ces acteurs précoces disparaissent, ce qui rend leur étude et leur réutilisation ultérieure difficiles.
Plusieurs types de cellules souches, un système dentaire intégré
Même après la formation complète des dents, plusieurs types de cellules souches restent nichés dans des niches protégées et continuent de soutenir l’entretien des tissus. Les cellules souches de la pulpe dentaire vivent à l’intérieur de la dent, où entrent vaisseaux sanguins et nerfs ; les cellules souches du ligament parodontal se situent entre la racine et l’os ; les cellules souches gingivales tapissent les gencives ; et les cellules mésenchymateuses de l’os alvéolaire (mâchoire) forment le « sol » qui ancre les dents. Chaque population partage des traits de base comme la capacité d’auto-renouvellement et de différenciation en cellules productrices d’os ou de dentine, mais elles ne sont pas interchangeables. Par exemple, les cellules pulpaires tendent à favoriser la dentine et les sortides de type nerveux, les cellules parodontales excellent dans la reconstruction de l’attache fibreuse et du cément à la surface radiculaire, et les cellules de l’os mandibulaire sont spécialisées pour une formation osseuse directe et rapide au niveau du visage. Cette division du travail intrinsèque aide à expliquer pourquoi la bouche réagit différemment selon que l’atteinte touche la pulpe, le ligament ou l’os.
Différences cachées au sein de chaque réservoir de cellules souches
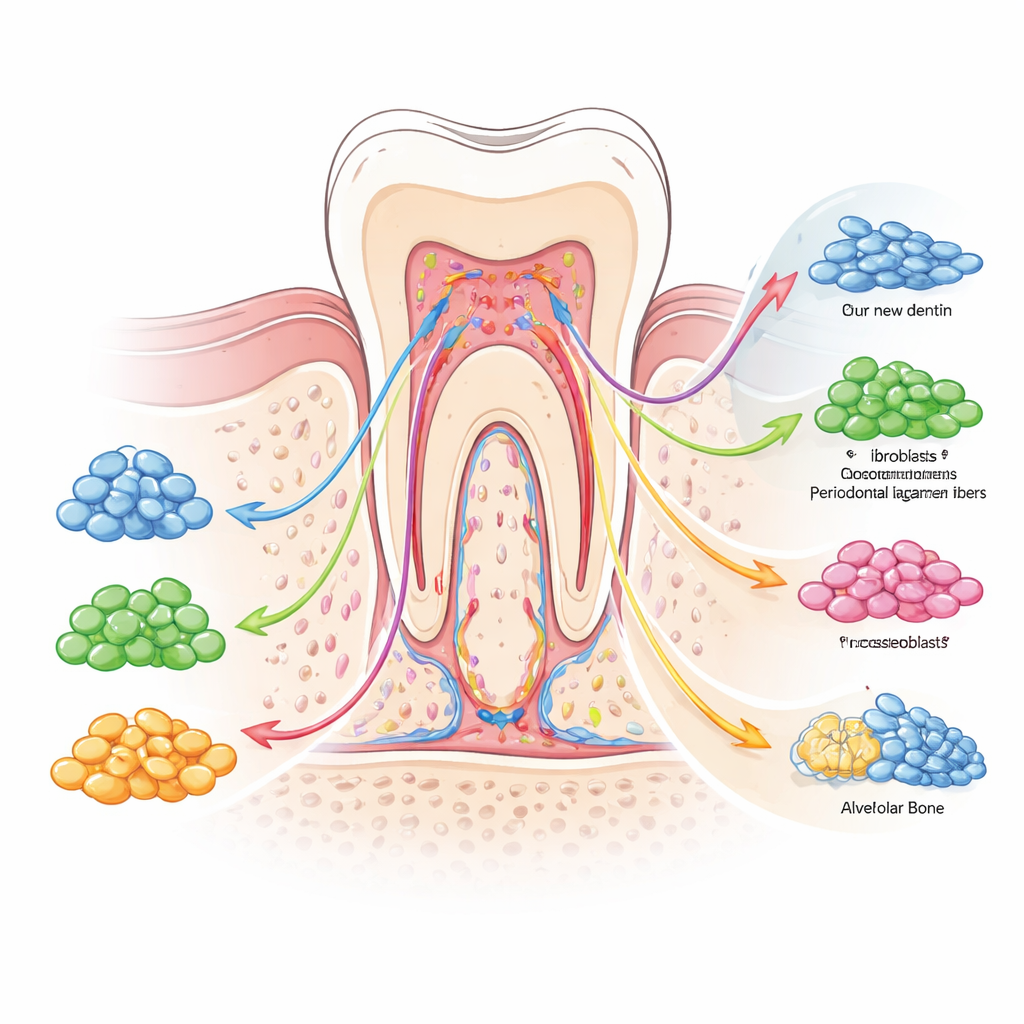
Un message clé de la revue est que l’hétérogénéité existe non seulement entre les différents types de cellules souches, mais aussi au sein de chacun d’eux. De nouvelles techniques comme le séquençage ARN unicellulaire permettent de profiler des milliers de cellules individuelles simultanément, révélant des sous-groupes avec une activité génique et des comportements distincts. Dans la pulpe dentaire, par exemple, les chercheurs ont cartographié plusieurs clusters : certains entretiennent le réservoir de réserve et pilotent la prolifération, d’autres sont prédisposés à la production de dentine, et d’autres encore tendent vers la formation de vaisseaux sanguins ou de cellules de type nerveux. Des sous-groupes similaires ont été identifiés dans les cellules souches du ligament parodontal, de l’os mandibulaire, des dents de lait et des gencives. Des marqueurs moléculaires à la surface cellulaire et dans le noyau aident à distinguer ces sous-populations, qui diffèrent par leur capacité de croissance, leur profil de vieillissement et leur réactivité aux forces mécaniques, à l’inflammation ou à l’attaque bactérienne.
Signaux et interrupteurs qui façonnent le comportement des cellules souches
Les auteurs soulignent que cette diversité n’est pas aléatoire. Elle est organisée par un réseau de signaux biochimiques et d’interrupteurs « épigénétiques » qui agissent comme des feux de circulation et des panneaux routiers pour le destin cellulaire. Des voies guidées par les protéines morphogénétiques osseuses (BMP), les signaux Wnt et le facteur de transformation bêta (TGF-β) poussent les cellules vers la construction de tissus durs comme la dentine et l’os, tandis que d’autres voies, dont Notch et PI3K/AKT, contribuent à maintenir un équilibre entre cellules souches et progénitrices. Parallèlement, des marques chimiques sur l’ADN et les protéines de condensation ajustent l’accès aux gènes, prédisposant certaines cellules à une réponse rapide en cas de lésion. Les forces mécaniques liées à la mastication, les molécules inflammatoires issues d’une infection et les signaux provenant des vaisseaux sanguins ou des nerfs voisins orientent également l’équilibre vers la réparation, la cicatrisation ou la dégradation. Ensemble, ces couches de contrôle forment un système de réparation flexible, mais parfois imprévisible.
Ce que cela signifie pour les soins dentaires futurs
Pour le non-spécialiste, la conclusion principale est que la régénération des dents et des gencives n’est plus de la science-fiction, mais que son succès dépendra de la gestion de la diversité des cellules souches plutôt que de son ignorance. La revue soutient que savoir quelles sous-populations spécifiques construisent la dentine, le ligament, l’os ou les nerfs — et quels signaux les guident — aidera les chercheurs à affiner la sélection cellulaire, les biomatériaux et les indices médicamenteux pour obtenir des résultats prévisibles. Dans le même temps, les auteurs mettent en garde que la plupart des cartes détaillées proviennent d’études animales et de cultures en laboratoire, et que le bruit technique peut brouiller l’image. Ils plaident pour des approches intégrées « multi-omiques » sur des tissus humains, une meilleure standardisation et des tests rigoureux in vivo. En définitive, décoder l’hétérogénéité des cellules souches mésenchymateuses dentaires pourrait permettre aux dentistes de passer du remplacement de structures endommagées par des matériaux inertes à la régénération réelle de dents vivantes et fonctionnelles et de leurs tissus de soutien.
Citation: Fu, H., Chen, P., Wu, Z. et al. Research progress in heterogeneity of dental mesenchymal stem cells. Int J Oral Sci 18, 31 (2026). https://doi.org/10.1038/s41368-026-00433-8
Mots-clés: cellules souches dentaires, régénération dentaire, réparation parodontale, séquençage unicellulaire, ingénierie des tissus buccaux