Clear Sky Science · zh
人类空肠类器官在肥胖中的表征;用于研究GLP-1细胞的模型
为何微型肠道模型对体重和血糖重要
肥胖和2型糖尿病通常被视为脂肪组织或胰腺的问题,但肠道也在其中扮演着重要而低调的角色。小肠内的细胞会释放有助于控制食欲和血糖的激素。其中最重要的之一是GLP‑1,这也是当今强效减重药物所模拟的激素。本研究从严重肥胖者(有无糖尿病)体内构建实验室培养的迷你肠段,以便在体外观察其产生GLP‑1的细胞如何表现。
从患者组织构建微型肠道
在对严重肥胖者实施胃旁路手术时,外科医生可以安全取下小肠空肠(小肠中段,负责吸收大量营养)的一小块组织样本。研究者从这些组织碎片中分离出位于肠隐窝的干细胞,并将其培养成称为人类空肠类器官的三维结构。这些球状细胞簇重现了肠道上皮中常见的主要细胞类型。研究团队分别来自三组患者建立了类器官:肥胖但血糖正常者、肥胖且糖尿病前期者以及肥胖且已确诊2型糖尿病者。
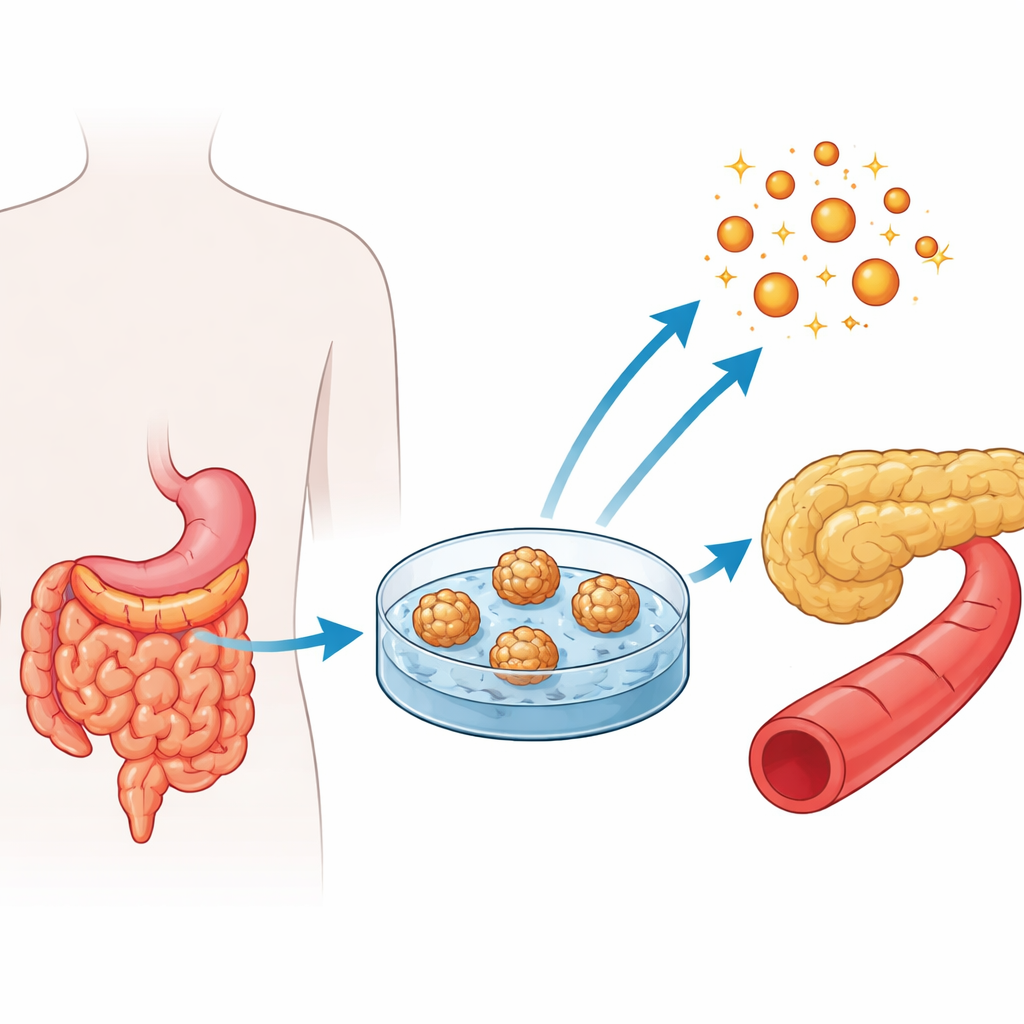
验证肠道模型在形态和功能上与真实组织相似
为了有用,微型肠道必须类似于天然组织。研究者利用荧光标记和蛋白质测定确认,类器官中含有分裂的细胞和预期的多种专门化肠细胞,包括吸收细胞、分泌黏液的细胞、潘氏细胞(支持干细胞并参与宿主防御)以及稀有的分泌激素的肠内分泌细胞。这些不同细胞类型的关键标志物在三组患者的类器官中水平相近,表明肥胖、糖尿病前期和糖尿病并未阻碍在培养中形成基本的肠道结构。
聚焦产生激素的细胞
团队进一步放大观察产生GLP‑1及其他肠激素的细胞。他们寻找将未分化肠细胞驱动为激素产生细胞的基因开关以及激素本身。类器官表达了这些分化开关并产生了包括GLP‑1、GIP和PYY在内的多种激素,其表达模式与人体空肠中所见相似。重要的是,产生GLP‑1的细胞密度以及将较大前体蛋白切割为活性GLP‑1所需的分子机械在供体是否血糖正常、处于糖尿病前期或已患2型糖尿病之间大体相当。这意味着即使供体有严重代谢疾病,实验室培养组织形成GLP‑1细胞的基本能力仍然被保留。
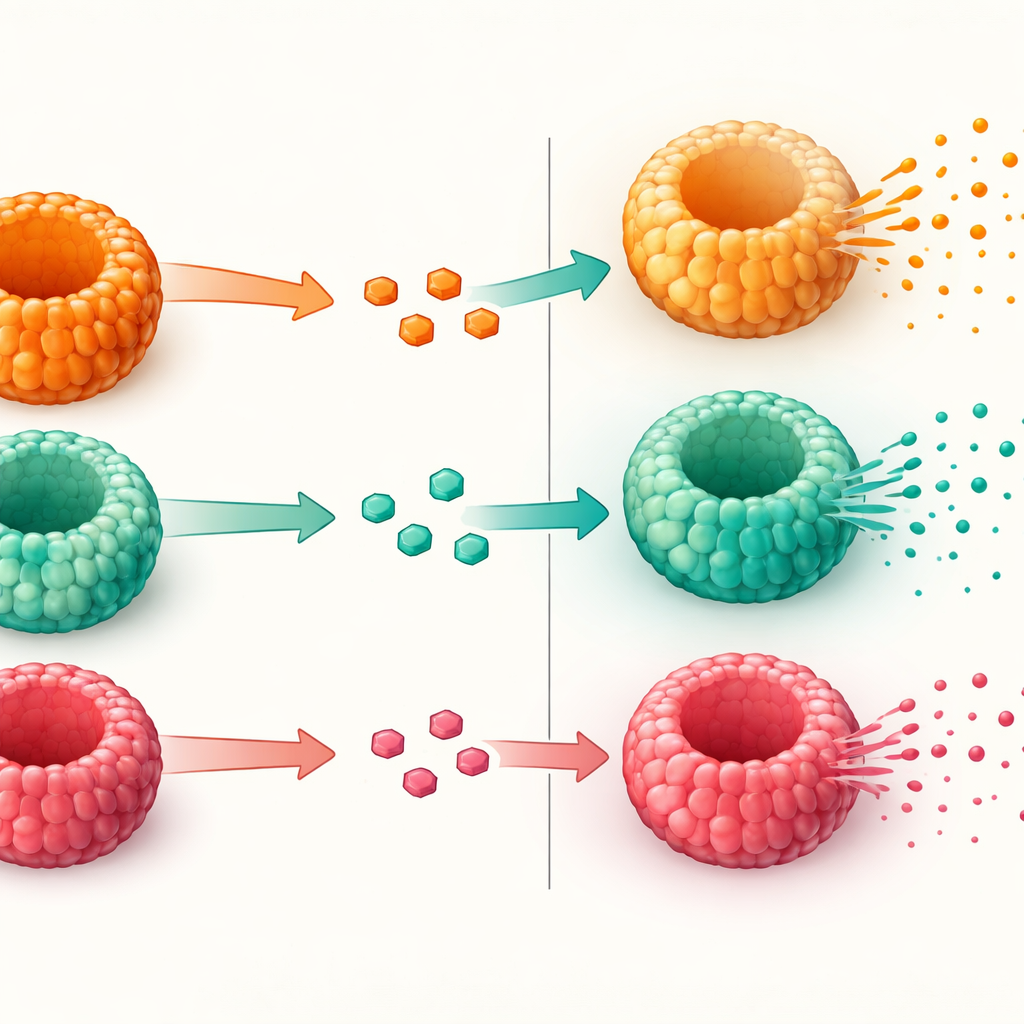
测试这些细胞释放GLP-1的能力
在确认微型肠道包含适当的GLP‑1细胞后,研究者测试了这些细胞在遇糖刺激时释放激素的能力。他们先用一种促使干细胞走向分泌命运的化合物提高激素产生细胞的比例。随后将类器官置于含有中等或非常高葡萄糖浓度的溶液中,类似餐后肠道可能出现的情形。所有类器官——无论供体代谢状态如何——在高葡萄糖条件下均释放出活性GLP‑1。然而,来自肥胖并伴2型糖尿病患者的类器官,其GLP‑1释放的增强幅度低于来自肥胖但血糖正常者的类器官。参与糖感知和激素释放的基因大体存在,提示问题并非出在生成GLP‑1或形成这些细胞上,而是在分泌的最终步骤上出现了障碍。
对未来治疗的意义
这项工作表明,人类空肠类器官是一个稳健的、源自患者的模型,可用于研究肥胖与糖尿病中肠激素细胞的功能。尽管产生GLP‑1的细胞很稀少,但在这一简化体系中能够被详尽研究。研究显示,在2型糖尿病患者中,这些细胞仍能形成并合成GLP‑1,但在遭遇糖刺激时释放能力下降。该差异很重要:它表明,提升现存肠激素细胞的分泌性能,而不仅仅是增加其数量,可能是改善血糖控制和支持体重减轻的新疗法的有希望方向。
引用: Osinski, C., Martinez-Oca, P., Moret, D. et al. Characterization of jejunal enteroids in human obesity; a model for studying GLP-1 cells. Int J Obes 50, 916–927 (2026). https://doi.org/10.1038/s41366-026-02024-3
关键词: GLP-1, 类器官, 肥胖, 2型糖尿病, 肠激素