Clear Sky Science · zh
氟哌啶醇在小鼠和人源脊髓性肌萎缩模型中诱导神经保护并增强神经肌肉功能
把一种精神科药物变成神经保护剂
脊髓性肌萎缩(SMA)是一种遗传性疾病,会削弱肌肉并可能在儿童期致命。现有疗法对许多患者有帮助,但给药复杂、费用高昂,且无法完全恢复肌肉与神经的健康。本文提出了一个简单却有力量的问题:是否可以将长期使用的抗精神病药物氟哌啶醇以远低于精神科剂量的用量重新定位,用来保护SMA受累的神经细胞与肌肉,从而提供一种更易获得且可互补的选择?
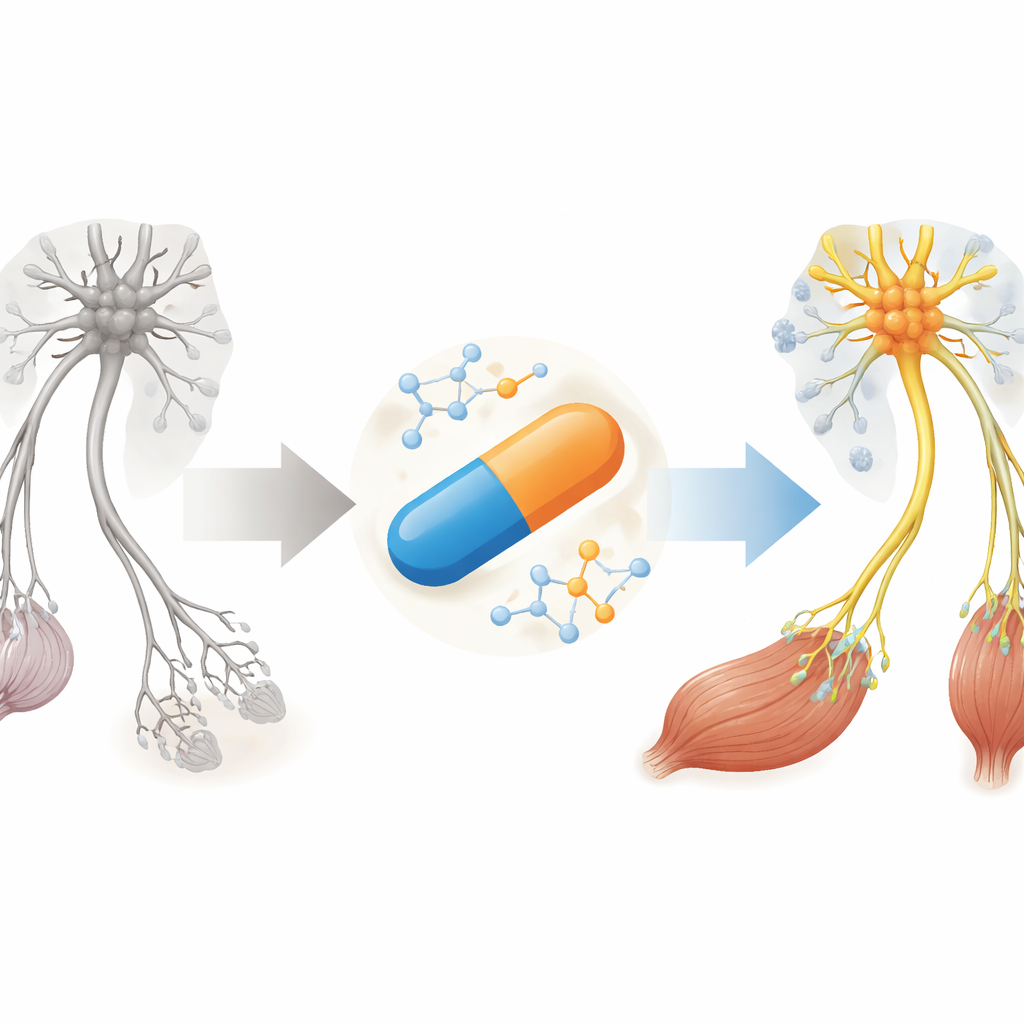
为何肌肉萎缩性疾病需要新方案
SMA由一种称为SMN的蛋白不足引起,运动神经元——即控制运动的神经细胞——需要该蛋白才能存活。当前药物几乎全部集中在通过提升神经系统中的SMN,通常需要脊髓注射或昂贵的基因疗法。然而,即使经过数月治疗,许多患者在神经与肌肉之间的微小接触点——神经肌肉接头处仍存在缺陷。作者认为,未来的治疗不仅要更广泛地提高体内SMN水平,还要平抑有害炎症并直接支持肌肉与接头的健康。
在小鼠与人类细胞中测试氟哌啶醇
该团队此前在果蝇和人源细胞中筛选已获批药物,发现氟哌啶醇能改善备用基因SMN2的剪接,从而增加SMN蛋白。在本研究中,他们从出生后不久开始给一种重度SMA小鼠系低剂量氟哌啶醇。与未处理的同窝小鼠相比,受试小鼠寿命更长、体重增加更好,平衡、姿势和肢体力量也有所改善。同时间,研究人员用干细胞方法从SMA患者建立了运动神经元与肌肉细胞。当这些人源细胞暴露于极低剂量的氟哌啶醇时,更多运动神经元得以存活,树突分支网络更丰富,在共培养中形成的肌纤维更大且连接更完善。
保护神经、抚慰支持细胞并强化肌肉
在小鼠脊髓内,氟哌啶醇将SMN蛋白提高了约一半,而在腿部肌肉中几乎翻倍。受治动物的运动神经元数量更多,表现出较少的细胞程序性死亡分子标志。基因活性分析显示,数百条与RNA加工、细胞存活和突触结构相关的基因表达朝更健康的方向转变,其中包括许多已知的SMN依赖靶标。重要的是,氟哌啶醇还降低了过度活化的星形胶质细胞标记,并使小胶质细胞——大脑的免疫细胞——呈现更平静、更休眠的形态。在肌肉中,脆弱股肌的肌纤维长得更大,更多神经肌肉接头实现了充分的神经支配并正确成熟,表明神经与肌肉之间的通讯更强且更可靠。
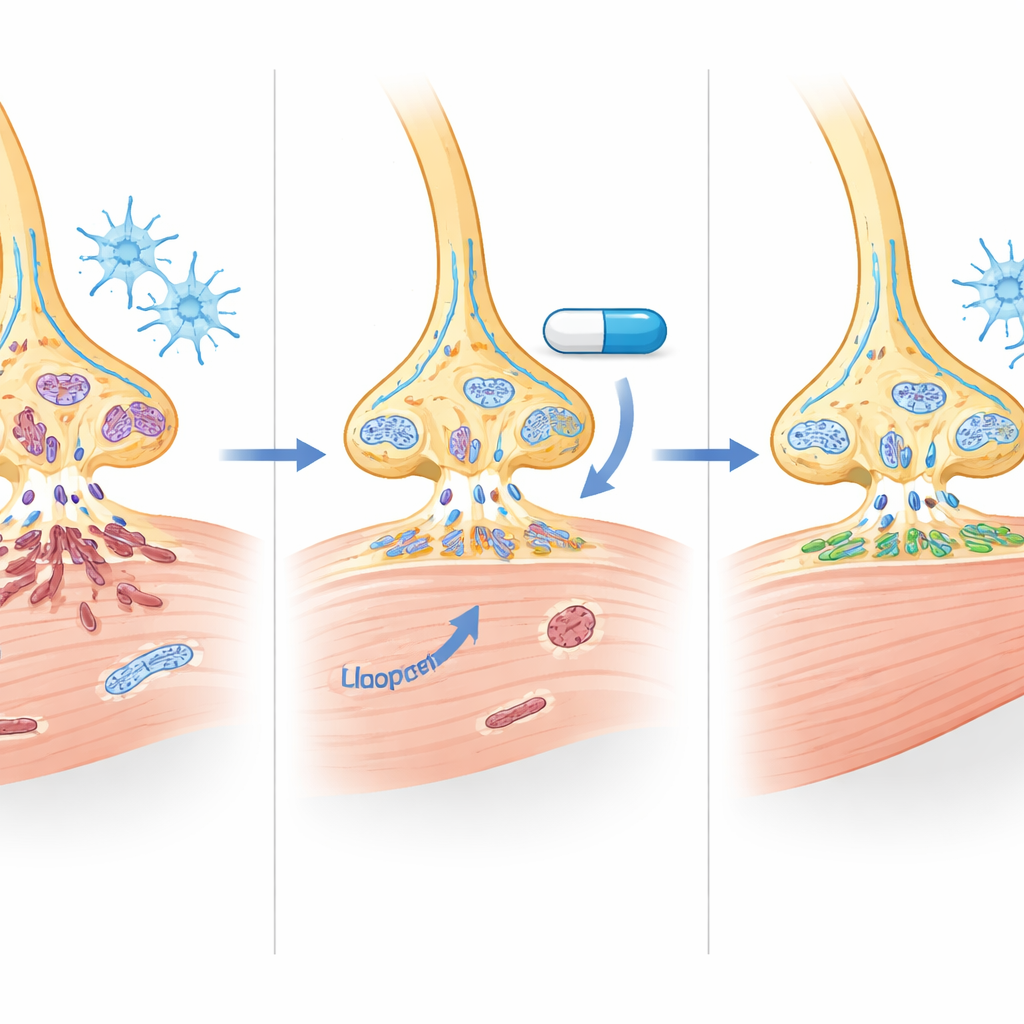
关于药物作用机制的线索
氟哌啶醇以阻断多巴胺D2受体的精神科作用最为人知,但本研究使用的低剂量并未在小鼠脑、脊髓或患者来源的神经元中显著改变这些受体。相反,数据指向双重作用:SMN蛋白的小幅但具有意义的增加,以及对RNA加工、细胞凋亡通路、炎症和线粒体功能等更广泛的“家务性”效应。一些与能量产生和肌肉脂质代谢相关的基因也发生了改变,这提示该药可能部分纠正SMA肌肉中观察到的代谢紊乱,尽管对线粒体的确切影响仍需后续研究。
这对SMA患者可能意味着什么
对非专业读者来说,核心信息是:一种陈旧且价格低廉的药物——氟哌啶醇——在经过谨慎选择的低剂量下,可能有助于维持SMA中的神经—肌肉连接,而不仅仅是改变情绪或行为。在小鼠和人源细胞模型中,它延长了运动神经元的存活、改善了肌肉体积,并增强了驱动运动的微观接头,同时抑制了有害的炎症。尽管仍需大量测试,特别是关于长期安全性以及如何与现有SMA疗法最佳配合,这项研究表明氟哌啶醇最终可能成为一种实用的补充或替代治疗,使现有在力量和独立性方面取得的改善更持久。
引用: Menduti, G., Perez-Gomez, R., Berenger-Currias, N. et al. Haloperidol induces neuroprotection and enhances neuromuscular function in both murine and human models of spinal muscular atrophy. Exp Mol Med 58, 1216–1229 (2026). https://doi.org/10.1038/s12276-026-01689-0
关键词: 脊髓性肌萎缩, 药物再利用, 氟哌啶醇, 运动神经元, 神经肌肉接头