Clear Sky Science · de
Haloperidol induziert Neuroprotektion und verbessert die neuromuskuläre Funktion in Maus‑ und Humanmodellen der spinalen Muskelatrophie
Ein Psychopharmakon als Nervenschutzmittel
Die spinale Muskelatrophie (SMA) ist eine genetische Erkrankung, die Muskeln schwächt und im Kindesalter tödlich verlaufen kann. Bestehende Therapien helfen vielen Patientinnen und Patienten, sind aber schwer zugänglich, sehr teuer und stellen die Muskel‑ und Nervengesundheit nicht vollständig wieder her. Diese Studie stellt eine einfache, aber folgenschwere Frage: Kann Haloperidol, ein seit langem eingesetztes Antipsychotikum, in deutlich niedrigeren Dosen umgenutzt werden, um die in SMA betroffenen Nervenzellen und Muskeln zu schützen und so eine leichter zugängliche und ergänzende Behandlungsoption zu bieten?
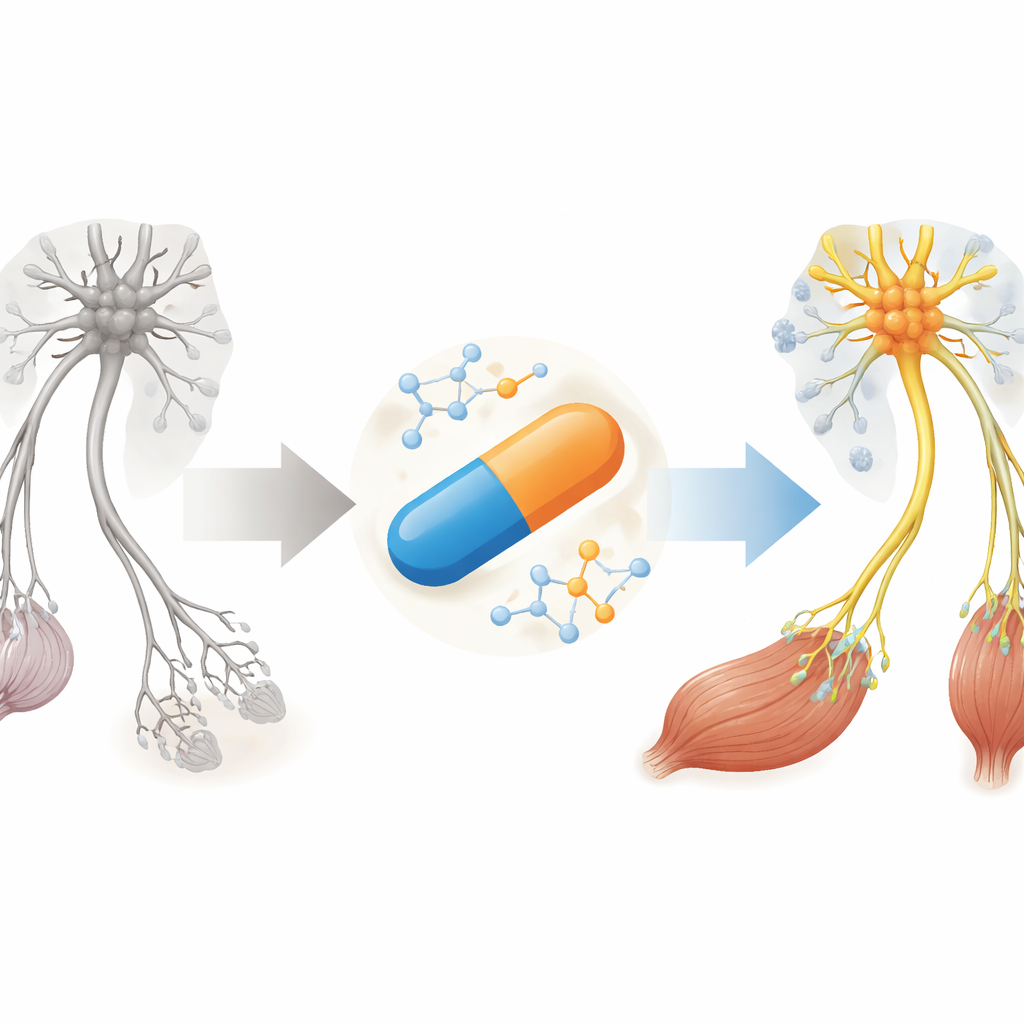
Warum eine muskelschwächende Krankheit neue Optionen braucht
SMA wird durch einen Mangel an einem Protein namens SMN verursacht, das Motoneurone—die Nervenzellen, die Bewegung steuern—zum Überleben benötigen. Aktuelle Medikamente zielen fast ausschließlich darauf ab, SMN im Nervensystem zu erhöhen, häufig über Injektionen in den Wirbelkanal oder teure Gentherapien. Dennoch zeigen viele Patientinnen und Patienten auch nach monatelanger Behandlung weiterhin Defekte an der neuromuskulären Synapse, den winzigen Kontaktstellen, an denen Nerven mit Muskeln kommunizieren. Die Autorinnen und Autoren argumentieren, dass künftige Therapien nicht nur SMN‑Spiegel weiter im Körper anheben müssen, sondern auch schädliche Entzündungsreaktionen dämpfen und direkt Muskulatur und Synapsen stärken sollten.
Prüfung von Haloperidol in Mäusen und menschlichen Zellen
Das Team hatte zuvor zugelassene Wirkstoffe in Fruchtfliegen und menschlichen Zellen gescreent und festgestellt, dass Haloperidol die Verarbeitung des Ersatzg ens SMN2 verbessern und so die SMN‑Proteinmenge erhöhen kann. In dieser Studie verabreichten sie einer schweren SMA‑Mauslinie ab dem frühen Neugeborenenalter eine niedrige Dosis Haloperidol. Die behandelten Mäuse lebten länger, nahmen mehr Gewicht zu und zeigten bessere Balance, Haltung und Gliedmaßenstärke als unbehandelte Wurfgeschwister. Parallel dazu züchteten die Forschenden Motoneurone und Muskelzellen aus SMA‑Patienten mittels Stammzellverfahren. Wurden diese menschlichen Zellen winzigen Haloperidolmengen ausgesetzt, überlebten mehr Motoneurone, bildeten reichere Verzweigungsnetze und erzeugten in der Ko‑Kultur größere, besser verbundene Muskelfasern.
Nerven schützen, Stütz-Zellen beruhigen und Muskeln stärken
Im Rückenmark der Mäuse erhöhte Haloperidol das SMN‑Protein um etwa die Hälfte und verdoppelte es nahezu in Beinmuskeln. Motoneurone in behandelten Tieren waren zahlreicher und wiesen weniger molekulare Zeichen für programmierter Zelltod auf. Genexpressionsuntersuchungen zeigten, dass hunderte Transkripte, die mit RNA‑Verarbeitung, Zellüberleben und Synapsenstruktur verknüpft sind, sich in Richtung eines gesünderen Musters verschoben, darunter viele bekannte SMN‑abhängige Zielgene. Wichtig ist, dass Haloperidol auch Marker überaktiver Astrozyten reduzierte und Mikroglia—die Immunzellen des Gehirns—zu einer ruhigeren, eher ruhenden Form umgestaltete. In der Muskulatur wuchsen Fasern eines besonders anfälligen Oberschenkelmuskels und mehr neuromuskuläre Synapsen waren vollständig innerviert und korrekt gereift, was auf eine stärkere und verlässlichere Kommunikation zwischen Nerven und Muskeln hinweist.
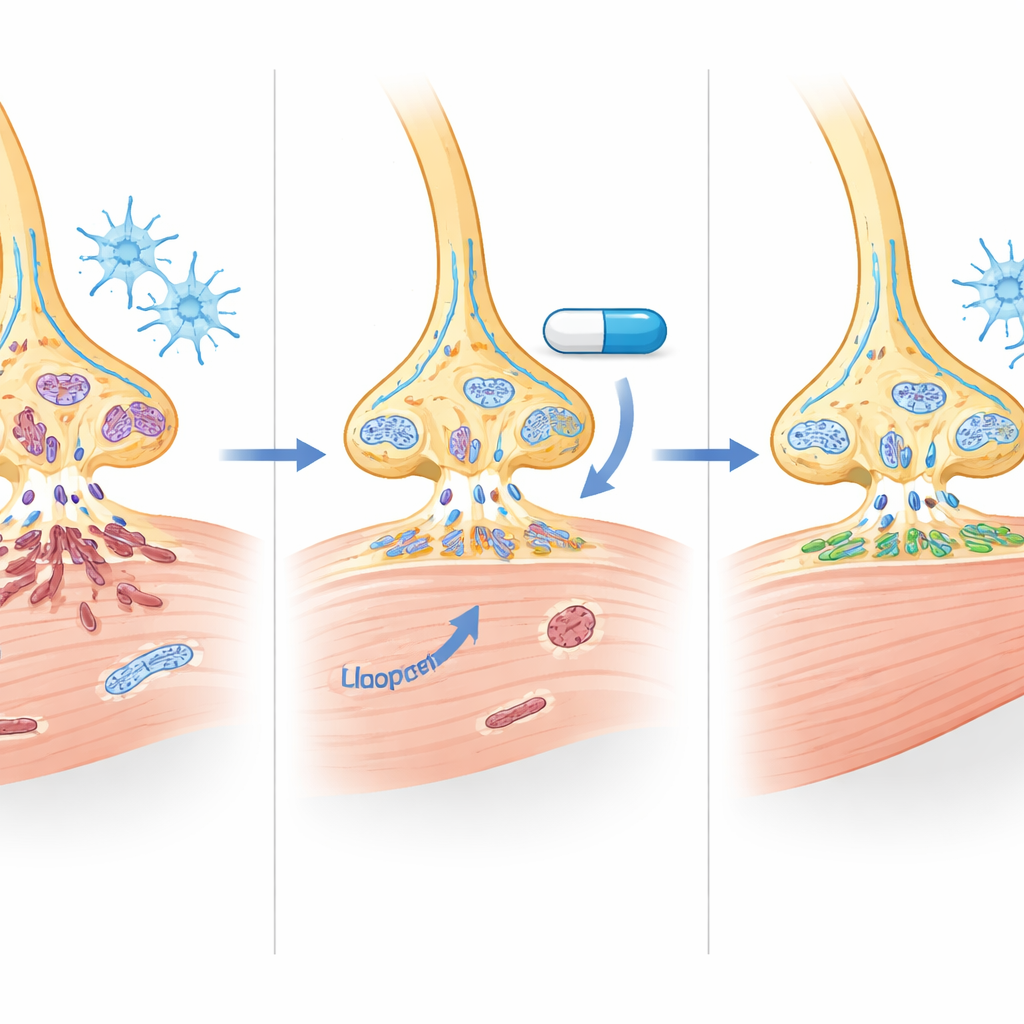
Hinweise auf die Wirkungsweise hinter den Kulissen
Haloperidol ist vor allem für die Blockade von Dopamin‑D2‑Rezeptoren in psychiatrischen Dosen bekannt, doch die hier verwendeten niedrigen Dosen veränderten diese Rezeptoren in Mausgehirn, Rückenmark oder patientenabgeleiteten Neuronen nicht messbar. Stattdessen deuten die Daten auf eine doppelte Wirkung hin: moderate, aber bedeutsame Erhöhungen des SMN‑Proteins zusammen mit breit angelegten "Haushalts"‑Effekten auf RNA‑Verarbeitung, Zelltodwege, Entzündung und Mitochondrienfunktion. Einige Gene, die mit Energieproduktion und Fettstoffwechsel in Muskelgewebe verknüpft sind, verschoben sich ebenfalls, was darauf hindeutet, dass das Medikament möglicherweise teilweise die metabolischen Störungen in SMA‑Muskeln korrigiert—wobei die genaue Auswirkung auf Mitochondrien künftige Untersuchungen erfordert.
Was das für Menschen mit SMA bedeuten könnte
Für Laien lautet die Kernbotschaft: Ein altes, preiswertes Medikament—Haloperidol—könnte bei sorgfältig gewählten niedrigen Dosen helfen, die Verbindung zwischen Nerven und Muskeln bei SMA zu erhalten, statt nur Stimmung oder Verhalten zu verändern. In Maus‑ und menschlichen Zellmodellen verlängerte es das Überleben von Motoneuronen, verbesserte die Muskelgröße und stärkte die mikroskopischen Synapsen, die Bewegung antreiben, und dämpfte gleichzeitig schädliche Entzündungsreaktionen. Zwar bleibt Vieles zu prüfen, insbesondere zur Langzeitsicherheit und zur besten Kombination mit bestehenden SMA‑Therapien, doch die Arbeit legt nahe, dass Haloperidol schließlich als praktikable Ergänzung oder Alternative dienen könnte, um erzielte Verbesserungen von Kraft und Unabhängigkeit nachhaltiger zu machen.
Zitation: Menduti, G., Perez-Gomez, R., Berenger-Currias, N. et al. Haloperidol induces neuroprotection and enhances neuromuscular function in both murine and human models of spinal muscular atrophy. Exp Mol Med 58, 1216–1229 (2026). https://doi.org/10.1038/s12276-026-01689-0
Schlüsselwörter: spinale Muskelatrophie, Wiederverwendung von Medikamenten, Haloperidol, Motoneurone, neuromuskuläre Synapse