Clear Sky Science · fr
L'halopéridol induit une neuroprotection et améliore la fonction neuromusculaire dans des modèles murins et humains d'atrophie musculaire spinale
Transformer un médicament psychiatrique en protecteur nerveux
L'atrophie musculaire spinale (AMS) est une maladie génétique qui affaiblit les muscles et peut être mortelle pendant l'enfance. Les traitements existants aident de nombreux patients mais sont difficiles à administrer, très coûteux et ne restaurent pas entièrement la santé musculaire et nerveuse. Cette étude pose une question simple mais puissante : l'halopéridol, un antipsychotique utilisé depuis longtemps, pourrait‑il être réutilisé à des doses beaucoup plus faibles pour protéger les cellules nerveuses et les muscles touchés par l'AMS, offrant une option plus accessible et complémentaire ?
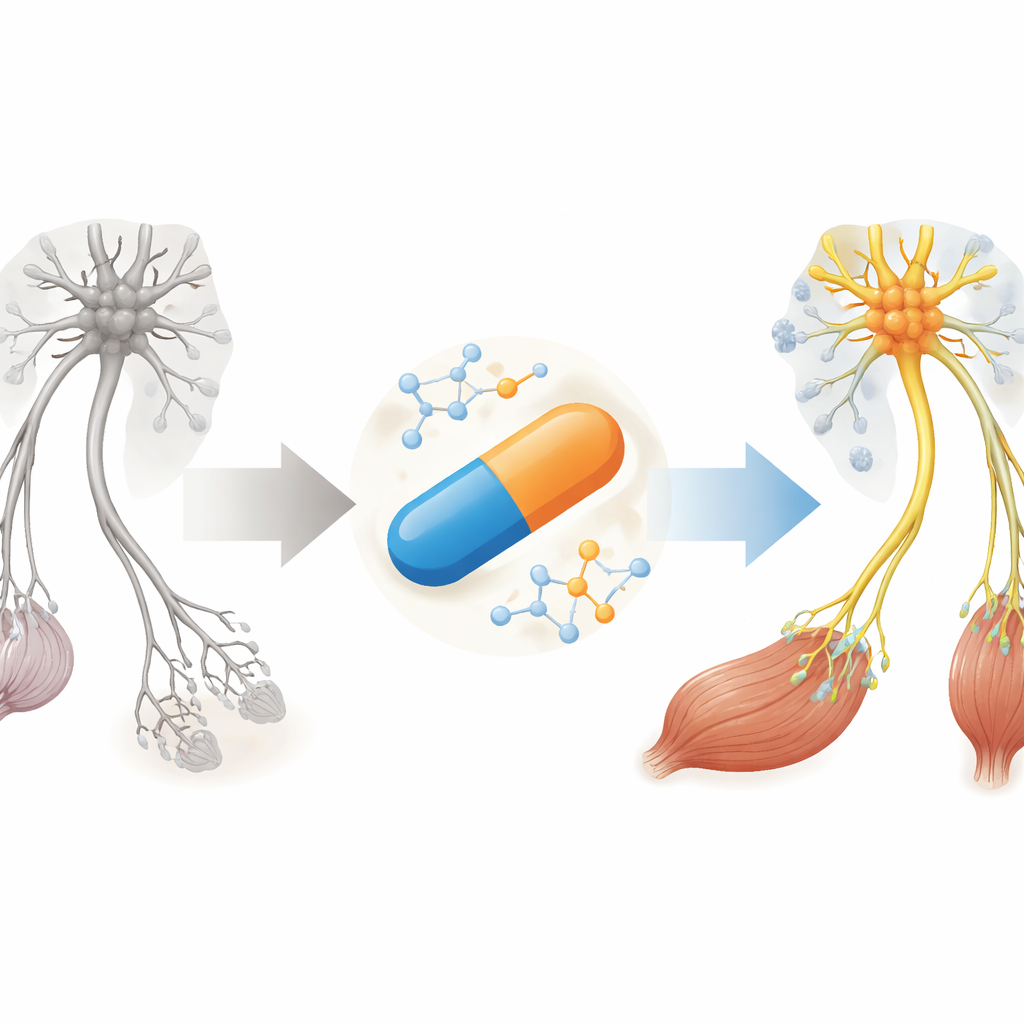
Pourquoi une maladie de fonte musculaire a besoin de nouvelles options
L'AMS est provoquée par une insuffisance d'une protéine appelée SMN, dont les motoneurones — les cellules nerveuses qui contrôlent le mouvement — ont besoin pour survivre. Les médicaments actuels visent presque exclusivement à augmenter le SMN dans le système nerveux, souvent par injections spinales ou thérapies géniques coûteuses. Pourtant, de nombreux patients présentent encore des anomalies au niveau de la jonction neuromusculaire, ces minuscules points de contact où les nerfs communiquent avec les muscles, même après des mois de traitement. Les auteurs soutiennent que les traitements futurs doivent non seulement élever les niveaux de SMN plus largement dans l'organisme, mais aussi apaiser l'inflammation nuisible et soutenir directement la santé des muscles et des jonctions.
Tester l'halopéridol chez la souris et dans des cellules humaines
L'équipe avait auparavant testé des médicaments approuvés chez la drosophile et dans des cellules humaines et constaté que l'halopéridol pouvait améliorer le traitement du gène de secours SMN2, augmentant ainsi la protéine SMN. Dans cette étude, ils ont administré une faible dose d'halopéridol à une souche murine sévère d'AMS dès la période néonatale. Les souris traitées ont vécu plus longtemps, pris plus de poids et montré un meilleur équilibre, une meilleure posture et une plus grande force des membres que leurs congénères non traitées. Parallèlement, les chercheurs ont développé des motoneurones et des cellules musculaires à partir de patients atteints d'AMS en utilisant des méthodes à partir de cellules souches. Lorsqu'elles ont été exposées à de très faibles quantités d'halopéridol, davantage de motoneurones ont survécu, formé des réseaux d'embranchements plus riches et produit des fibres musculaires plus grandes et mieux connectées en co‑culture.
Protéger les nerfs, calmer les cellules de soutien et renforcer les muscles
Dans la moelle épinière des souris, l'halopéridol a augmenté la protéine SMN d'environ la moitié et a presque doublé le SMN dans les muscles des pattes. Les motoneurones des animaux traités étaient plus nombreux et présentaient moins de signes moléculaires d'apoptose. Les analyses de l'activité génique ont révélé que des centaines de transcrits liés au traitement de l'ARN, à la survie cellulaire et à la structure des synapses évoluaient vers un profil plus sain, y compris de nombreuses cibles connues dépendantes de SMN. Fait important, l'halopéridol a également réduit des marqueurs d'astrocytes hyperactifs et reconfiguré les microglies — les cellules immunitaires du cerveau — vers une forme plus calme et au repos. Dans les muscles, les fibres d'un muscle de la cuisse vulnérable ont augmenté de taille, et davantage de jonctions neuromusculaires étaient pleinement innervées et correctement maturées, ce qui indique une communication nerveuse‑musculaire plus solide et plus fiable.
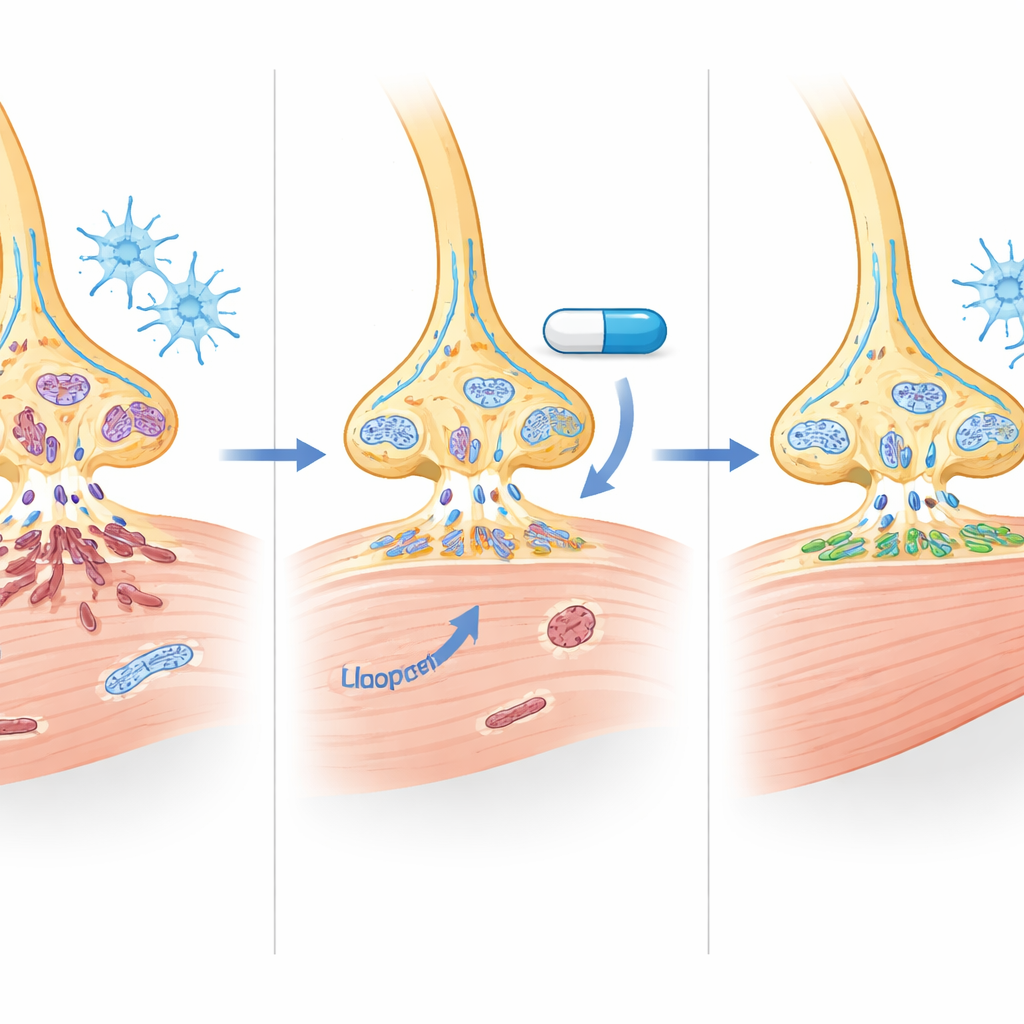
Indices sur le mécanisme d'action du médicament
L'halopéridol est surtout connu pour bloquer les récepteurs dopaminergiques D2 à des doses psychiatriques, mais les faibles doses utilisées ici n'ont pas modifié de façon mesurable ces récepteurs dans le cerveau, la moelle épinière ou les neurones dérivés de patients. Au lieu de cela, les données suggèrent une double action : des augmentations modestes mais significatives de la protéine SMN associées à des effets globaux de « maintenance » sur le traitement de l'ARN, les voies de mort cellulaire, l'inflammation et la fonction mitochondriale. Certains gènes liés à la production d'énergie et au métabolisme des lipides dans le muscle ont aussi été modifiés, ce qui laisse penser que le médicament pourrait corriger partiellement les perturbations métaboliques observées dans le muscle atteinte d'AMS, bien que l'impact exact sur les mitochondries nécessitera des travaux futurs.
Ce que cela pourrait signifier pour les personnes atteintes d'AMS
Pour le grand public, le message clé est qu'un médicament ancien et peu coûteux — l'halopéridol — pourrait, à des doses basses soigneusement choisies, aider à préserver la connexion nerf‑muscle dans l'AMS plutôt que de se limiter à modifier l'humeur ou le comportement. Chez la souris comme dans les modèles cellulaires humains, il a prolongé la survie des motoneurones, amélioré la taille musculaire et renforcé les jonctions microscopiques qui assurent le mouvement, tout en atténuant l'inflammation néfaste. Bien que de nombreuses questions restent à explorer, notamment la sécurité à long terme et la meilleure manière de l'associer aux thérapies AMS existantes, ces recherches suggèrent que l'halopéridol pourrait éventuellement devenir un traitement complémentaire ou alternatif pratique qui rend plus durables les bénéfices actuels en termes de force et d'autonomie.
Citation: Menduti, G., Perez-Gomez, R., Berenger-Currias, N. et al. Haloperidol induces neuroprotection and enhances neuromuscular function in both murine and human models of spinal muscular atrophy. Exp Mol Med 58, 1216–1229 (2026). https://doi.org/10.1038/s12276-026-01689-0
Mots-clés: atrophie musculaire spinale, réorientation thérapeutique, halopéridol, motoneurones, jonction neuromusculaire