Clear Sky Science · ar
الهالوبيريدول يحفِّز الحماية العصبية ويعزِّز الوظيفة العَصَبِيَّة-العضلية في نماذج الفأر والإنسان لضمور العضلات الشوكي
تحويل دواء نفسي إلى حاجز عصبي
ضمور العضلات الشوكي (SMA) هو مرض وراثي يضعف العضلات وقد يكون قاتلاً في مرحلة الطفولة. العلاجات الحالية تساعد كثيراً من المرضى لكنها صعبة التقديم ومكلِّفة جداً، ولا تعيد بالكامل صحة العضلات والأعصاب. يطرح هذا البحث سؤالاً بسيطاً لكنه ذي أثر كبير: هل يمكن إعادة توظيف الهالوبيريدول، وهو مضاد ذهان مستخدم منذ زمن طويل، بجرعات أقل بكثير ليحمي الخلايا العصبية والعضلات المتأثرة في SMA، مقدمًا خيارًا أكثر توفراً ومكملاً؟
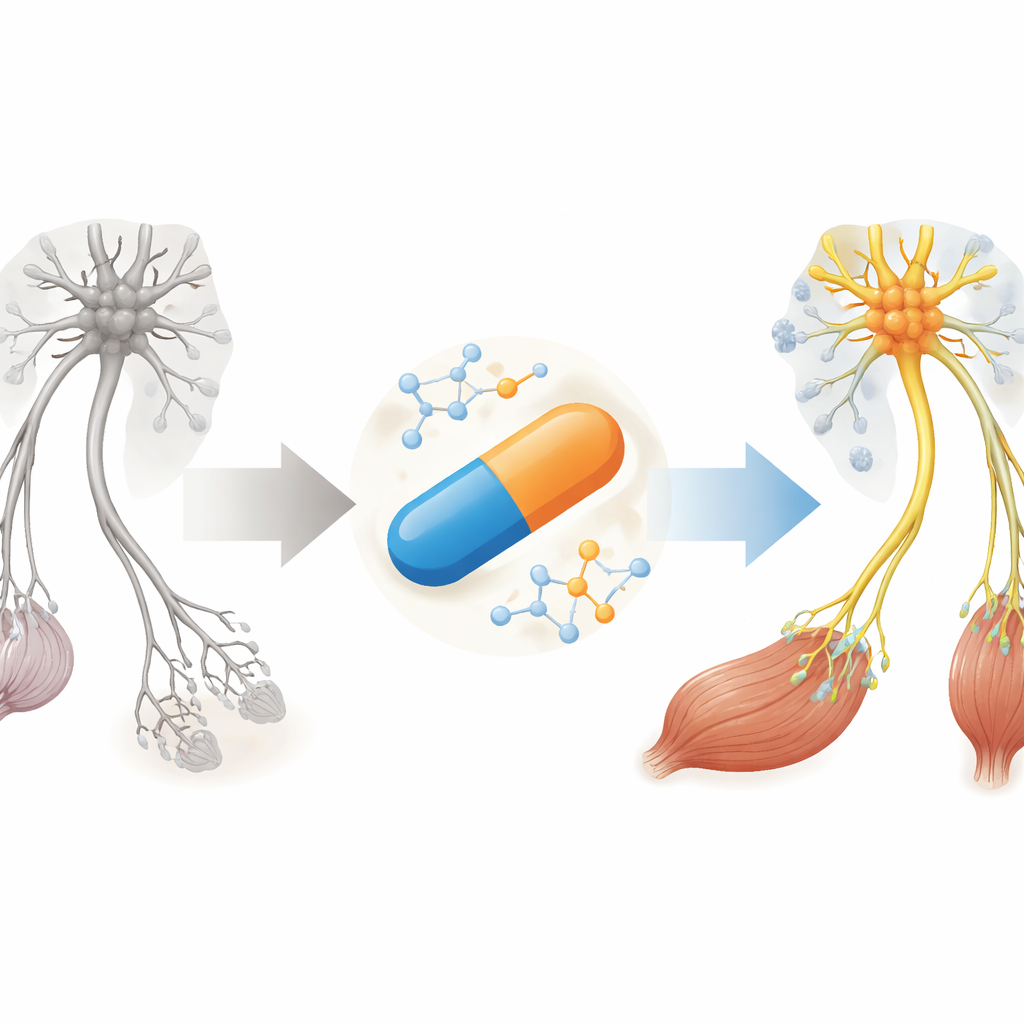
لماذا يحتاج مرض هدران العضلات إلى خيارات جديدة
ينجم SMA عن نقص في بروتين يُدعى SMN، وهو البروتين الذي تحتاجه الخلايا العصبية الحركية—خلايا الأعصاب المسؤولة عن الحركة—لتبقى على قيد الحياة. تركز الأدوية الحالية إلى حد كبير على رفع مستوى SMN في الجهاز العصبي، غالبًا عبر حقن فوق الجافية أو من خلال علاج جيني باهظ التكلفة. ومع ذلك، يظل كثير من المرضى يعانون من عيوب في الوَصل العَصَبِيّ-العضلي، نقاط الاتصال الدقيقة حيث تتواصل الأعصاب مع العضلات، حتى بعد شهور من العلاج. يجادل المؤلفون بأن العلاجات المستقبلية يجب ألا ترفع SMN في الجهاز العصبي فحسب، بل يجب أيضاً تهدئة الالتهاب الضار ودعم صحة العضلات والوصلات بشكل مباشر.
اختبار الهالوبيريدول في الفئران وخلايا الإنسان
سبق أن أجرى الفريق فحوصاً لأدوية مُصرَّح بها في ذبابة الفاكهة وخلايا بشرية، ووجد أن الهالوبيريدول يمكنه تحسين كيفية معالجة الجين الاحتياطي SMN2، مما يزيد بروتين SMN. في هذه الدراسة، أعطوا جرعة منخفضة من الهالوبيريدول لسلالة فأرية شديدة الإصابة بـSMA منذ الفترة بعد الولادة مباشرة. عاش الفئران المعالجة لفترة أطول، وزادت أوزانها، وأظهرت توازناً ووضعية وقوة أطراف أفضل من الأشقاء غير المعالجين. بالتوازي، نمَّى الباحثون خلايا عصبية حركية وخلايا عضلية مشتقة من مرضى SMA باستخدام طرق الخلايا الجذعية. عندما تعرَّضت هذه الخلايا البشرية لكميات ضئيلة من الهالوبيريدول، نجت خلايا عصبية حركية أكثر، وشكلت شبكات أغصان أغنى، ونمت ألياف عضلية أكبر وأكثر ترابطًا في الثقافة المشتركة.
حماية الأعصاب، تهدئة خلايا الدعم، وتقوية العضلات
داخل الحبل الشوكي للفأر، رفع الهالوبيريدول مستوى بروتين SMN بنحو نصف المقدار وضاعف تقريباً مستوى SMN في عضلات الساق. كانت الخلايا العصبية الحركية في الحيوانات المعالجة أكثر عدداً وأظهرت إشارات جزيئية أقل لانتحار الخلايا المبرمج. كشفت مسوح نشاط الجينات أن مئات الرسائل المرتبطة بمعالجة الحمض النووي الريبي والبقاء الخلوي وبنية المشابك اتجهت نحو نمط أكثر صحة، بما في ذلك العديد من الأهداف المعروفة المعتمدة على SMN. والأهم أن الهالوبيريدول قلل أيضاً من مؤشرات النجمية المفرطة النشاط وأعاد تشكيل الميكروغليا—خلايا المناعة في الدماغ—نحو حالة أكثر هدوءًا وسكونًا. في العضلات، نمت ألياف في عضلة فخذ معرضة للخطر بشكل أكبر وصارت أكبر، كما كانت المزيد من الوصلات العَصَبِيَّة-العضلية معصبة بالكامل وناضجة بشكل صحيح، ما يدل على تواصل أقوى وأكثر موثوقية بين الأعصاب والعضلات.
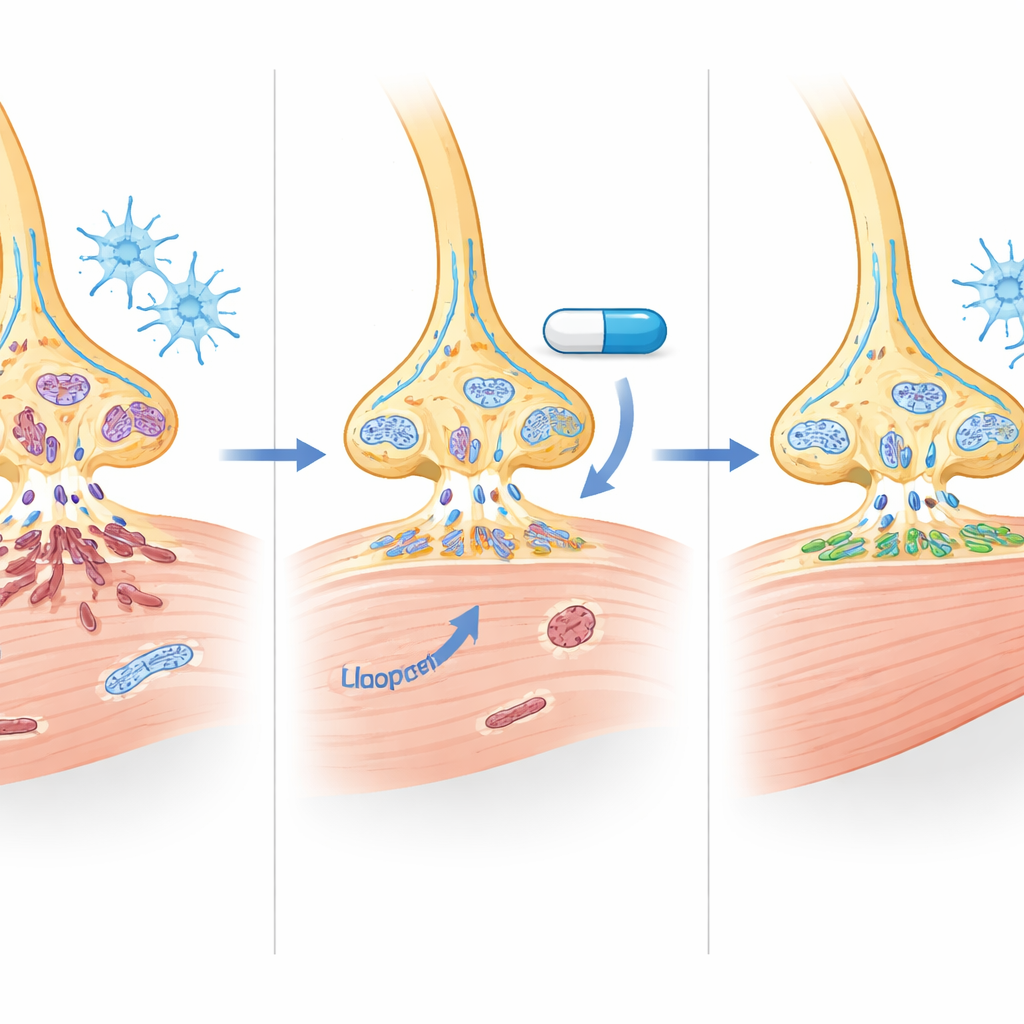
دلائل على كيفية عمل الدواء تحت الغطاء
يُعرف الهالوبيريدول أساسًا بقدرته على حجب مستقبلات الدوبامين من النوع D2 عند الجرعات النفسية، لكن الجرعات المنخفضة المستخدمة هنا لم تغير تلك المستقبلات بشكل يُقاس في مخ أو حبل شوكي الفأر أو في الخلايا العصبية المشتقة من المرضى. بدلاً من ذلك، تشير البيانات إلى فعل مزدوج: زيادات متواضعة لكنها ذات معنى في بروتين SMN إلى جانب تأثيرات أوسع «للصيانة» على معالجة الحمض النووي الريبي، ومسارات موت الخلايا، والالتهاب، ووظيفة الميتوكوندريا. تحركت بعض الجينات المرتبطة بإنتاج الطاقة والتعامل مع الدهون في العضلة أيضاً، مما يلمّح إلى أن الدواء قد يصحِح جزئياً الاضطرابات الأيضية الملحوظة في عضلات SMA، رغم أن التأثير الدقيق على الميتوكوندريا سيتطلب دراسات لاحقة.
ماذا قد يعني هذا للأشخاص المصابين بـSMA
للقارئ العام، الرسالة الأساسية هي أن دواء قديم وغير مكلف—الهالوبيريدول—قد يساعد، بجرعات منخفضة مختارة بعناية، في الحفاظ على الوصلة بين العصب والعضلة في SMA بدلاً من تغيير المزاج أو السلوك فقط. في نماذج الفأر والخلايا البشرية، مدد بقاء الخلايا العصبية الحركية، وحسَّن حجم العضلات، وعزز الوصلات المجهرية المسؤولة عن الحركة، وكل ذلك مع تخفيف الالتهاب الضار. بينما لا يزال هناك الكثير للاختبار، وخصوصًا فيما يتعلق بالسلامة على المدى الطويل وكيفية الجمع الأنسب مع علاجات SMA القائمة، تشير هذه الدراسة إلى أن الهالوبيريدول قد يصبح في نهاية المطاف إضافة عملية أو علاجًا بديلاً يعمق مكاسب القوة والاستقلالية الحالية.
الاستشهاد: Menduti, G., Perez-Gomez, R., Berenger-Currias, N. et al. Haloperidol induces neuroprotection and enhances neuromuscular function in both murine and human models of spinal muscular atrophy. Exp Mol Med 58, 1216–1229 (2026). https://doi.org/10.1038/s12276-026-01689-0
الكلمات المفتاحية: ضمور العضلات الشوكي, إعادة توظيف الأدوية, الهالوبيريدول, الخلايا العصبية الحركية, الوَصْل العَصَبِيّ-العضلي