Clear Sky Science · pt
Haloperidol induz neuroproteção e melhora a função neuromuscular em modelos murinos e humanos de atrofia muscular espinhal
Transformando um antipsicótico em um protetor de nervos
A atrofia muscular espinhal (AME) é uma doença genética que enfraquece os músculos e pode ser fatal na infância. Tratamentos existentes ajudam muitos pacientes, mas são de difícil administração, muito caros e não restauram completamente a saúde muscular e nervosa. Este estudo faz uma pergunta simples, porém poderosa: o haloperidol, um antipsicótico de uso antigo, pode ser reposicionado em doses muito menores para proteger as células nervosas e os músculos afetados na AME, oferecendo uma opção mais acessível e complementar?
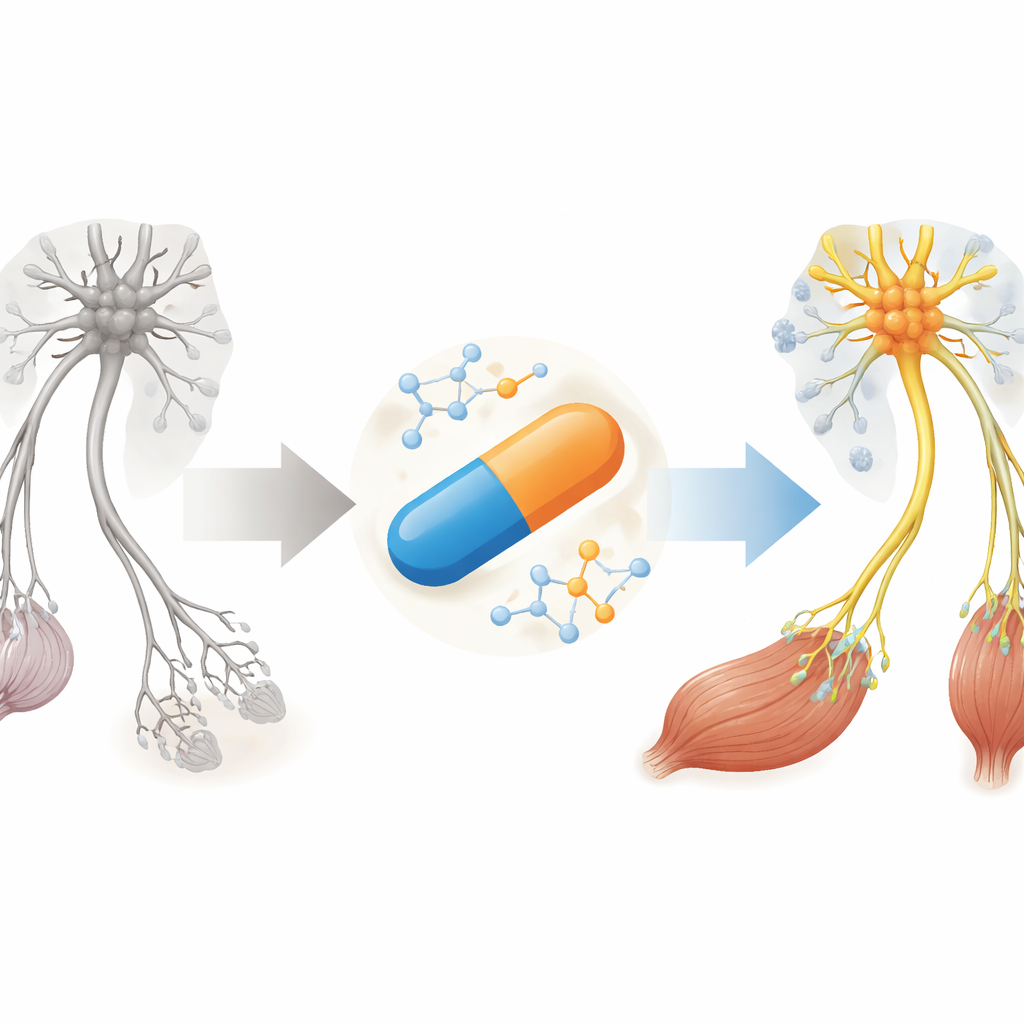
Por que uma doença que causa perda muscular precisa de novas opções
A AME é causada pela falta de uma proteína chamada SMN, da qual os neurônios motores — as células nervosas que controlam o movimento — precisam para sobreviver. Medicamentos atuais concentram‑se quase inteiramente em aumentar SMN no sistema nervoso, muitas vezes por injeções espinhais ou terapia gênica cara. Ainda assim, muitos pacientes continuam a apresentar defeitos na junção neuromuscular, os pequenos pontos de contato onde nervos se comunicam com músculos, mesmo após meses de terapia. Os autores argumentam que tratamentos futuros devem não só elevar os níveis de SMN de forma mais ampla no organismo, mas também reduzir a inflamação prejudicial e apoiar diretamente a saúde dos músculos e das junções.
Testando o haloperidol em camundongos e células humanas
A equipe previamente triou medicamentos aprovados em moscas da fruta e células humanas e descobriu que o haloperidol podia melhorar o processamento do gene suplente SMN2, aumentando a proteína SMN. Neste estudo, administraram uma baixa dose de haloperidol a uma linhagem de camundongo com AME severa desde logo após o nascimento. Os camundongos tratados viveram mais, ganharam mais peso e mostraram melhor equilíbrio, postura e força dos membros do que os irmãos não tratados. Em paralelo, os pesquisadores cultivaram neurônios motores e células musculares de pacientes com AME usando métodos de células‑tronco. Quando essas células humanas foram expostas a quantidades ínfimas de haloperidol, mais neurônios motores sobreviveram, formaram redes de ramos mais ricas e geraram fibras musculares maiores e melhor conectadas em co‑cultivo.
Protegendo nervos, acalmando células de suporte e fortalecendo músculos
Dentro da medula espinhal dos camundongos, o haloperidol elevou a proteína SMN em cerca de metade e quase dobrou a SMN nos músculos das pernas. Neurônios motores em animais tratados foram mais numerosos e mostraram menos sinais moleculares de morte celular programada. Levantamentos da atividade gênica revelaram que centenas de mensagens ligadas ao processamento de RNA, sobrevivência celular e estrutura das sinapses mudaram para um padrão mais saudável, incluindo muitos alvos conhecidos dependentes de SMN. Importante, o haloperidol também reduziu marcadores de astrócitos hiperativos e remodelou micróglias — as células imunes do cérebro — para um estado mais calmo e de repouso. Nos músculos, fibras em um músculo da coxa vulnerável cresceram mais e mais junções neuromusculares estavam totalmente inervadas e adequadamente maduras, indicando comunicação entre nervos e músculos mais forte e confiável.
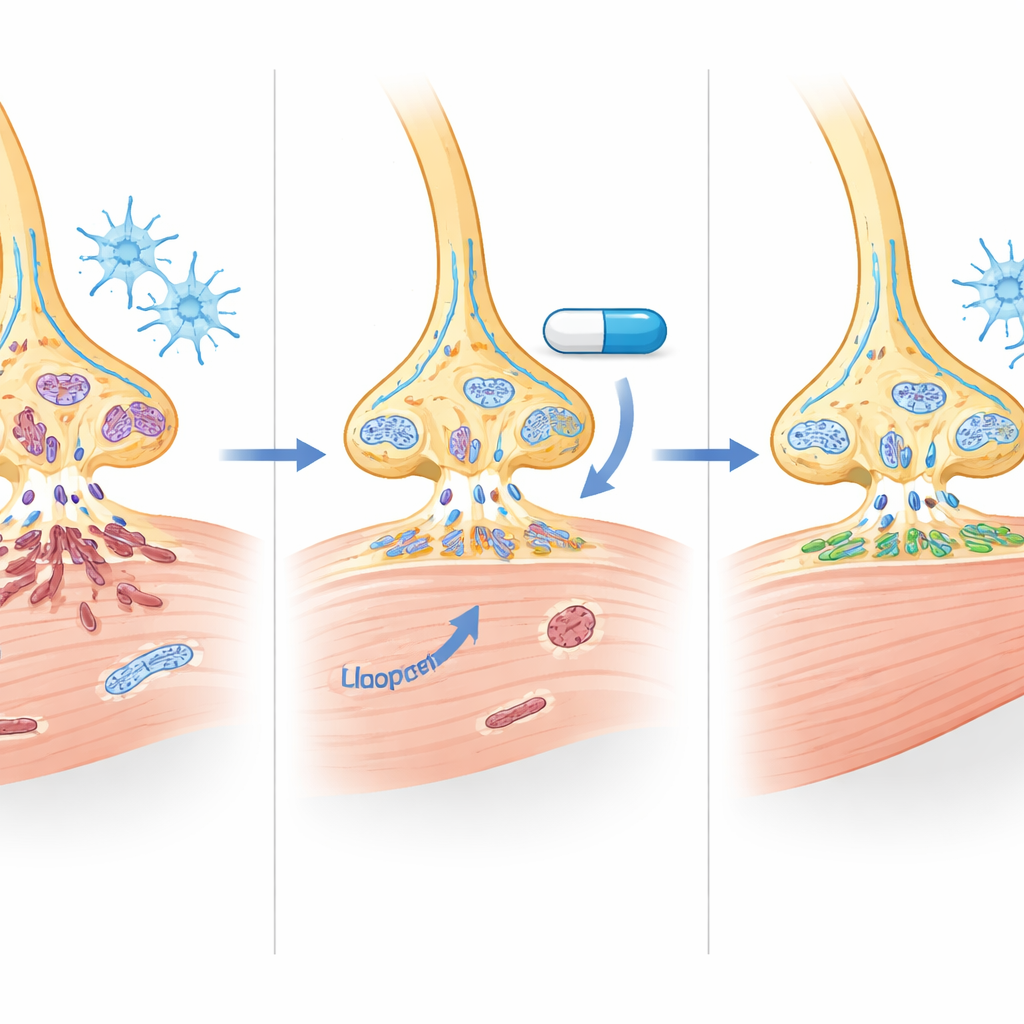
Pistas sobre como a droga age nos bastidores
O haloperidol é mais conhecido por bloquear receptores de dopamina D2 em doses psiquiátricas, mas as doses baixas usadas aqui não alteraram de forma mensurável esses receptores no cérebro, medula espinhal ou neurônios derivados de pacientes. Em vez disso, os dados apontam para uma ação dupla: aumentos modestos, porém significativos, na proteína SMN juntamente com efeitos ‘‘de manutenção’’ mais amplos sobre processamento de RNA, vias de morte celular, inflamação e função mitocondrial. Alguns genes ligados à produção de energia e ao manejo de lipídios no músculo também mudaram, sugerindo que a droga pode corrigir parcialmente as alterações metabólicas vistas no músculo da AME, embora o impacto exato sobre as mitocôndrias exija estudos futuros.
O que isso pode significar para pessoas com AME
Para leitores não especialistas, a mensagem principal é que um medicamento antigo e barato — o haloperidol — pode, em doses baixas cuidadosamente escolhidas, ajudar a preservar a conexão nervo‑músculo na AME em vez de apenas alterar o humor ou o comportamento. Em modelos de camundongo e de células humanas, prolongou a sobrevivência dos neurônios motores, melhorou o tamanho muscular e fortaleceu as junções microscópicas que impulsionam o movimento, tudo isso enquanto atenuava a inflamação prejudicial. Embora muito ainda precise ser testado, especialmente quanto à segurança a longo prazo e a melhor forma de combiná‑lo com terapias de AME existentes, esta pesquisa sugere que o haloperidol poderia eventualmente se tornar um tratamento prático de complemento ou alternativa que torne os ganhos atuais em força e independência mais duradouros.
Citação: Menduti, G., Perez-Gomez, R., Berenger-Currias, N. et al. Haloperidol induces neuroprotection and enhances neuromuscular function in both murine and human models of spinal muscular atrophy. Exp Mol Med 58, 1216–1229 (2026). https://doi.org/10.1038/s12276-026-01689-0
Palavras-chave: atrofia muscular espinhal, reposicionamento de fármacos, haloperidol, neurônios motores, junção neuromuscular