Clear Sky Science · he
הלופרידול מעודד הגנה עצבית ומשפר תפקוד נוירומוסקולרי במודלים של שיתוק שרירי ספינלי בעכברים ובבני אדם
הפיכת תרופה פסיכיאטרית למגן עצבי
שיתוק שרירי ספינלי (SMA) הוא מחלה תורשתית שמחלישה שרירים ועלולה להיות קטלנית בילדות. טיפולים קיימים מסייעים למטופלים רבים אך קשים להענקה, יקרים מאוד ואינם משחזרים במלואם את בריאות השריר והעצב. המחקר הזה שואל שאלה פשוטה אך בעלת עוצמה: האם אפשר להשתמש מחדש בהלופרידול, אנטי־פסיכוטי בעל שימוש ארוך, במינונים נמוכים בהרבה כדי להגן על תאי העצב והשרירים הפגומים ב־SMA, ולהציע אופציה נגישה ומשלימה?
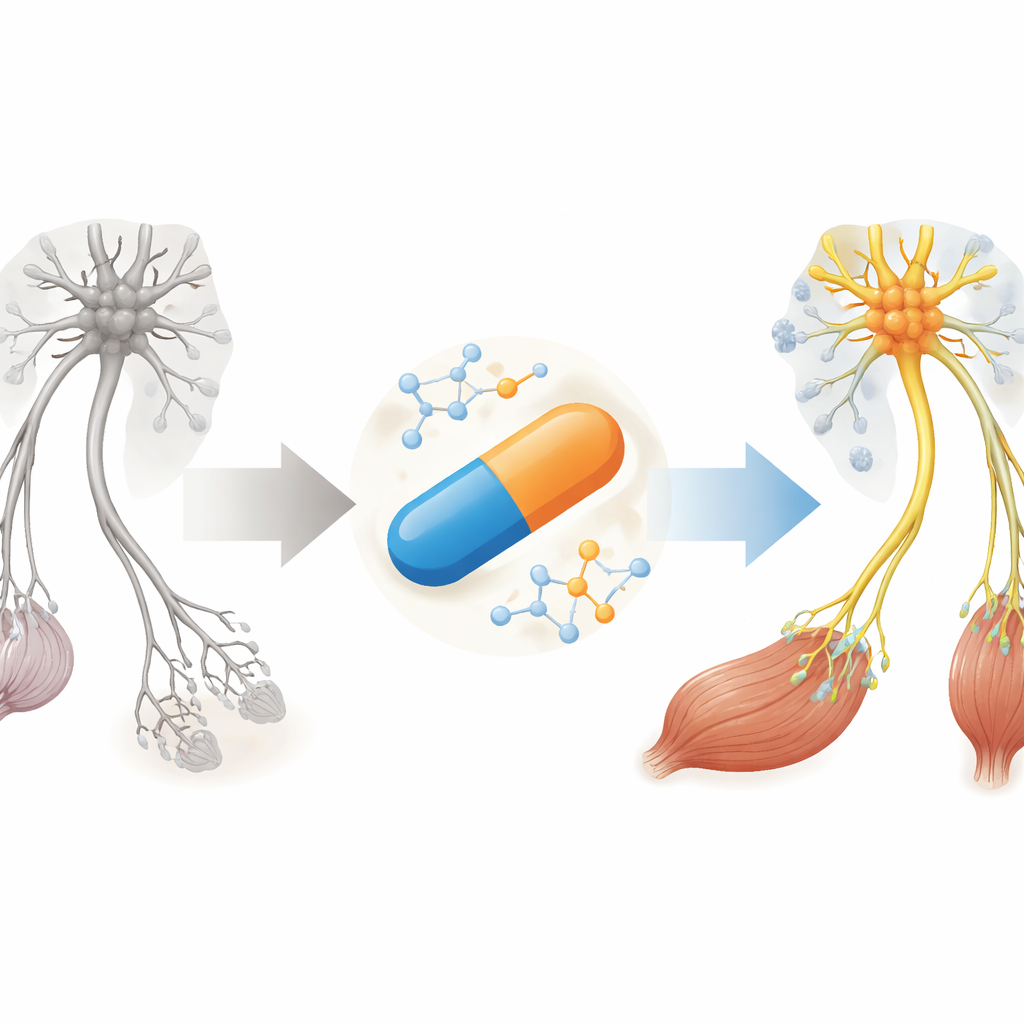
מדוע מחלת שחיקה שרירית זקוקה לאפשרויות חדשות
SMA נגרמת מחוסר בחלבון בשם SMN, שנוירוני תנועה — תאי העצב השולטים בתנועה — זקוקים לו כדי לשרוד. התרופות הקיימות מתמקדות כמעט באופן בלעדי בהעלאת רמות SMN במערכת העצבים, לעתים באמצעות הזרקות לעמוד השדרה או טיפולי גֵן יקרים. ובכל זאת, מטופלים רבים ממשיכים להראות ליקויים במוצא הנוירומסקולרי — נקודות המגע הזעירות שבהן העצבים מתקשרים עם השרירים — גם לאחר חודשים של טיפול. החוקרים טוענים שטיפולים עתידיים צריכים לא רק להעלות את רמות ה‑SMN באופן רחב יותר בגוף אלא גם להרגיע דלקת מזיקה ולתמוך ישירות בבריאות השריר והמוצא.
בדיקת הלופרידול בעכברים ובתאים אנושיים
הצוות סרק בעבר תרופות מאושרות בזבובים ופחותפות אנושיות ומצא שהלופרידול יכול לשפר איך הגן המשלים SMN2 מעובד, ובכך להעלות את חלבוני ה‑SMN. במחקר הנוכחי נתנו מינון נמוך של הלופרידול לזן עכברים עם SMA קשה החל מיד לאחר הלידה. העכברים שטופלו חיו זמן רב יותר, עלו במשקל והציגו שיווי משקל, יציבה וחוזק גפיים טובים יותר בהשוואה לאחיותיהם הלא מטופלות. במקביל, החוקרים גידלו נוירוני תנועה ותאי שריר ממטופלים ב‑SMA באמצעות שיטות תאי גזע. כשהתאים האנושיים נחשפו לכמויות זעירות של הלופרידול, יותר נוירוני תנועה שרדו, יצרו רשתות ענפיות עשירות יותר וגרמו לסיבי שריר גדולים ומחוברים טוב יותר בקו‑תרבית.
הגנה על עצבים, הרגעת תאי תמך וחיזוק שרירים
בחוט השדרה של העכברים, הלופרידול העלה את חלבון ה‑SMN בכמעט חצי וכמעט הכפיל את ה‑SMN בשרירי הרגל. נוירוני תנועה בבעלי החיים המטופלים היו רבים יותר והראו פחות סימנים מולקולריים של מוות תאי מתוכנת. סקרי ביטוי גנים חשפו שמאות מסרים הקשורים לעיבוד RNA, הישרדות תאים ומבנה הסינפסה זזו לכיוון דפוס בריא יותר, כולל רבים מהמטרות המוכרות כתלויות ב‑SMN. חשוב מכך, הלופרידול גם צמצם סמני אסטרוציטים עודפים ושינה את המיקרוגליה — תאי החיסון של המוח — לצורת מנוחה רגועה יותר. בשרירים, סיבי שריר בשריר ירך פגיע גדלו ויותר מוצאי נוירומוסקולריים היו מיושבים ומבוגרים כראוי, מה שמעיד על תקשורת חזקה ואמינה יותר בין עצבים לשרירים.
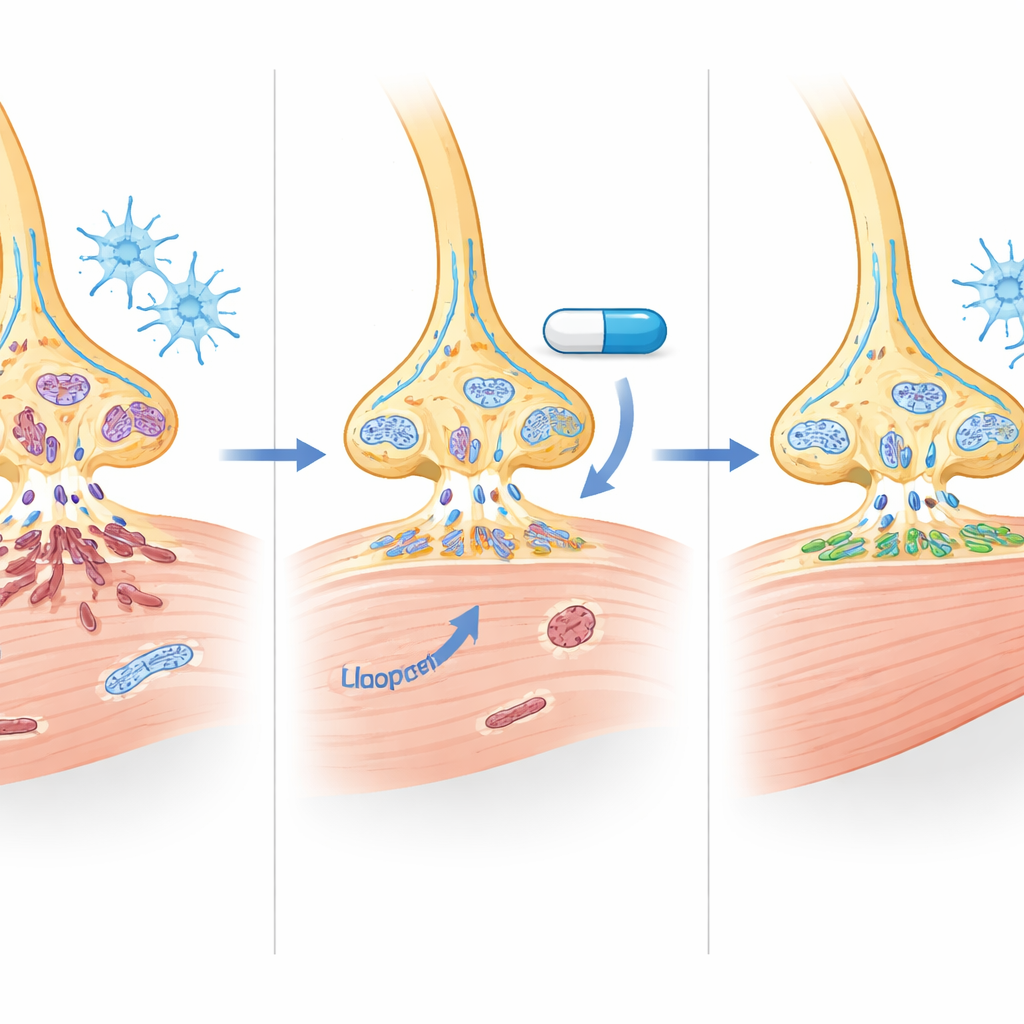
רמזים לאופן פעולת התרופה
הלופרידול ידוע בעיקר כחוסם קולטני דופמין D2 במינונים פסיכיאטריים, אך המינונים הנמוכים ששימשו כאן לא שינו בצורה מדידה את הקולטנים האלה במוח העכבר, בחוט השדרה או בנוירונים שמקורם בחולים. במקום זאת, הנתונים מצביעים על פעולה כפולה: עלייה צנועה אך משמעותית בחלבוני SMN יחד עם אפקטים כלליים יותר של "שימור בית" על עיבוד RNA, מסלולי מוות תאי, דלקת ותפקוד מיטוכונדריאלי. כמה גנים הקשורים לייצור אנרגיה ולעיבוד שומנים בשריר גם השתנו, מה רומז שהתרופה עשויה לתקן חלקית את ההפרעות המטבוליות הנצפות בשריר ה‑SMA, אף שבחינה מדויקת של השפעתה על המיטוכונדריה תדרוש מחקר עתידי.
מה זה עשוי להצביע עבור אנשים עם SMA
לקהל הרחב, המסר המרכזי הוא שתרופה ישנה וזולה — הלופרידול — עשויה, במינונים נמוכים הנבחרים בקפידה, לעזור לשמר את הקשר בין עצב לשריר ב‑SMA במקום להגביל את השפעתה רק על מצב הרוח או ההתנהגות. גם בעכברים וגם במודלים של תאים אנושיים היא האריכה את השרידות של נוירוני התנועה, שיפרה את גודל השריר וחיזקה את המוצאים המיקרוסקופיים שמפעילים תנועה, וכל זאת תוך דיכוי דלקת מזיקה. למרות שנדרש עוד בדיקות, ובפרט לגבי בטיחות לטווח הארוך ואיך לשלב אותה בצורה מיטבית עם טיפולים קיימים ל‑SMA, הממצא מציע שהלופרידול עשוי בסופו של דבר להפוך לתוספת מעשית או חלופה טיפולית שתעשה את ההישגים הנוכחיים בחוזק ובעצמאות לעמידים יותר.
ציטוט: Menduti, G., Perez-Gomez, R., Berenger-Currias, N. et al. Haloperidol induces neuroprotection and enhances neuromuscular function in both murine and human models of spinal muscular atrophy. Exp Mol Med 58, 1216–1229 (2026). https://doi.org/10.1038/s12276-026-01689-0
מילות מפתח: שיתוק שרירי ספינלי, איתור שימושים חדשים לתרופות, הלופרידול, נוירוני תנועה, מוצא נוירומסקולרי