Clear Sky Science · zh
利用 CRISPR–Cas9 对人类多能干细胞进行工程化以治疗帕金森病
这项研究为何与日常生活相关
帕金森病剥夺了人们流畅的动作、言语和独立生活能力,而现有药物通常只能暂时缓解症状。本文探讨科学家如何将两种强大工具——人类干细胞与被称为 CRISPR 的DNA切割蛋白——结合起来,更好地理解帕金森病中关键脑细胞为何死亡,并设计更安全、持久的细胞疗法,未来可能真正恢复丧失的功能,而不仅仅掩盖疾病。
理解一种常见的大脑疾病
帕金森病影响全球数百万人,且随年龄增长发病率升高。该疾病的核心是位于中脑小区域的多巴胺生成神经细胞的缓慢丧失,以及细胞内一种名为α-突触核蛋白的黏性蛋白团块。像左旋多巴这样的常规治疗可以暂时替代缺失的多巴胺,但无法阻止这些细胞继续死亡。动物模型提供了线索,但往往无法完整再现疾病在人类中缓慢进展的特征,这在实验室发现与对患者有效的治疗之间留下了巨大鸿沟。
在培养皿中培育人体神经细胞
人类多能干细胞能分化为几乎任何细胞类型,现在使研究者能够在实验室中大量培养产生多巴胺的神经元。这些体外培养的细胞重现了帕金森病的许多标志性特征,包括细胞能量工厂的功能障碍、废物处理系统受损以及α-突触核蛋白的积聚。由于这些细胞可以源自个体本人的组织,它们也携带该个体的精确遗传信息,使科学家能够在人体背景下模拟遗传性和更常见的散发性疾病形式,并直接在易损细胞类型上测试候选药物。
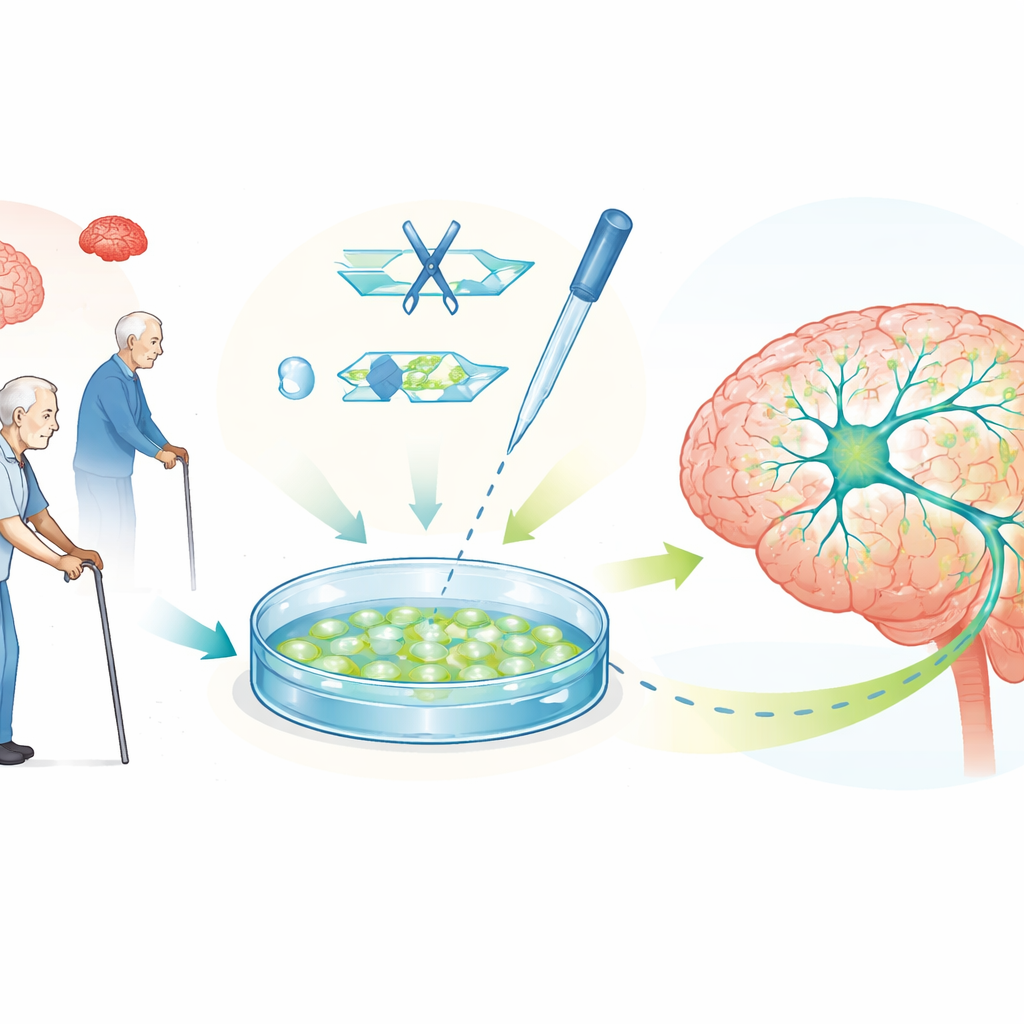
编辑基因以探究病因并检验假设
CRISPR–Cas9 这一精确的基因编辑工具,使这些干细胞模型更强大。通过改变单个 DNA 碱基、删除基因或纠正突变,研究者可以创建成对的细胞系,二者除一个帕金森风险因子外完全相同。对比它们可以揭示特定基因如何影响多巴胺神经元的健康、能量平衡和蛋白质积聚。综述列举了许多此类例子,包括对控制线粒体、蛋白质回收和神经元通讯的基因的编辑。文章还涵盖了无需切割 DNA 即能打开或关闭基因的“开关型”CRISPR 版本,以及可调节 DNA 包装状态的设计系统,这些工具有助于将 α-突触核蛋白的水平调整到较安全的范围。
智能标签、应激测试与大规模筛查
除了简单的基因切割外,CRISPR 还允许研究者在关键基因中插入发光标签或小型发光片段。这些标签使他们能够观察多巴胺神经元的发育、追踪 α-突触核蛋白的团块,并在药物测试中以高灵敏度测量蛋白水平。其他工程化工具使用光来触发快速的 α-突触核蛋白聚集,使有毒事件在数天内展开而非数年,从而加速发现。文章还强调了全基因组 CRISPR 筛查,能并行敲除数千个基因,以寻找 α-突触核蛋白及线粒体清道夫途径的隐性调控因子,指向原本难以事先猜测的新药物靶点。
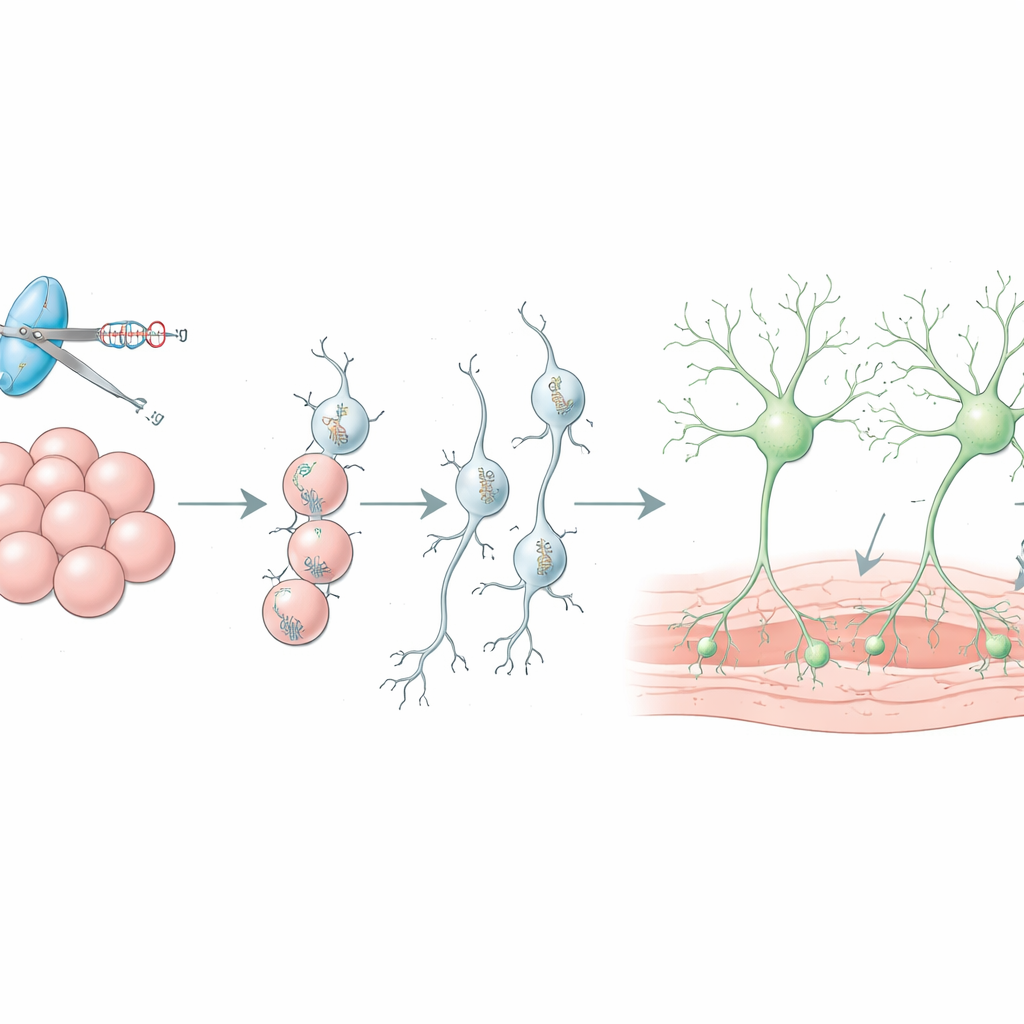
为大脑构建更好的移植组织
源自干细胞的多巴胺神经元已进入人体试验,作为替代帕金森病中丧失细胞的一种方式,但移植后常有超过九成的细胞在手术后不久死亡,而且不想要的细胞类型也可能混入移植体中。综述解释了如何在活体动物中利用 CRISPR 寻找控制移植体存活的基因,进而发展出诸如用现有药物阻断特定免疫信号以保护新生神经元的策略。它还描述了报告标签如何帮助在植入前分选出更纯净的多巴胺神经元批次,以及如何用 CRISPR 插入的化学遗传学开关,让医生通过无害的特效药远程调节移植体的活动。
展望未来疗法
综观本文所述工作,将人类干细胞与精确基因编辑相结合,正在改变科学家研究并有望治疗帕金森病的方式。这些工具创建了更接近患者所见的缓慢、与年龄相关损伤的人源模型,并有助于设计更安全、更强健且更能抵御有毒蛋白扩散的移植细胞。尽管在这些方法成为常规治疗之前,仍需解决许多科学、安全和伦理问题,但这张路线图指向了一个未来——疗法不仅仅缓解帕金森病的症状,而是保护或重建那些脆弱的脑回路本身。
引用: Park, S.B., Kim, JS., Ha, Y. et al. Human pluripotent stem cell engineering with CRISPR–Cas9 for Parkinson’s disease. Exp Mol Med 58, 993–1009 (2026). https://doi.org/10.1038/s12276-026-01679-2
关键词: 帕金森病, 人类干细胞, CRISPR 基因编辑, 多巴胺神经元, 细胞疗法