Clear Sky Science · fr
Ingénierie de cellules souches pluripotentes humaines avec CRISPR–Cas9 pour la maladie de Parkinson
Pourquoi cette recherche compte pour la vie quotidienne
La maladie de Parkinson prive les personnes de mouvements fluides, de la parole et de leur autonomie, et les médicaments actuels n’atténuent les symptômes que temporairement. Cet article explore comment les scientifiques combinent deux outils puissants, les cellules souches humaines et les protéines découpeuses d’ADN connues sous le nom de CRISPR, pour mieux comprendre pourquoi des cellules cérébrales clés meurent dans la maladie de Parkinson et pour concevoir des thérapies cellulaires plus sûres et plus durables qui pourraient un jour restaurer des fonctions perdues plutôt que de simplement masquer la maladie.
Comprendre un trouble cérébral courant
La maladie de Parkinson touche des millions de personnes dans le monde et devient plus fréquente avec l’âge. La pathologie repose sur la perte lente de neurones producteurs de dopamine dans une petite région du mésencéphale et sur l’accumulation de morceaux d’une protéine collante appelée alpha-synucléine à l’intérieur des cellules. Les traitements standard comme la lévodopa peuvent remplacer temporairement la dopamine manquante, mais ils n’empêchent pas la mort de ces cellules. Les modèles animaux ont permis de découvrir des indices, mais ils reproduisent souvent mal l’évolution lente et spécifique à l’humain de la maladie, laissant d’importants écarts entre les découvertes en laboratoire et des traitements utiles pour les patients.
Cultiver des neurones humains en laboratoire
Les cellules souches pluripotentes humaines, capables de se différencier en presque n’importe quel type cellulaire, permettent désormais aux chercheurs de cultiver en grand nombre des neurones humains producteurs de dopamine en laboratoire. Ces cellules cultivées reproduisent de nombreux signes caractéristiques de la maladie de Parkinson, notamment des dysfonctionnements des usines énergétiques cellulaires, des anomalies du système d’élimination des déchets et l’accumulation d’alpha-synucléine. Parce qu’elles peuvent être dérivées des tissus d’une personne, ces cellules portent aussi le bagage génétique exact de cette personne, permettant aux scientifiques de modéliser à la fois les formes héréditaires et les formes sporadiques plus communes de la maladie dans un contexte humain et de tester des médicaments candidats directement sur les types cellulaires vulnérables.
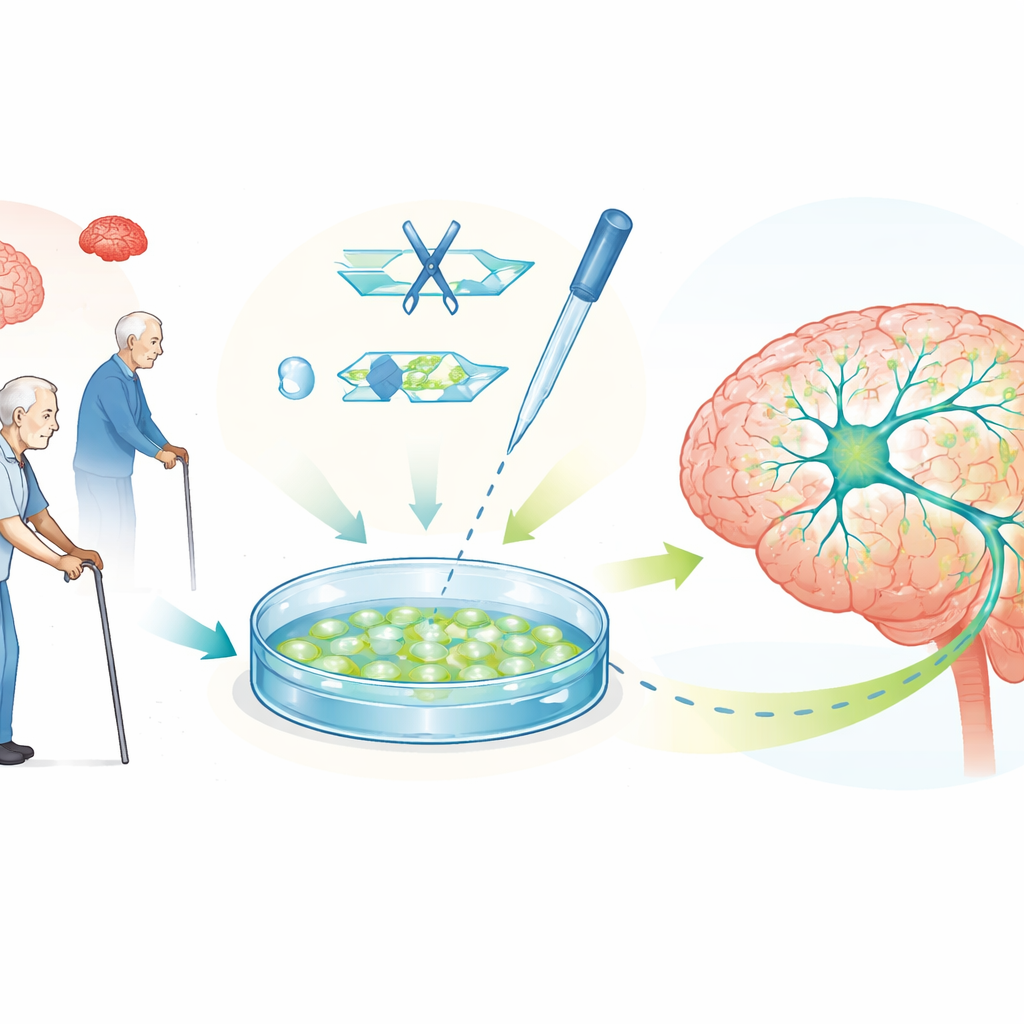
Éditer les gènes pour sonder les causes et tester des hypothèses
CRISPR–Cas9, un outil d’édition génétique précis, rend ces modèles de cellules souches bien plus puissants. En changeant une seule lettre d’ADN, en supprimant des gènes ou en corrigeant des mutations, les chercheurs peuvent créer des paires de lignées cellulaires identiques sauf pour un facteur de risque lié à la maladie de Parkinson. Les comparer révèle précisément comment tel ou tel gène affecte la santé des neurones dopaminergiques, l’équilibre énergétique et l’accumulation de protéines. La revue décrit de nombreux exemples de ce type, incluant des modifications de gènes qui contrôlent les mitochondries, le recyclage des protéines et la communication neuronale. Elle couvre aussi des versions « interrupteur » de CRISPR qui augmentent ou diminuent l’expression génétique sans couper l’ADN, ainsi que des systèmes conçus pour modifier la façon dont l’ADN est emballé, qui aident tous à réduire les niveaux d’alpha-synucléine à des plages plus sûres.
Étiquettes intelligentes, tests de stress et recherches à grande échelle
Au-delà des simples coupures de gènes, CRISPR permet d’insérer des marqueurs fluorescents ou de petits modules producteurs de lumière dans des gènes clés. Ces étiquettes permettent d’observer le développement des neurones dopaminergiques, de suivre les agrégats d’alpha-synucléine et de mesurer les niveaux de protéines avec une grande sensibilité lors d’essais pharmacologiques. D’autres outils ingénieux utilisent la lumière pour déclencher rapidement l’agrégation d’alpha-synucléine afin que des événements toxiques se produisent en quelques jours plutôt qu’en plusieurs années, accélérant ainsi la découverte. L’article met également en avant des criblages CRISPR à l’échelle du génome qui inactivent des milliers de gènes en parallèle pour identifier des régulateurs cachés de l’alpha-synucléine et de la voie de nettoyage mitochondriale, pointant vers de nouvelles cibles médicamenteuses difficiles à deviner a priori.
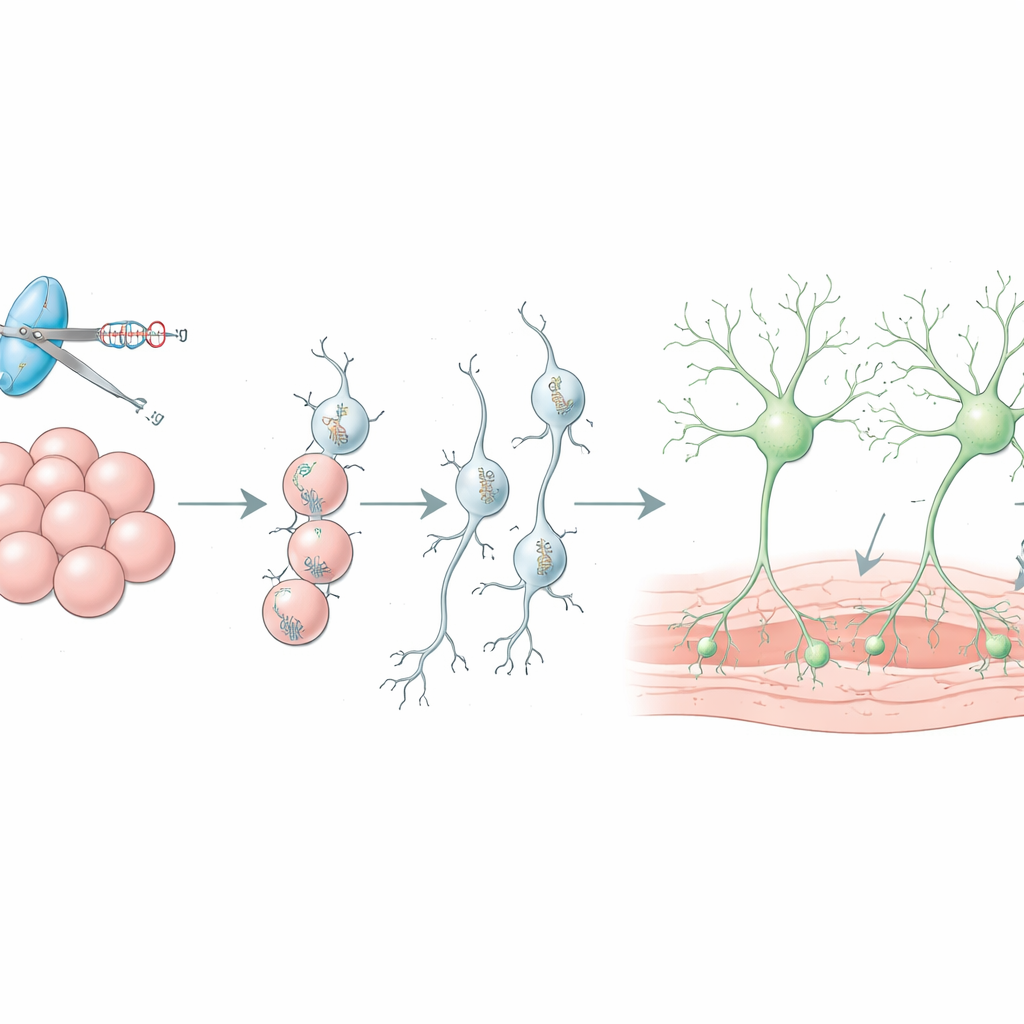
Construire de meilleurs greffons cellulaires pour le cerveau
Des neurones dopaminergiques dérivés de cellules souches sont déjà testés chez l’homme comme moyen de remplacer les cellules perdues dans la maladie de Parkinson, mais plus de quatre-vingt-dix pour cent des cellules transplantées meurent souvent peu après la chirurgie, et des types cellulaires indésirables peuvent s’insérer dans le greffon. La revue explique comment CRISPR est utilisé chez l’animal vivant pour rechercher des gènes qui contrôlent la survie des greffons, conduisant à des stratégies telles que le blocage de signaux immunitaires spécifiques avec des médicaments existants pour protéger les nouveaux neurones. Elle décrit aussi comment des marqueurs rapporteurs aident à trier des lots plus purs de neurones dopaminergiques avant l’implantation et comment des interrupteurs chimio‑génétiques, insérés par CRISPR, permettent aux médecins d’ajuster à distance l’activité du greffon à l’aide de médicaments conçus inoffensifs.
Perspectives pour des traitements futurs
Pris dans leur ensemble, les travaux résumés dans cet article montrent que la combinaison de cellules souches humaines et d’une édition génomique précise transforme la façon dont les scientifiques étudient et potentiellement traitent la maladie de Parkinson. Ces outils créent des modèles humains qui reflètent plus fidèlement les dommages lents liés à l’âge observés chez les patients et aident à concevoir des cellules transplantées plus sûres, plus résistantes et moins susceptibles d’être affectées par la propagation de protéines toxiques. Bien que de nombreuses questions scientifiques, de sécurité et d’éthique restent à résoudre avant que ces approches puissent devenir des soins standards, cette feuille de route laisse entrevoir un avenir où les thérapies viseraient non seulement à atténuer les symptômes de la maladie de Parkinson, mais aussi à protéger ou reconstruire les circuits cérébraux vulnérables eux‑mêmes.
Citation: Park, S.B., Kim, JS., Ha, Y. et al. Human pluripotent stem cell engineering with CRISPR–Cas9 for Parkinson’s disease. Exp Mol Med 58, 993–1009 (2026). https://doi.org/10.1038/s12276-026-01679-2
Mots-clés: maladie de Parkinson, cellules souches humaines, édition génomique CRISPR, neurones dopaminergiques, thérapie cellulaire