Clear Sky Science · de
Ingenieurwesen humaner pluripotenter Stammzellen mit CRISPR–Cas9 für die Parkinson‑Krankheit
Warum diese Forschung für den Alltag wichtig ist
Die Parkinson‑Krankheit raubt Menschen flüssige Bewegungen, Sprachfähigkeit und Selbstständigkeit, und die heutigen Medikamente lindern die Symptome oft nur vorübergehend. Dieser Artikel beschreibt, wie Forscher zwei mächtige Werkzeuge — humane Stammzellen und DNA‑schneidende Proteine namens CRISPR — kombinieren, um besser zu verstehen, warum zentrale Gehirnzellen bei Parkinson absterben, und um sicherere, langlebigere Zelltherapien zu entwickeln, die eines Tages verlorene Funktionen wiederherstellen könnten, statt die Krankheit nur zu überdecken.
Ein häufiges Gehirnleiden verstehen
Die Parkinson‑Krankheit betrifft weltweit Millionen Menschen und nimmt mit dem Alter zu. Im Mittelpunkt steht der schrittweise Verlust von Dopamin produzierenden Nervenzellen in einer kleinen Region der Mittelhirns sowie Ansammlungen eines klebrigen Proteins namens Alpha‑Synuclein in Zellen. Standardbehandlungen wie Levodopa können fehlendes Dopamin zeitweise ersetzen, stoppen jedoch nicht das Absterben dieser Zellen. Tiermodelle haben Hinweise geliefert, erfassen aber oft nicht den langsamen, menschenspezifischen Verlauf der Erkrankung, sodass große Lücken zwischen Laborbefunden und wirksamen Behandlungen für Patienten bleiben.
Wachsende menschliche Nervenzellen im Reagenzglas
Humane pluripotente Stammzellen, die sich in nahezu jeden Zelltyp verwandeln können, erlauben es Forschern heute, große Mengen menschlicher Dopamin‑neurone im Labor zu züchten. Diese im Labor erzeugten Zellen zeigen viele Kennzeichen von Parkinson, darunter Störungen der Energieerzeugung, der Abfallentsorgung und die Ansammlung von Alpha‑Synuclein. Da sie aus dem Gewebe einer Person gewonnen werden können, tragen die Zellen auch das exakte genetische Profil dieser Person, sodass Forscher sowohl erbliche als auch häufigere sporadische Formen der Krankheit in einem menschlichen Kontext nachbilden und Wirkstoffkandidaten direkt an gefährdeten Zelltypen testen können.
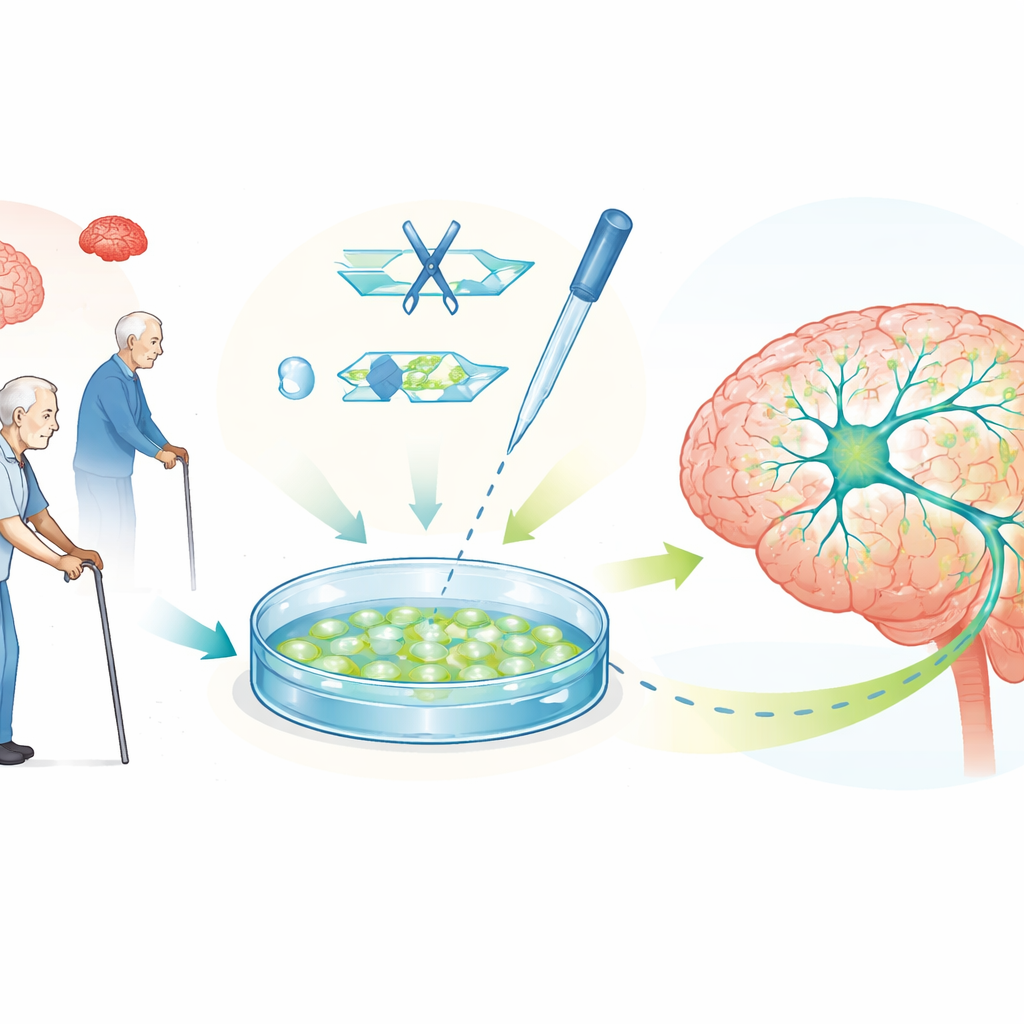
Gene editieren, um Ursachen zu erforschen und Hypothesen zu prüfen
CRISPR–Cas9, ein präzises Geneditierungswerkzeug, macht diese Stammzellmodelle deutlich aussagekräftiger. Durch das Ändern einzelner DNA‑Buchstaben, das Löschen von Genen oder das Korrigieren von Mutationen können Wissenschaftler Zelllinienpaare erzeugen, die bis auf einen Parkinson‑Risikofaktor identisch sind. Ihr Vergleich zeigt genau, wie bestimmte Gene die Gesundheit von Dopaminneuronen, das Energiegleichgewicht und die Proteinansammlung beeinflussen. Der Übersichtsartikel beschreibt viele solcher Beispiele, darunter Veränderungen in Genen, die Mitochondrien, Proteinrecycling und neuronale Kommunikation steuern. Er behandelt auch „schalterartige“ CRISPR‑Versionen, die Gene hoch- oder herunterregulieren, ohne DNA zu schneiden, sowie Designer‑Systeme, die die Verpackung von DNA modifizieren — alles Instrumente, mit denen sich Alpha‑Synuclein‑Spiegel auf sicherere Werte einstellen lassen.
Intelligente Marker, Stresstests und großangelegte Suchen
Über einfache Genschnitte hinaus erlaubt CRISPR das Einfügen leuchtender Marker oder kleiner lichtproduzierender Elemente in Schlüsselfunktionen. Diese Marker ermöglichen es, die Entwicklung von Dopaminneuronen zu beobachten, Alpha‑Synuclein‑Ablagerungen zu verfolgen und Proteinmengen mit hoher Empfindlichkeit während Wirkstofftests zu messen. Andere gezielte Werkzeuge nutzen Licht, um rapid Alpha‑Synuclein‑Aggregation auszulösen, sodass toxische Ereignisse innerhalb von Tagen statt Jahren ablaufen und die Entdeckung beschleunigt wird. Der Artikel hebt zudem genomweite CRISPR‑Screens hervor, die Tausende Gene parallel ausschalten, um verborgene Regulatoren von Alpha‑Synuclein und des mitochondrialen Reinigungswegs zu finden — Hinweise auf neue Arzneizielstrukturen, die vorher schwer zu vermuten gewesen wären.
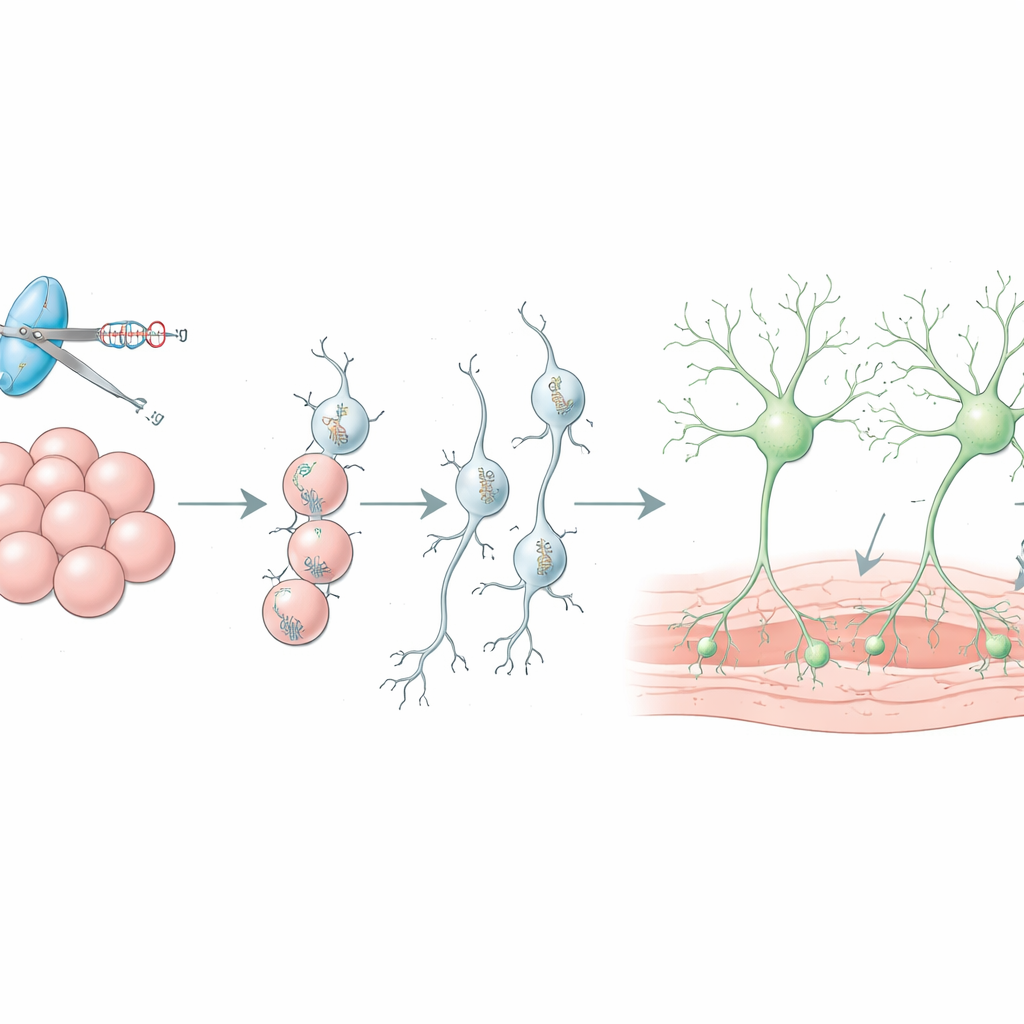
Bessere Zelltransplantate fürs Gehirn bauen
Dopaminneurone aus Stammzellen werden bereits beim Menschen getestet, um verlorene Zellen bei Parkinson zu ersetzen, doch oft sterben mehr als neunzig Prozent der transplantierten Zellen kurz nach der Operation, und unerwünschte Zelltypen können sich in das Transplantat einschleichen. Die Übersichtsarbeit erläutert, wie CRISPR in lebenden Tieren verwendet wird, um Gene zu finden, die das Überleben des Transplantats steuern, und beschreibt Strategien wie das Blockieren bestimmter Immun‑Signale mit bereits verfügbaren Medikamenten zum Schutz neuer Neurone. Sie zeigt auch, wie Reporter‑Marker helfen, vor der Implantation reinere Chargen von Dopaminneuronen zu sortieren, und wie mit CRISPR eingesetzte chemogenetische Schalter Ärzten ermöglichen, die Aktivität des Transplantats aus der Ferne mit harmlosen Wirkstoffen hoch- oder herunterzuregulieren.
Blick auf zukünftige Behandlungen
In der Summe zeigt die zusammengefasste Arbeit, dass die Kombination menschlicher Stammzellen mit präziser Geneditierung die Art und Weise verändert, wie Wissenschaftler Parkinson erforschen und potenziell behandeln. Diese Werkzeuge schaffen menschenbasierte Modelle, die den langsamen, altersbedingten Schaden bei Patienten besser nachbilden, und helfen dabei, transplantierte Zellen zu entwerfen, die sicherer, robuster und widerstandsfähiger gegen die Ausbreitung toxischer Proteine sind. Obwohl viele wissenschaftliche, sicherheitsrelevante und ethische Fragen geklärt werden müssen, bevor solche Ansätze zur Standardtherapie werden können, skizziert diese Roadmap eine Zukunft, in der Therapien nicht nur Symptome lindern, sondern verletzliche Hirnnetzwerke schützen oder wiederaufbauen sollen.
Zitation: Park, S.B., Kim, JS., Ha, Y. et al. Human pluripotent stem cell engineering with CRISPR–Cas9 for Parkinson’s disease. Exp Mol Med 58, 993–1009 (2026). https://doi.org/10.1038/s12276-026-01679-2
Schlüsselwörter: Parkinson‑Krankheit, humane Stammzellen, CRISPR‑Geneditierung, Dopaminneurone, Zelltherapie