Clear Sky Science · ru
Генная инженерия человеко́вых плюрипотентных стволовых клеток с помощью CRISPR–Cas9 при болезни Паркинсона
Почему это исследование важно для повседневной жизни
Болезнь Паркинсона лишает людей плавности движений, речи и независимости, а существующие лекарства лишь временно облегчают симптомы. В этой статье рассматривается, как учёные объединяют два мощных инструмента — человеческие стволовые клетки и белки, разрезающие ДНК, известные как CRISPR — чтобы лучше понять, почему ключевые клетки мозга погибают при Паркинсоне, и разработать более безопасные, долговечные клеточные терапии, которые однажды могли бы восстановить утраченные функции, а не просто маскировать болезнь.
Понимание распространённого расстройства мозга
Болезнь Паркинсона поражает миллионы людей во всём мире и становится более частой с возрастом. Заболевание связано с постепенной потерей дофамин-продуцирующих нервных клеток в небольшой области среднего мозга и с образованием скоплений липкой белковой структуры — альфа-синуклеина — внутри клеток. Стандартные лечения, такие как леводопа, временно восполняют дефицит дофамина, но не останавливают гибель этих клеток. Модели на животных помогли раскрыть ряд подсказок, однако часто не отражают медленного, специфичного для человека течения болезни, что оставляет значительный разрыв между лабораторными открытиями и эффективными методами лечения пациентов.
Выращивание человеческих нервных клеток в чашке Петри
Человеческие плюрипотентные стволовые клетки, способные превращаться почти в любой тип клетки, позволяют исследователям выращивать в лаборатории большое количество человеческих допаминовых нейронов. Эти клетки, выращенные в лаборатории, воспроизводят многие характерные черты Паркинсона, включая нарушения работы энергетических станций клетки, системы утилизации отходов и накопление альфа-синуклеина. Поскольку их можно получить из тканей конкретного человека, такие клетки несут его точный генетический набор, что даёт возможность моделировать как наследственные, так и более распространённые спорадические формы болезни в человеческой системе и тестировать кандидаты на лекарства прямо на уязвимых типах клеток.
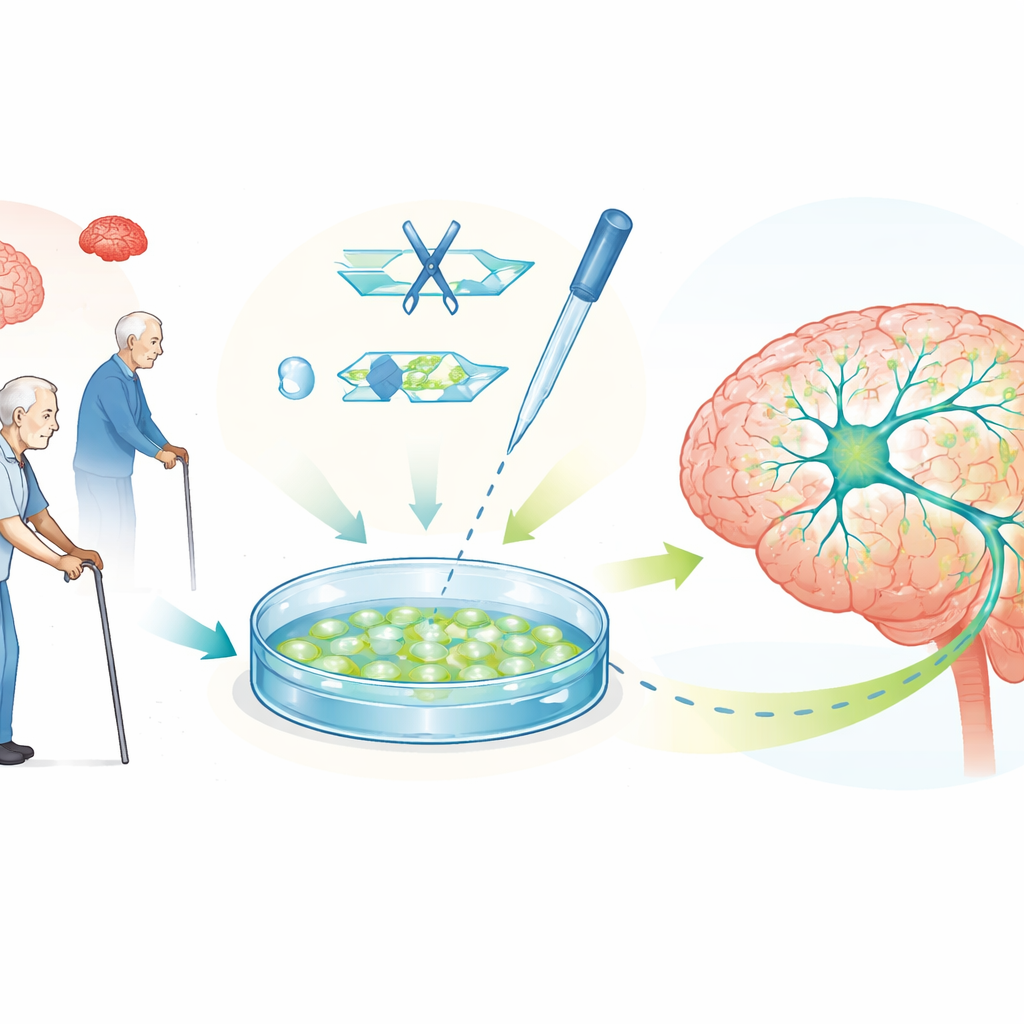
Редактирование генов для исследования причин и проверки гипотез
CRISPR–Cas9, точный инструмент генетического редактирования, делает эти модели стволовых клеток значительно мощнее. Изменяя одиночные буквы ДНК, удаляя гены или исправляя мутации, учёные могут создавать пары линий клеток, идентичных во всём, кроме одного фактора риска Паркинсона. Сравнение таких линий показывает, как конкретные гены влияют на здоровье допаминовых нейронов, энергетический баланс и накопление белков. В обзоре приводятся многие такие примеры, включая правки генов, которые контролируют митохондрии, утилизацию белков и передачу сигналов между нейронами. Также описаны «переключаемые» версии CRISPR, которые усиливают или подавляют активность генов без разрезания ДНК, и дизайнерские системы, меняющие упаковку ДНК — всё это помогает привести уровни альфа-синуклеина к более безопасным значениям.
Умные метки, стресс-тесты и крупномасштабные поиски
Помимо простых разрезов генома, CRISPR позволяет вставлять светящиеся метки или крошечные светопроизводящие фрагменты в ключевые гены. Эти метки дают возможность наблюдать за развитием допаминовых нейронов, отслеживать скопления альфа-синуклеина и измерять уровни белков с высокой чувствительностью в ходе тестирования лекарств. Другие инженерные инструменты используют свет для быстрого инициирования слипания альфа-синуклеина, так что токсические события разворачиваются за дни, а не годы, что ускоряет открытие. В статье также подчёркнуты геномные скрины CRISPR, которые параллельно выводят из строя тысячи генов, чтобы найти скрытые регуляторы альфа-синуклеина и митохондриальных путей очистки, указывая на новые цели для лекарств, которые было бы трудно предсказать заранее.
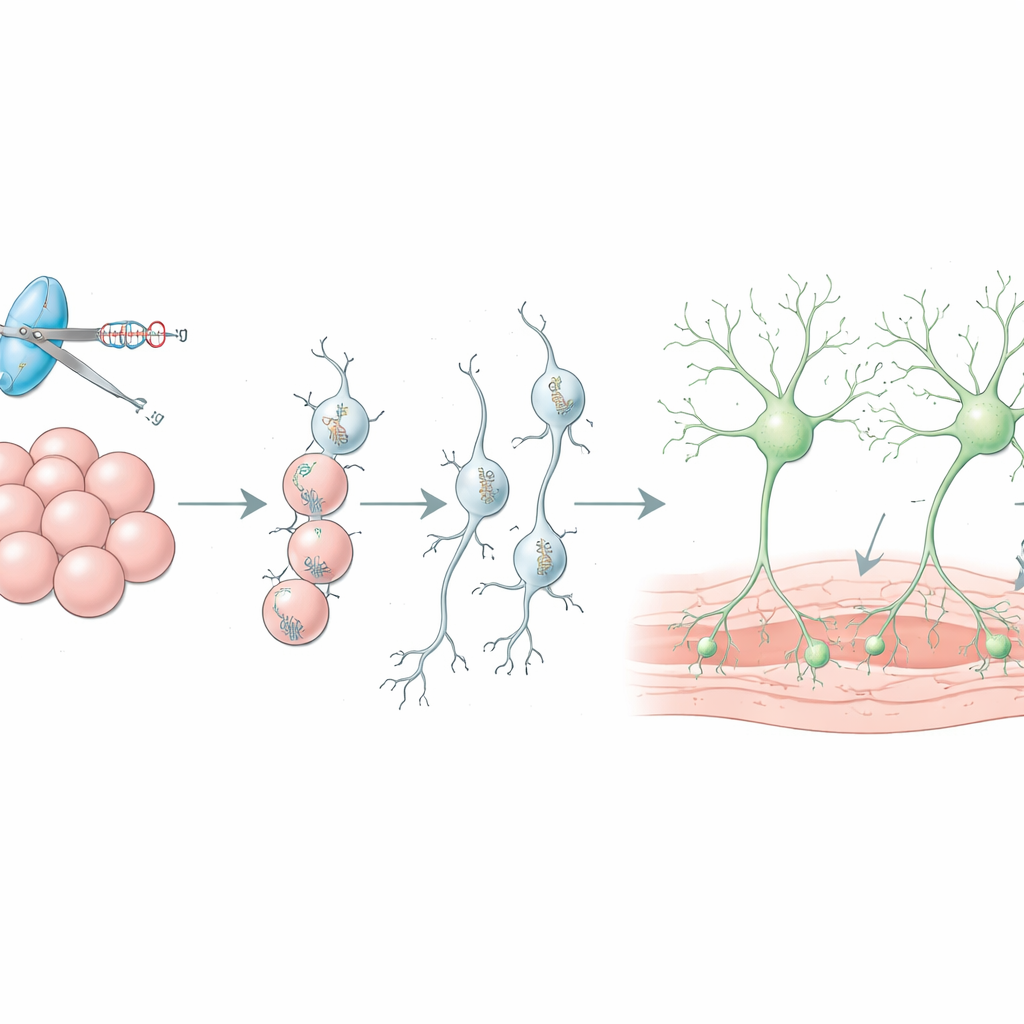
Создание лучших трансплантатов для мозга
Допаминовые нейроны, полученные из стволовых клеток, уже испытываются у людей как способ замещения утраченных клеток при болезни Паркинсона, но более девяноста процентов трансплантированных клеток часто погибают вскоре после операции, а нежелательные типы клеток могут проникать в трансплантат. В обзоре объясняется, как CRISPR используется в живых животных для поиска генов, контролирующих выживание трансплантата, что привело к стратегиям, таким как блокирование определённых иммунных сигналов с помощью уже существующих лекарств для защиты новых нейронов. Также описано, как репортерные метки помогают сортировать более чистые партии допаминовых нейронов перед имплантацией и как химогенетические переключатели, внедрённые с помощью CRISPR, позволяют врачам дистанционно регулировать активность трансплантата с помощью безопасных дизайнерских препаратов.
Взгляд в будущее лечения
В совокупности работа, суммированная в этой статье, показывает, что сочетание человеческих стволовых клеток и точного генетического редактирования меняет подход к изучению и потенциальному лечению болезни Паркинсона. Эти инструменты создают модели на основе человека, которые ближе отражают медленное, связанное с возрастом повреждение, наблюдаемое у пациентов, и помогают проектировать трансплантированные клетки, которые более безопасны, выносливы и устойчивы к распространению токсичных белков. Хотя перед внедрением таких подходов в рутинную клиническую практику остаётся много научных, безопасностных и этических вопросов, эта дорожная карта указывает на будущее, в котором терапии стремятся не просто облегчить симптомы Паркинсона, но защитить или восстановить уязвимые мозговые цепи сами по себе.
Цитирование: Park, S.B., Kim, JS., Ha, Y. et al. Human pluripotent stem cell engineering with CRISPR–Cas9 for Parkinson’s disease. Exp Mol Med 58, 993–1009 (2026). https://doi.org/10.1038/s12276-026-01679-2
Ключевые слова: Болезнь Паркинсона, человеческие стволовые клетки, генетическое редактирование CRISPR, допаминовые нейроны, клеточная терапия