Clear Sky Science · ar
هندسة الخلايا الجذعية متعددة القدرات البشرية باستخدام CRISPR–Cas9 لمرض باركنسون
لماذا يهم هذا البحث في الحياة اليومية
يسلب مرض باركنسون الناس القدرة على الحركة السلسة والكلام والاستقلالية، والأدوية الحالية تخفف الأعراض لفترة فقط. تستعرض هذه المقالة كيف يجمع العلماء بين أداتين قويتين، الخلايا الجذعية البشرية والبروتينات القاطعة للحمض النووي المعروفة باسم CRISPR، لفهم أفضل لأسباب موت خلايا الدماغ الرئيسية في باركنسون وتصميم علاجات خلوية أكثر أمانًا وطويلة الأمد قد تستعيد الوظيفة المفقودة بدلًا من مجرد إخفاء المرض.
فهم اضطراب دماغي شائع
يصيب مرض باركنسون ملايين الأشخاص حول العالم ويزداد شيوعًا مع التقدم في العمر. يتمحور المرض حول الفقدان البطيء للخلايا العصبية المنتجة للدوبامين في منطقة صغيرة من الدماغ الأوسط وترسبات بروتين لزج تُسمى ألفا ساينوكلين داخل الخلايا. العلاجات القياسية مثل ليفودوبا يمكن أن تحل محل الدوبامين المفقود مؤقتًا، لكنها لا توقف موت هذه الخلايا. ساعدت نماذج حيوانية في الكشف عن أدلة، لكنها غالبًا ما تفشل في التقاط مجرى المرض البطيء والمميز للإنسان، مما يترك فجوات كبيرة بين الاكتشافات المخبرية والعلاجات المفيدة للمرضى.
زراعة خلايا عصبية بشرية في المختبر
تسمح الخلايا الجذعية متعددة القدرات البشرية، التي يمكن أن تتحول إلى أي نوع خلايا تقريبًا، للباحثين الآن بزراعة أعداد كبيرة من الخلايا العصبية البشرية المنتجة للدوبامين في المختبر. تحاكي هذه الخلايا المزروعة العديد من سمات باركنسون، بما في ذلك مشكلات مصانع الطاقة داخل الخلية، وأنظمة التخلص من النفايات، وتراكم ألفا ساينوكلين. وبما أنه يمكن صنعها من أنسجة شخص معين، فإن هذه الخلايا تحمل أيضًا التكوين الجيني ذاته لذلك الشخص، مما يتيح للعلماء نمذجة الأشكال الموروثة والشائعة العرضية للمرض في سياق بشري واختبار الأدوية المرشحة مباشرة على أنواع الخلايا المعرضة للخطر.
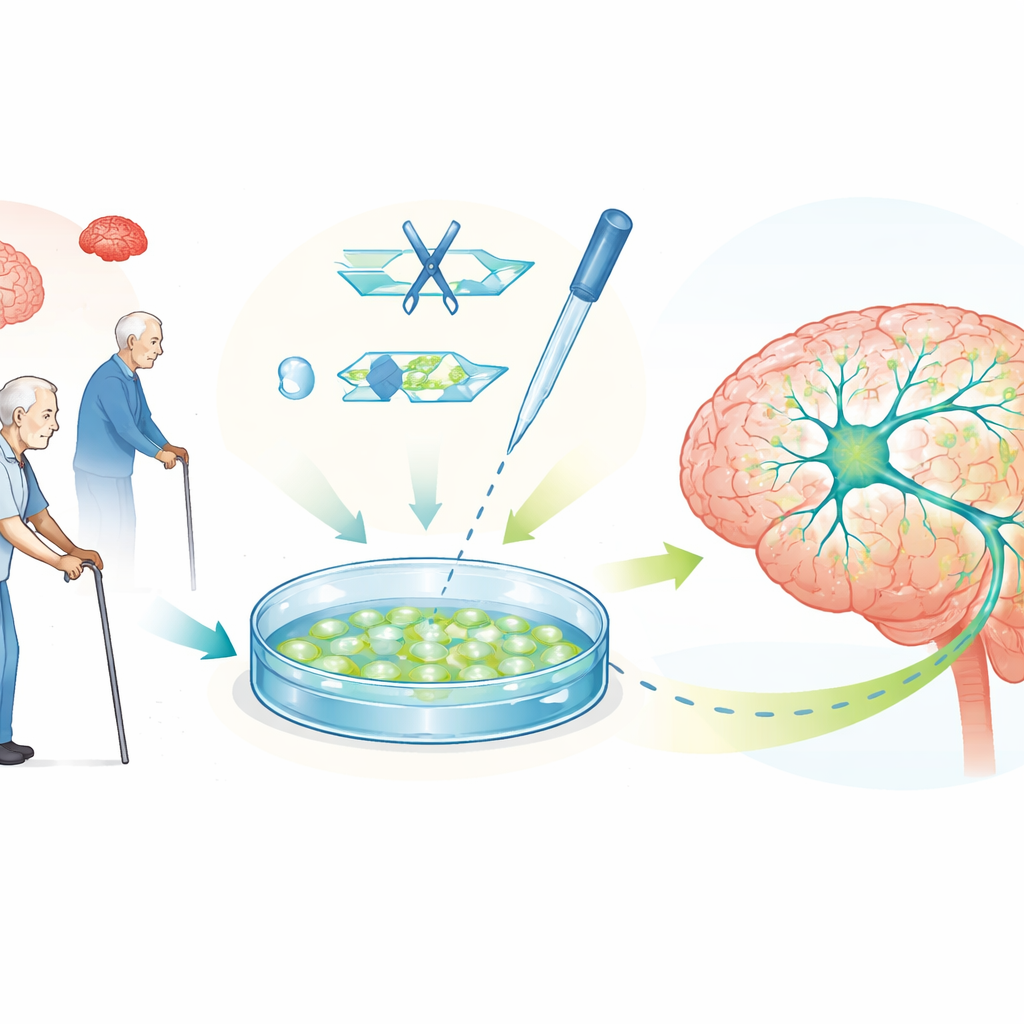
تعديل الجينات لاستكشاف الأسباب واختبار الأفكار
يجعل CRISPR–Cas9، أداة تحرير الجينات الدقيقة، هذه النماذج القائمة على الخلايا الجذعية أقوى بكثير. من خلال تغيير حرف واحد من الحمض النووي، حذف جينات، أو تصحيح طفرات، يمكن للعلماء إنشاء أزواج من خطوط الخلايا متطابقة باستثناء عامل خطر واحد لباركنسون. يكشف المقارنة بينهما بالضبط كيف تؤثر جينات معينة على صحة نيورونات الدوبامين، توازن الطاقة، وتراكم البروتينات. تشرح المراجعة العديد من أمثلة هذه التعديلات، بما في ذلك تغييرات في جينات تتحكم في الميتوكوندريا، تدوير البروتينات، والتواصل العصبي. كما تغطي نسخًا "شبيهة بالمفاتيح" من CRISPR التي ترفع أو تخفض نشاط الجينات دون قطع الحمض النووي، وأنظمة مُصمَمة تعدّل كيفية ترتيب الحمض النووي، وكلها تساعد في ضبط مستويات ألفا ساينوكلين ضمن نطاقات أكثر أمانًا.
وسوم ذكية، اختبارات إجهاد، وبحث على نطاق واسع
بعيدًا عن القصّات الجينية البسيطة، يتيح CRISPR للباحثين إدخال وسوم متوهجة أو قطع صغيرة تنتج الضوء داخل جينات رئيسية. تسمح هذه الوسوم بمراقبة تطور نيورونات الدوبامين، تتبع تجمعات ألفا ساينوكلين، وقياس مستويات البروتينات بحساسية عالية أثناء اختبار الأدوية. تستخدم أدوات مهندَسة أخرى الضوء لتحفيز تجمع ألفا ساينوكلين بسرعة بحيث تتكشف الأحداث السامة في أيام بدلًا من سنوات، مسرِّعة الاكتشاف. تبرز المقالة أيضًا شاشات CRISPR على مستوى الجينوم التي تُعطّل آلاف الجينات بالتوازي للعثور على منظمات خفية لألفا ساينوكلين ومسار تنظيف الميتوكوندريا، مشيرة إلى أهداف دوائية جديدة كان من الصعب توقعها مقدمًا.
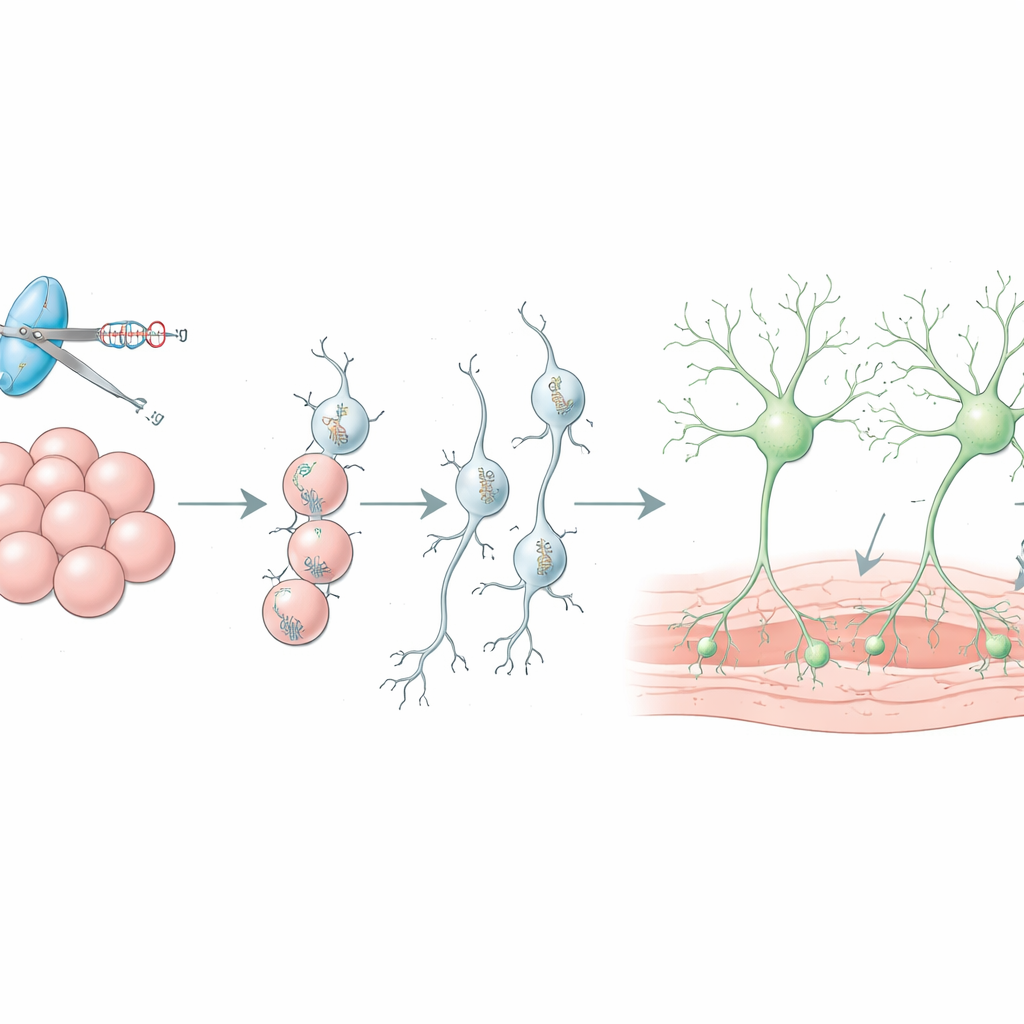
بناء طُعوم خلوية أفضل للدماغ
تُجرّب نيورونات الدوبامين المشتقة من الخلايا الجذعية بالفعل في البشر كوسيلة لاستبدال الخلايا المفقودة في مرض باركنسون، لكن أكثر من تسعين في المئة من الخلايا المزروعة غالبًا ما تموت بعد الجراحة بفترة وجيزة، وقد تزحف أنواع خلوية غير مرغوب فيها إلى الطُعم. تشرح المراجعة كيف يُستخدم CRISPR في الحيوانات الحية للبحث عن جينات تتحكم في بقاء الطعوم، مما يؤدي إلى استراتيجيات مثل حجب إشارات مناعية محددة بأدوية متاحة لحماية النيورونات الجديدة. كما تصف كيف تساعد وسوم المراصد في فرز دفعات أنقى من نيورونات الدوبامين قبل الزرع وكيف تسمح مفاتيح كيموجينية، المُدخلة بواسطة CRISPR، للأطباء بضبط نشاط الطعم عن بُعد لأعلى أو لأسفل باستخدام أدوية مصممة غير ضارة.
نظرة إلى العلاجات المستقبلية
بشكل إجمالي، يُظهر العمل الملخّص في هذه المقالة أن الجمع بين الخلايا الجذعية البشرية وتحرير الجينات الدقيق يعيد تشكيل طريقة دراسة وعلاج مرض باركنسون المحتمل. تخلق هذه الأدوات نماذج قائمة على الإنسان تُحاكي بشكل أوثق الضرر البطيء المرتبط بالعمر الذي يُرى لدى المرضى وتساعد في تصميم خلايا مزروعة أكثر أمانًا ومتانة ومقاومة لانتشار البروتينات السامة. وبينما تبقى الكثير من الأسئلة العلمية والسلامة والأخلاق قبل أن تصبح مثل هذه المناهج رعاية قياسية، يرسم هذا الدليل طريقًا نحو مستقبل تهدف فيه العلاجات ليس فقط لتخفيف أعراض باركنسون بل لحماية أو إعادة بناء الدوائر الدماغية الضعيفة نفسها.
الاستشهاد: Park, S.B., Kim, JS., Ha, Y. et al. Human pluripotent stem cell engineering with CRISPR–Cas9 for Parkinson’s disease. Exp Mol Med 58, 993–1009 (2026). https://doi.org/10.1038/s12276-026-01679-2
الكلمات المفتاحية: مرض باركنسون, الخلايا الجذعية البشرية, تحرير الجينات بواسطة CRISPR, نيورونات الدوبامين, علاج الخلايا