Clear Sky Science · he
מהנדסי תאי גזע פלוריפוטנטיים אנושיים עם CRISPR–Cas9 למחלת פרקינסון
מדוע המחקר הזה חשוב לחיי היום־יום
מחלת פרקינסון גוזלת מאנשים תנועות חלקות, דיבור ועצמאות, והתרופות הקיימות כיום מרחמות רק על הסימפטומים לזמן מוגבל. המאמר בוחן כיצד מדענים משלבים שני כלים רבי‑עוצמה — תאי גזע אנושיים וחלבונים החותכים DNA הידועים כ‑CRISPR — כדי להבין טוב יותר מדוע תאי מוח מרכזיים מתים בפרקינסון ולתכנן טיפולי תאים בטוחים ועמידים יותר שעשויים יום אחד להשיב תפקוד שאבד במקום רק להסתיר את המחלה.
הבנת הפרעה מוחית שכיחה
מחלת פרקינסון משפיעה על מיליונים ברחבי העולם והיא נפוצה יותר עם העלייה בגיל. המחלה מתמקדת באובדן הדרגתי של תאי עצב שמייצרים דופמין באזור קטן במידבריין ובצבירים של חלבון דביק בשם אלפא‑סינוקלאין בתוך התאים. טיפולים סטנדרטיים כמו לוודופה יכולים להחליף באופן זמני את הדופמין החסר, אך אינם עוצרים את מוות התאים הללו. מודלים בעלי חיים חשפו רמזים רבים, אך לעתים קרובות אינם מצליחים לשחזר את מהלך המחלה האיטי והמיוחד לבני אדם, מה שמשאיר פערים גדולים בין גילויים במעבדה לטיפולים שימושיים עבור מטופלים.
גידול תאי עצב אנושיים בצלחת
תאי גזע פלוריפוטנטיים אנושיים, היכולים להימרח כמעט לכל סוג תא, מאפשרים כיום לחוקרים לגדל כמויות גדולות של נוירונים אנושיים שמייצרים דופמין במעבדה. תאים שגדלו במעבדה מדמים סימנים רבים של פרקינסון, כולל תפקוד לקוי של תחנות האנרגיה בתא, בעיות במערכות הסילוק של פסולת ותצטברויות של אלפא‑סינוקלאין. מכיוון שניתן להכיןם מרקמות של אדם מסוים, תאים אלה נושאים גם את המטען הגנטי המדויק של אותו אדם, ומאפשרים למדענים לדמות הן צורות תורשתיות והן צורות ספונטניות הנפוצות יותר של המחלה בסביבה אנושית ולבחון תרופות מועמדות ישירות על סוגי תאים הפגיעים.
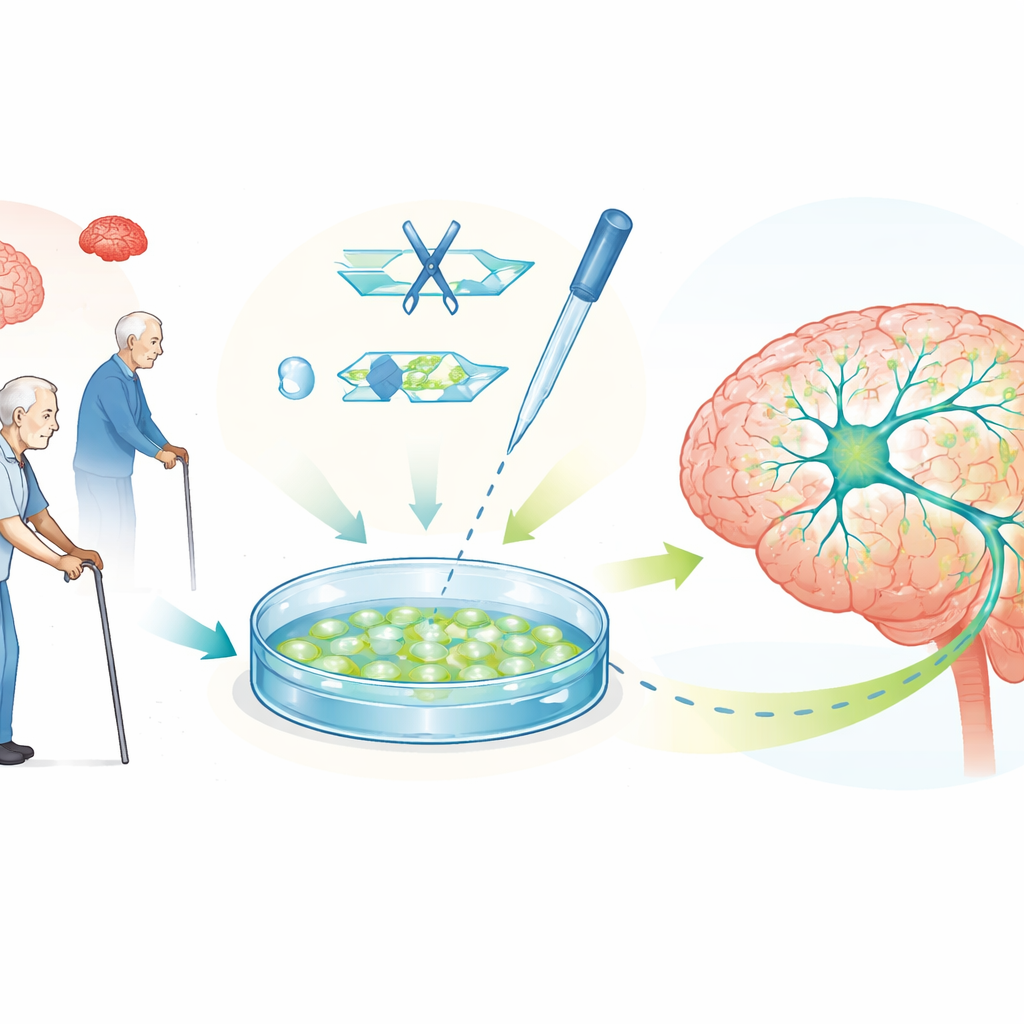
עריכה גנטית לחקירת סיבות ובחינת רעיונות
CRISPR–Cas9, כלי מדויק לעריכת גנים, מחזק משמעותית את המודלים הללו של תאי גזע. על‑ידי שינוי אותיות יחידות DNA, מחיקה של גנים או תיקון מוטציות, מדענים יכולים ליצור זוגות של קווי תאים זהים למעט גורם סיכון אחד לפרקינסון. השוואה ביניהם חושפת בדיוק כיצד גנים מסוימים משפיעים על בריאות נוירוני הדופמין, על מאזן האנרגיה ועל הצטברות חלבונים. הסקירה מתארת דוגמאות רבות כאלה, כולל עריכות בגנים השולטים על המיטוכונדריה, מחזור חלבונים ותקשורת עצבית. היא כוללת גם גרסאות "מתג" של CRISPR שמגבירות או מדכאות ביטוי גנים ללא חיתוך ה‑DNA, ומערכות מעוצבות שמותאמות לשנות את אופן אריזת ה‑DNA — כל אלה מסייעים לכוונן את רמות האלפא‑סינוקלאין לטווחים בטוחים יותר.
תגים חכמים, מבחני לחץ וחיפושים בקנה מידה גדול
מעבר לחיתוכים פשוטים של גנים, CRISPR מאפשר לחוקרים להכניס תגים זוהרים או חלקים מייצרי אור זעירים לגנים מרכזיים. תגיות אלה מאפשרות להם לצפות בהתפתחות נוירוני הדופמין, לעקוב אחר צבירי אלפא‑סינוקלאין ולמדוד רמות חלבון ברגישות גבוהה במהלך בדיקות תרופות. כלים מהונדסים אחרים משתמשים באור כדי לגרום להצטברויות מהירות של אלפא‑סינוקלאין כך שאירועים רעילים מתרחשים בתוך ימים במקום שנים, מה שמאיץ את הגילוי. המאמר מדגיש גם מסכי CRISPR ברמת הגנום השלמים שמכבים אלפי גנים במקביל כדי למצוא רגולטורים נסתרי של אלפא‑סינוקלאין ושל מסלולי ניקיון המיטוכונדריה, ומצביעים על מטרות תרופתיות חדשות שהיו קשות לניחוש מראש.
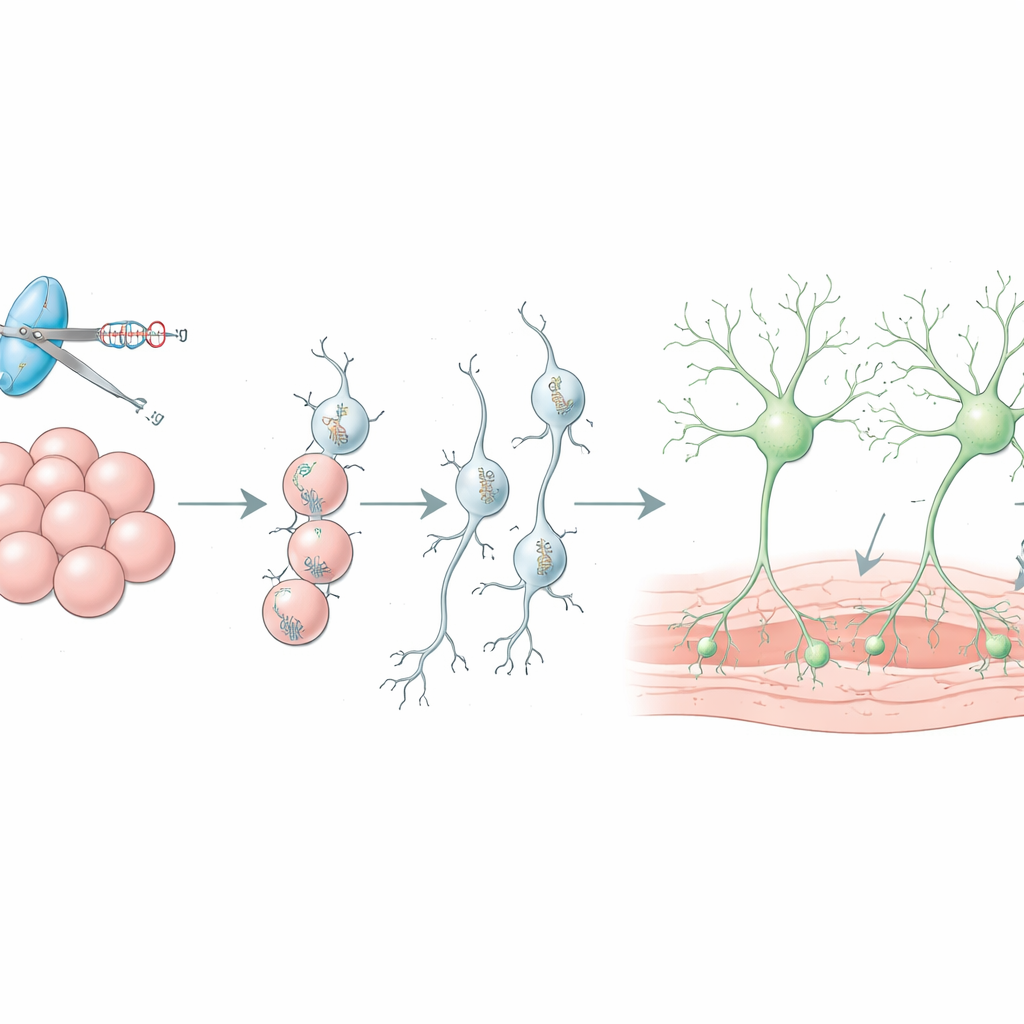
בניית שתלים תאים משופרים למוח
נוירוני דופמין שמקורם בתאי גזע כבר נבחנים בבני אדם כאמצעי להחלפת תאים שאבדו במחלת פרקינסון, אך בדרך כלל יותר מתשעים אחוזים מהתאים המושתלים מתים זמן קצר לאחר הניתוח, וסוגי תאים לא רצויים עלולים להשתלב בתרומה. הסקירה מסבירה כיצד משתמשים ב‑CRISPR בחיות חיות כדי לצוד גנים שמבקרים את הישרדות השתל, מה שמוביל לאסטרטגיות כגון חסימת אותות חיסון מסוימים עם תרופות קיימות כדי להגן על הנוירונים החדשים. היא גם מתארת כיצד תגי דוחות עוזרים למיין אצוות טהורים יותר של נוירוני דופמין לפני ההשתלה וכיצד מתגים כימוגנטיים, המוכנסים בעזרת CRISPR, מאפשרים לרופאים לכוון מרחוק את פעילות השתל כלפי מעלה או מטה באמצעות תרופות מעוצבות שאינן מזיקות.
מבט לעתיד טיפולים
במכלול, העבודה המסוכמת במאמר זה מראה ששילוב של תאי גזע אנושיים עם עריכת גנים מדויקת משנה את הדרך שבה מדענים לומדים ועלולים לטפל במחלת פרקינסון. כלים אלה יוצרים מודלים מבוססי אדם שמשקפים קרוב יותר את הנזק האיטי התלוי גיל שנצפה במטופלים ועוזרים לתכנן תאים מושתלים שהם בטוחים יותר, עמידים יותר ועמידים יותר מפני התפשטות חלבונים רעילים. בעוד שעוד נשארים שאלות מדעיות, בטיחותיות ואתיות רבות לפני שגישות כאלה יוכלו להפוך לטיפול שגרתי, מפת הדרך הזו מצביעה על עתיד שבו טיפולים שואפים לא רק להקל על תסמיני פרקינסון אלא להגן או לבנות מחדש את המעגלים המוחיים הפגיעים עצמם.
ציטוט: Park, S.B., Kim, JS., Ha, Y. et al. Human pluripotent stem cell engineering with CRISPR–Cas9 for Parkinson’s disease. Exp Mol Med 58, 993–1009 (2026). https://doi.org/10.1038/s12276-026-01679-2
מילות מפתח: מחלת פרקינסון, תאי גזע אנושיים, עריכת גנים CRISPR, נוירוני דופמין, טיפול תאי