Clear Sky Science · nl
Menselijke pluripotente stamcelengineering met CRISPR–Cas9 voor de ziekte van Parkinson
Waarom dit onderzoek van belang is voor het dagelijks leven
De ziekte van Parkinson berooft mensen van vloeiende beweging, spraak en zelfstandigheid, en de huidige medicijnen verlichten de symptomen vaak slechts tijdelijk. Dit artikel onderzoekt hoe wetenschappers twee krachtige instrumenten — menselijke stamcellen en DNA-knippende eiwitten bekend als CRISPR — combineren om beter te begrijpen waarom cruciale hersencellen afsterven bij Parkinson en om veiligere, langduriger celtherapieën te ontwerpen die op den duur verloren functies kunnen herstellen in plaats van de ziekte alleen te maskeren.
Inzicht in een veelvoorkomende hersenaandoening
De ziekte van Parkinson treft wereldwijd miljoenen mensen en komt vaker voor naarmate men ouder wordt. De aandoening draait om het geleidelijke verlies van dopamineproducerende zenuwcellen in een klein gebied van de middenhersenen en om ophopingen van een plakkerig eiwit genaamd alfa-synucleïne in cellen. Standaardbehandelingen zoals levodopa kunnen tijdelijk het ontbrekende dopamine vervangen, maar stoppen het afsterven van deze cellen niet. Diermodellen hebben aanwijzingen opgeleverd, maar slagen er vaak niet in het trage, mensgebonden ziekteverloop goed te vangen, waardoor grote kloften blijven tussen laboratoriumvondsten en bruikbare behandelingen voor patiënten.
Het kweken van menselijke zenuwcellen in het petrischaaltje
Menselijke pluripotente stamcellen, die in bijna elk celtype kunnen veranderen, stellen onderzoekers nu in staat grote aantallen menselijke dopamineproducerende neuronen in het laboratorium te laten groeien. Deze in het lab gekweekte cellen tonen veel kenmerken van Parkinson, waaronder problemen met de energiecentrales van de cel, afvalverwerkende systemen en de ophoping van alfa-synucleïne. Omdat ze ook gemaakt kunnen worden uit het weefsel van een persoon, dragen deze cellen de exacte genetische opmaak van die persoon, wat wetenschappers in staat stelt zowel erfelijke als de meer voorkomende sporadische vormen van de ziekte in een menselijke context na te bootsen en kandidaat-geneesmiddelen direct op kwetsbare celtypen te testen.
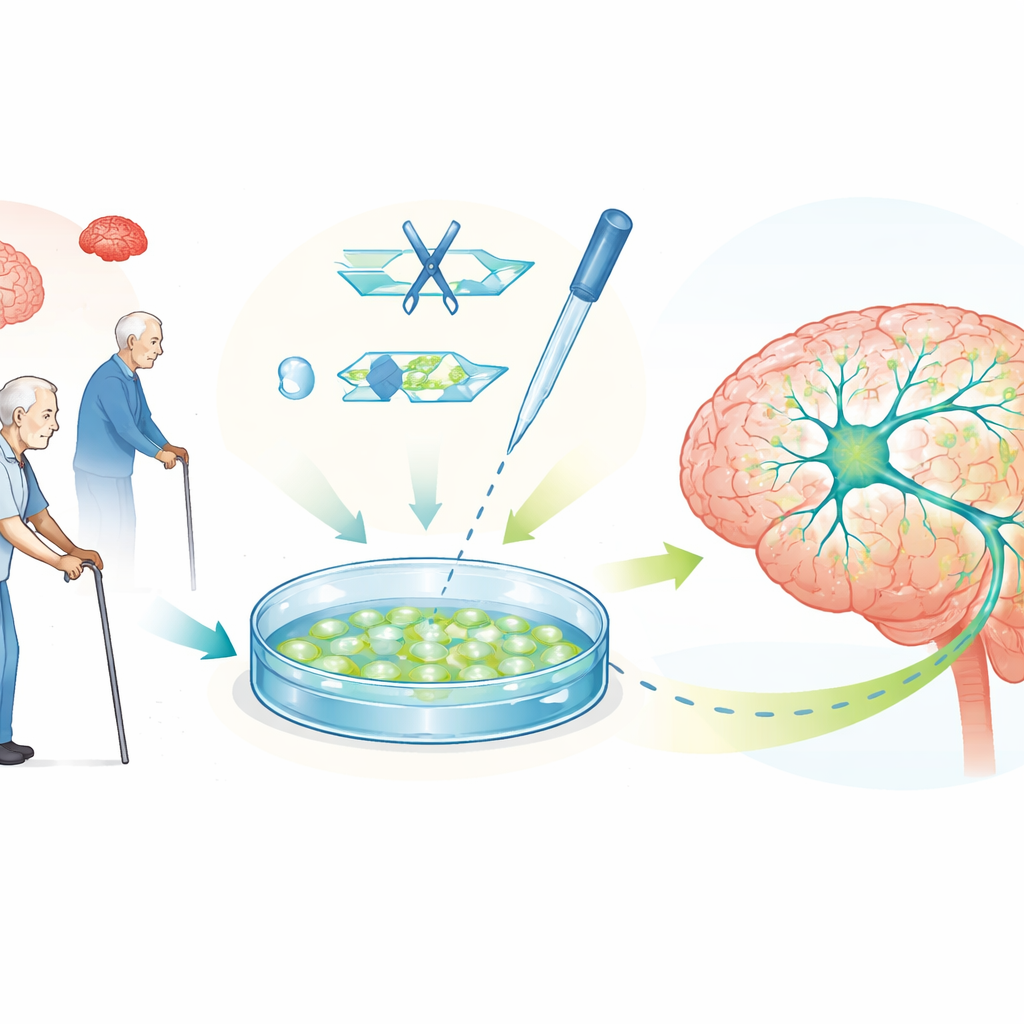
Genen bewerken om oorzaken te onderzoeken en ideeën te testen
CRISPR–Cas9, een nauwkeurig genbewerkingsinstrument, maakt deze stamcelmodellen veel krachtiger. Door enkele DNA-letters te veranderen, genen te verwijderen of mutaties te corrigeren, kunnen wetenschappers paren cellijnen creëren die identiek zijn behalve één Parkinson-risicofactor. Vergelijking daarvan onthult precies hoe bepaalde genen de gezondheid van dopaminerge neuronen, de energiebalans en eiwitophoping beïnvloeden. De review beschrijft vele voorbeelden, waaronder aanpassingen in genen die mitochondriën, eiwitrecycling en zenuwcelcommunicatie regelen. Ook komt de ‘schakelaarachtige’ versie van CRISPR aan bod die genen aan- of uitzet zonder DNA te knippen, en ontwerpsystemen die beïnvloeden hoe DNA wordt verpakt — allemaal hulpmiddelen om alfa-synucleïne tot veiligere niveaus te reguleren.
Slimme labels, stresstests en grootschalige zoektochten
Voorbij eenvoudige genknippen stelt CRISPR onderzoekers in staat lichtgevende labels of kleine lichtproducerende fragmenten in sleutelgenen in te voegen. Deze labels maken het mogelijk dopaminerge neuronen te volgen tijdens hun ontwikkeling, alfa-synucleïneklonten te traceren en eiwitniveaus zeer gevoelig te meten tijdens medicijntesten. Andere ontworpen hulpmiddelen gebruiken licht om snelle alfa-synucleïne-aggregatie te activeren, zodat toxische gebeurtenissen zich binnen dagen in plaats van jaren ontvouwen en de ontdekkingstijd verkort wordt. Het artikel belicht ook genoomwijde CRISPR-screens die duizenden genen gelijktijdig uitschakelen om verborgen regelaars van alfa-synucleïne en van het mitochondriale opruimproces te vinden, wat wijst op nieuwe medicijndoelen die moeilijk vooraf te raden zouden zijn geweest.
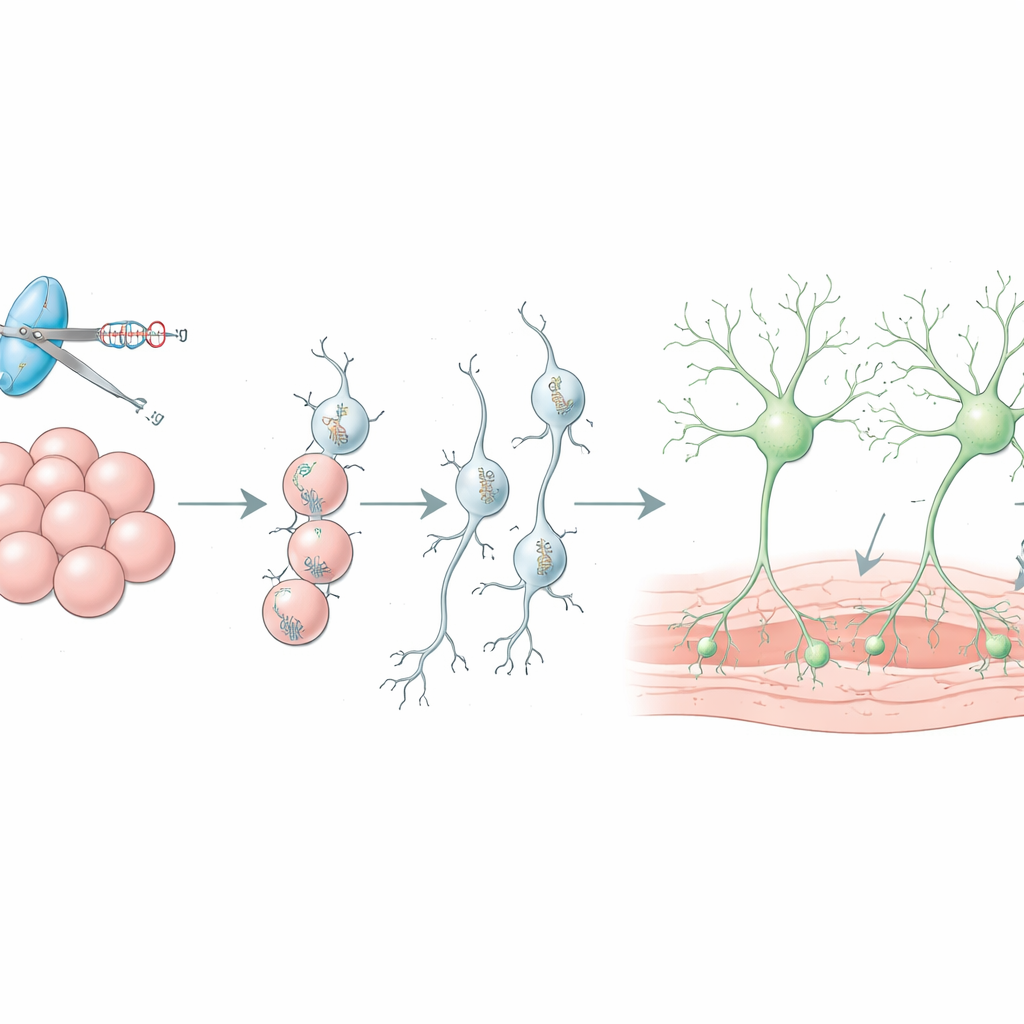
Betere celtransplantaten voor de hersenen bouwen
Uit stamcellen afgeleide dopaminerge neuronen worden al in mensen getest als manier om verloren cellen bij de ziekte van Parkinson te vervangen, maar vaak sterft meer dan negentig procent van de getransplanteerde cellen kort na de operatie, en ongewenste celtypen kunnen in het transplantaat terechtkomen. De review legt uit hoe CRISPR in levende dieren wordt gebruikt om genen te zoeken die transplantaatoverleving sturen, wat leidt tot strategieën zoals het blokkeren van specifieke immuunsignalen met bestaande medicijnen om nieuwe neuronen te beschermen. Ook wordt beschreven hoe reporterlabels helpen om zuiverdere partijen dopaminerge neuronen te sorteren vóór implantatie en hoe chemogenetische schakelaars, ingebracht met CRISPR, artsen in staat stellen de activiteit van het transplantaat op afstand hoger of lager te zetten met behulp van onschadelijke designerdrugs.
Vooruitkijken naar toekomstige behandelingen
Gezamenlijk toont het in dit artikel samengevatte werk aan dat de combinatie van menselijke stamcellen met precieze genbewerking de manier waarop wetenschappers Parkinson bestuderen en mogelijk behandelen opnieuw vormgeeft. Deze instrumenten creëren mensgerichte modellen die het langzame, leeftijdsgebonden letsel bij patiënten beter weerspiegelen en helpen bij het ontwerpen van getransplanteerde cellen die veiliger, robuuster en beter bestand zijn tegen de verspreiding van toxische eiwitten. Hoewel veel wetenschappelijke, veiligheids- en ethische vragen blijven voordat dergelijke benaderingen standaardzorg kunnen worden, schetst deze routekaart een toekomst waarin therapieën niet alleen gericht zijn op het verlichten van Parkinson-symptomen, maar op het beschermen of herbouwen van de kwetsbare hersencircuits zelf.
Bronvermelding: Park, S.B., Kim, JS., Ha, Y. et al. Human pluripotent stem cell engineering with CRISPR–Cas9 for Parkinson’s disease. Exp Mol Med 58, 993–1009 (2026). https://doi.org/10.1038/s12276-026-01679-2
Trefwoorden: Ziekte van Parkinson, menselijke stamcellen, CRISPR-genbewerking, dopaminerge neuronen, celtherapie