Clear Sky Science · zh
通过基因和药物操控H3K9甲基转移酶Suv39h1释放HMGB2转录以促进肝脏再生
这对肝脏健康为何重要
我们的肝脏在受损后具有显著的再生能力,但在许多患者中,这一自然修复过程不足以阻止肝功能衰竭。本研究提出了一个简单但影响深远的问题:是否存在一种分子“刹车”抑制肝脏再生,如果存在,能否安全地放松该刹车以帮助受损肝脏恢复?
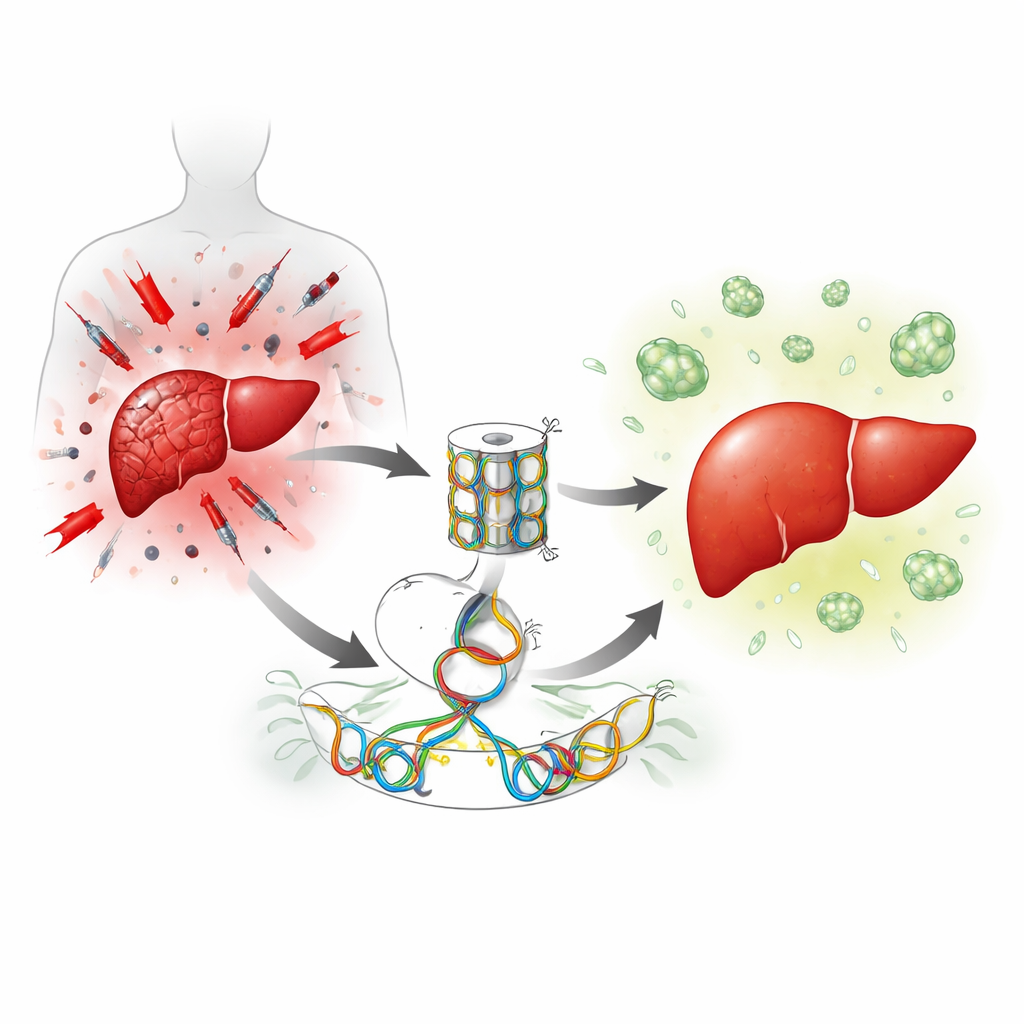
内置的肝脏再生制动器
肝脏主要通过促使处于静止期的肝细胞重新进入分裂来修复自身。作者聚焦于一种名为Suv39h1的酶,它通过紧缩DNA包装来维持基因沉默。在小鼠肝脏手术后,肝细胞内Suv39h1的水平短暂下降,这一变化受另一种在DNA上添加化学标记的酶控制。这提示Suv39h1通常可能充当抑制肝细胞增殖所需基因的刹车,释放这一刹车或可加速再生。
在小鼠中移除刹车
为检验这一想法,研究团队使用了在全身或仅在肝细胞中删除Suv39h1基因的小鼠。在正常条件下,这些动物与健康同窝鼠无异。但当通过手术切除大部分肝脏或用毒素损伤肝脏时,缺失Suv39h1的小鼠肝组织再生更快,分裂的肝细胞更多,并且在严重手术后存活率更高。这些益处似乎特异于Suv39h1的缺失,因为删除其近亲Suv39h2并未改善肝脏恢复。
一个被隐藏的辅助基因被释放
通过检查再生肝细胞中哪些基因被开启或关闭,研究人员发现了一个突出的参与者:HMGB2,一种帮助塑造DNA并调控众多其他基因的蛋白。当Suv39h1缺失时,HMGB2在已知生长信号作用下显著上调。进一步实验表明,Suv39h1通常与一种与基因沉默相关的化学标记一起位于HMGB2的调控区域。当Suv39h1和该标记被去除后,另一种因子即可结合并激活HMGB2。阻断HMGB2会消除Suv39h1缺失肝细胞的生长优势,而在小鼠中降低HMGB2则减慢肝脏再生,表明一旦刹车被释放,HMGB2就是关键的助力因子。
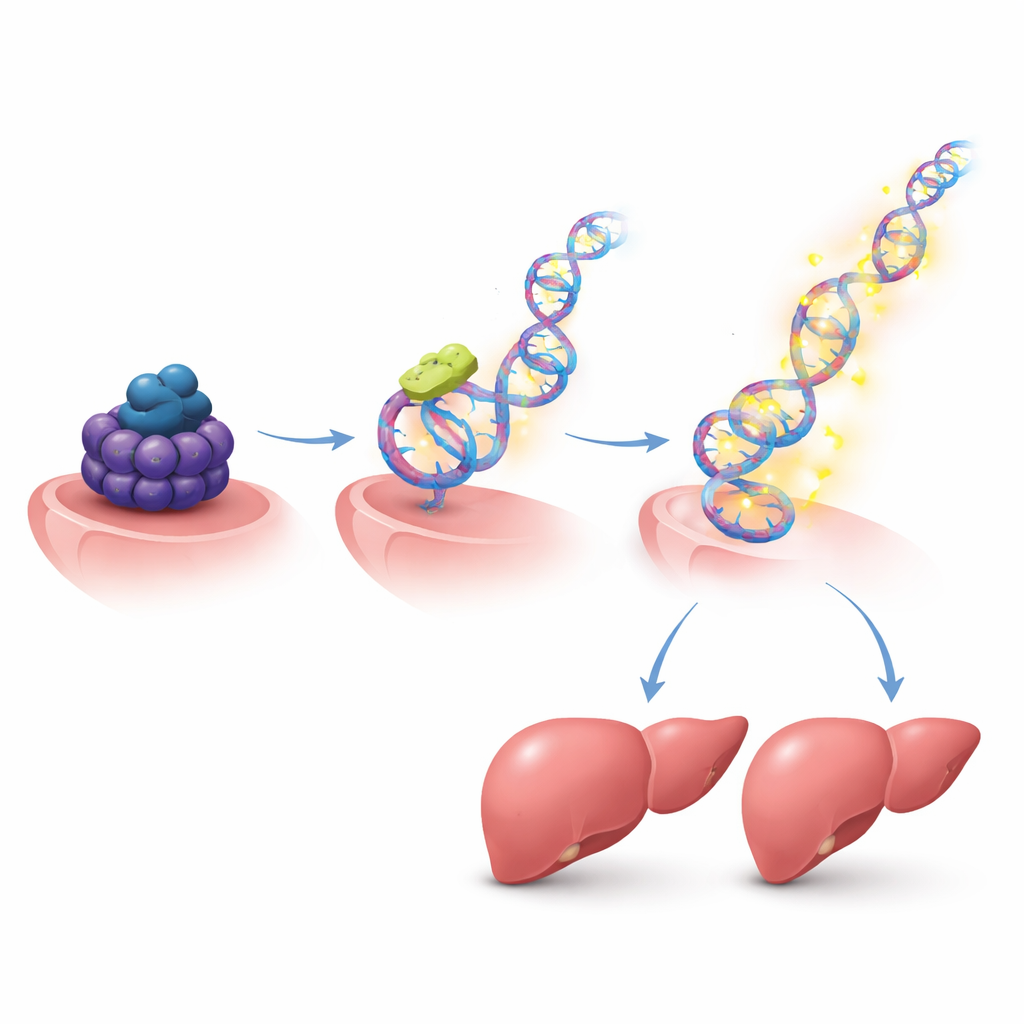
重连多基因的生长回路
由于HMGB2本身控制着广泛的基因网络,作者绘制了其在全基因组的活性图谱。在被刺激分裂的肝细胞中,HMGB2聚集到许多与细胞周期和再生相关基因的调控区。当HMGB2被降低时,这些与生长相关的基因群体出现显著变化,肝细胞的分裂减少。在这些靶基因中包括肝脏修复中已知的参与者,如信号分子、细胞表面受体以及驱动细胞周期的因子。这提示一旦Suv39h1允许HMGB2上升,HMGB2反过来会调节整个促生长程序。
药物线索与人类肝样本的迹象
研究团队随后探讨是否可用药物暂时削弱Suv39h1。用chaetocin处理的小鼠(该化合物可降低Suv39h1所形成的特定化学标记)在大范围手术或毒素损伤后表现出更强的肝脏再生、更多分裂细胞及更好的存活率。最后,在急性肝衰竭患者的肝脏样本中,较高的SUV39H1水平与更多组织损伤和更少的分裂细胞相关,而较高的HMGB2及其若干伙伴基因则与更好的再生迹象和较少损伤相关联。
这对未来治疗意味着什么
简言之,该研究揭示了一条控制链:Suv39h1将强大的生长助手HMGB2严密锁定。当这把锁被放松时,HMGB2可以开启许多有助于肝细胞增殖和替代受损组织的基因。谨慎地针对Suv39h1,未来可能通过比本研究所用更安全、更精确的药物来支持那些自身再生能力衰弱患者的肝脏恢复,但在将此类方法用于临床测试之前仍需大量工作。
引用: Lu, Y., Zhou, J., Miao, X. et al. Genetic and pharmaceutical manipulation of H3K9 methyltransferase Suv39h1 promotes liver regeneration by unleashing HMGB2 transcription. Exp Mol Med 58, 1158–1171 (2026). https://doi.org/10.1038/s12276-026-01677-4
关键词: 肝脏再生, 表观遗传学, Suv39h1, HMGB2, chaetocin