Clear Sky Science · ar
التحكم الجيني والدوائي في ميثيلترانسفيراز H3K9 Suv39h1 يعزز تجدد الكبد عبر تحرير نسخ HMGB2
لماذا هذا مهم لصحة الكبد
يمتلك كبدنا قدرة ملحوظة على النمو مرة أخرى بعد الإصابة، لكن عند كثير من المرضى تكون عملية الإصلاح الطبيعية ضعيفة للغاية بحيث لا تمنع فشل الكبد. تطرح هذه الدراسة سؤالًا بسيطًا ذو تداعيات كبيرة: هل هناك "مِكبح" جزيئي يعيق إعادة نمو الكبد، وإذا وُجد، هل يمكننا تخفيف هذا المكبح بأمان لمساعدة الكبد التالف على التعافي؟
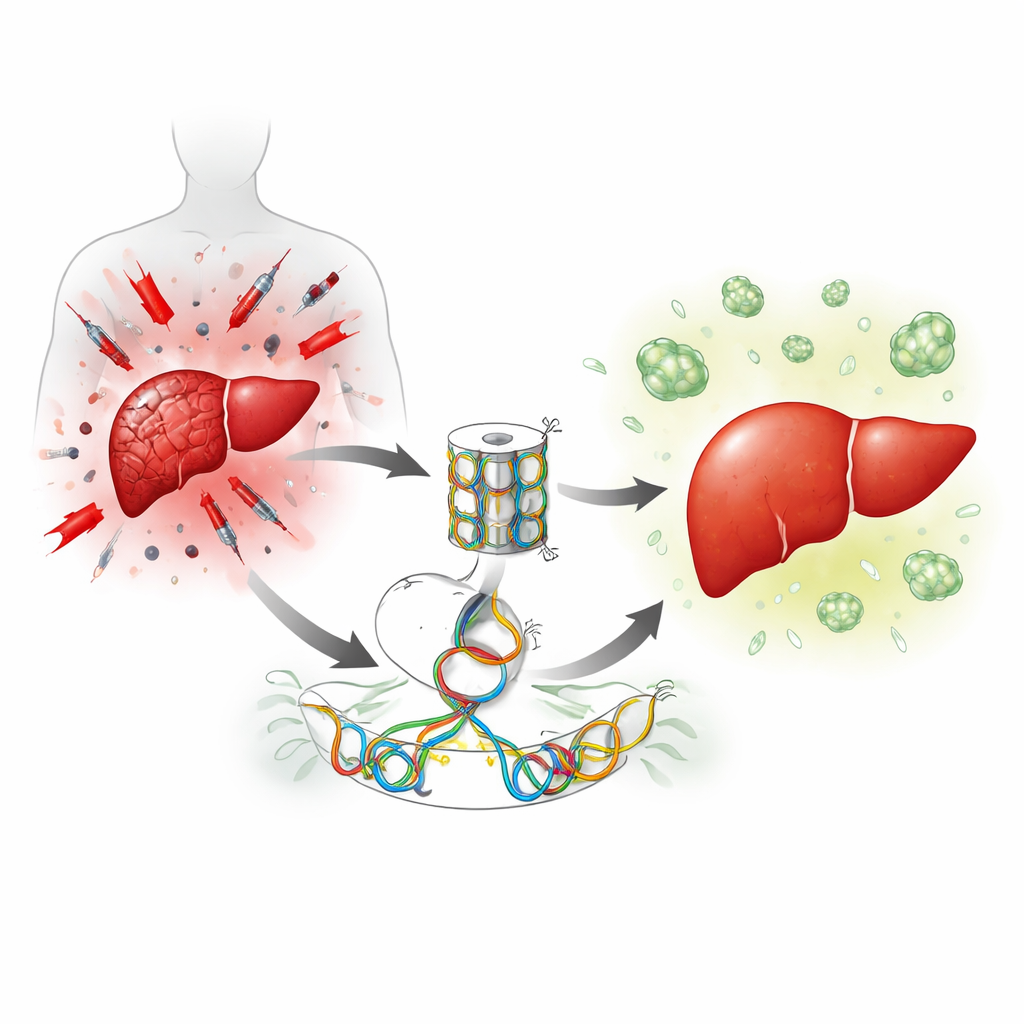
مكبح مدمج على إعادة نمو الكبد
يُصلح الكبد نفسه أساسًا عن طريق حث الخلايا الكبدية الراحة على بدء الانقسام من جديد. ركز المؤلفون على إنزيم يُدعى Suv39h1 يساعد على إبقاء الجينات مطفأة عن طريق تشديد طريقة تغليف الحمض النووي. بعد إجراء جراحة للكبد في الفئران، تنخفض مستويات Suv39h1 مؤقتًا في الخلايا الكبدية، بتأثير إنزيم آخر يضيف علامات كيميائية على الحمض النووي. أشار ذلك إلى أن Suv39h1 قد يعمل عادة كمكبح على الجينات اللازمة لتكاثر خلايا الكبد، وأن تحرير هذا المكبح قد يسرع التجدد.
إزالة المكبح في الفئران
لاختبار هذه الفكرة، استخدم الفريق فئرانًا حُذفت فيها جينة Suv39h1 إما في الجسم كله أو فقط في الخلايا الكبدية. في الظروف الطبيعية بدا هؤلاء الحيوانات مثل إخوتهم الأصحاء. لكن عندما أُزيل معظم الكبد جراحيًا أو تضرر بواسطة سم، أعادت الفئران التي تفتقر إلى Suv39h1 نسيج الكبد بسرعة أكبر، وكان لديها خلايا كبدية منقسمة أكثر، ونجت بشكل أفضل من الجراحة الشديدة. بدت هذه الفوائد محددة بفقدان Suv39h1، إذ أن حذف القريب المقارب Suv39h2 لم يحسّن تعافي الكبد.
إطلاق جين مساعد مخفي
من خلال فحص أي الجينات تُفتح وتُغلق في الخلايا الكبدية المتجددة، وجد الباحثون لاعبًا بارزًا واحدًا: HMGB2، بروتين يساعد في تشكيل الحمض النووي والسيطرة على العديد من الجينات الأخرى. عند غياب Suv39h1، ارتفعت مستويات HMGB2 بقوة استجابةً لإشارات النمو المعروفة. أظهرت تجارب إضافية أن Suv39h1 يجلس عادةً على منطقة التحكم في HMGB2 جنبًا إلى جنب مع علامة كيميائية مرتبطة بكتم الجينات. عند إزالة Suv39h1 وهذه العلامة، تمكن عامل آخر من الارتباط وتنشيط HMGB2. أدى حجب HMGB2 إلى محو ميزة النمو لدى خلايا الكبد ناقصة Suv39h1، وخفض HMGB2 في الفئران أبطأ إعادة نمو الكبد، مما يُظهر أن HMGB2 مساعد حاسم بمجرد تحرير المكبح.
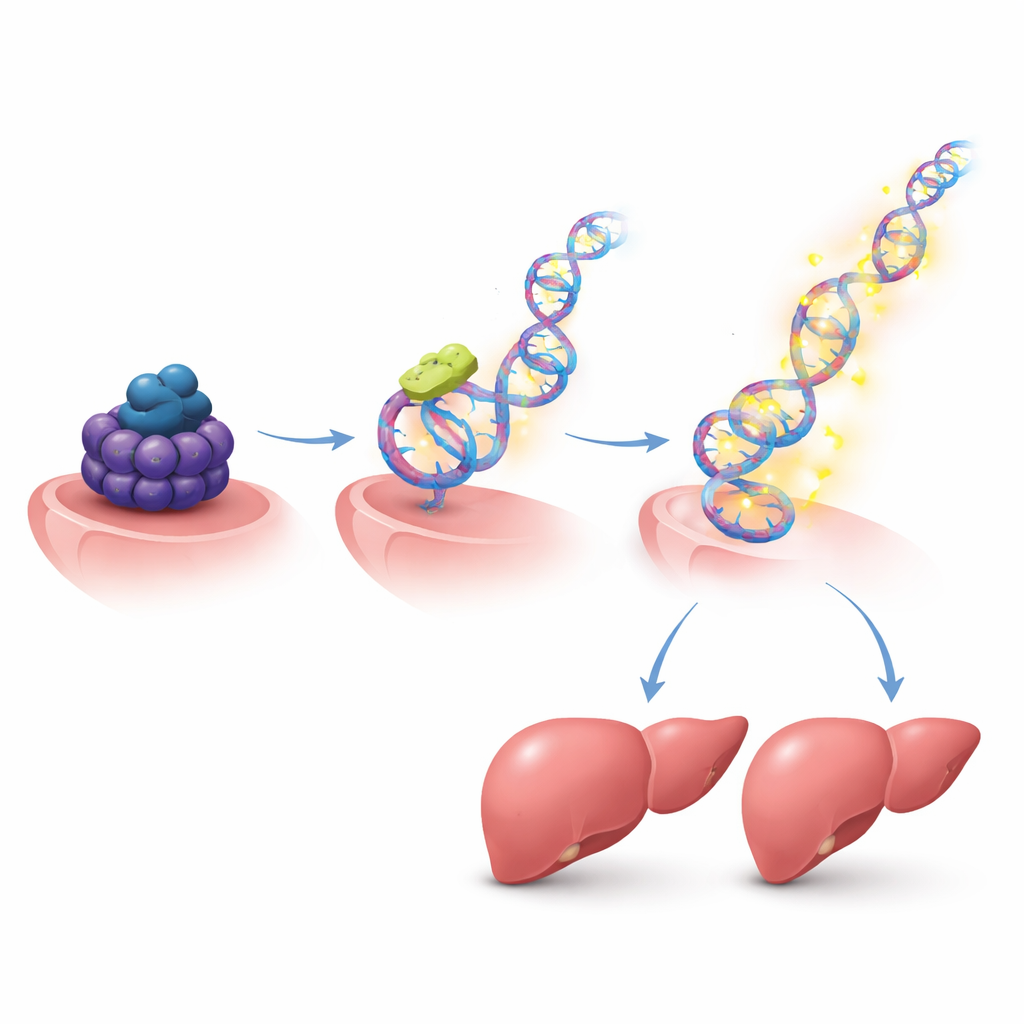
إعادة توصيل دوائر النمو عبر العديد من الجينات
بما أن HMGB2 نفسه يتحكم في شبكة واسعة من الجينات، قام المؤلفون برسم نشاطه عبر الجينوم. في الخلايا الكبدية المحفزة على الانقسام، تجمّع HMGB2 في مناطق التحكم بالعديد من الجينات المرتبطة بدورة الخلية والتجدد. عندما نُقص HMGB2، تغير نشاط مجموعة كبيرة من هذه الجينات المرتبطة بالنمو، وانقسمت خلايا الكبد أقل. من بين الأهداف كانت لاعبين معروفين في إصلاح الكبد، بما في ذلك جزيئات الإشارة، ومستقبلات على سطح الخلية، وعوامل تدفع دورة الخلية. يشير ذلك إلى أنه بمجرد أن يسمح Suv39h1 بارتفاع HMGB2، يقوم HMGB2 بدوره بضبط برنامج معزز للنمو بأكمله.
لمحة عن دواء وإشارات في أكباد بشرية
استكشف الفريق بعد ذلك ما إذا كان دواء يمكنه إضعاف Suv39h1 مؤقتًا. أظهرت الفئران المعالجة بالـ chaetocin، وهو مركب يخفض العلامة الكيميائية الخاصة التي يُنشئها Suv39h1، تجدد كبد أقوى، وخلايا منقسمة أكثر، وبقاء أفضل بعد جراحة واسعة أو إصابة بالسم. أخيرًا، في عينات كبد من أشخاص يعانون فشلًا كبديًا حادًا، ارتبطت مستويات أعلى من SUV39H1 بمزيد من تلف النسيج وعدد أقل من الخلايا المنقسمة، بينما ارتبطت مستويات أعلى من HMGB2 وعدد من جيناته الشريكة بعلامات أفضل للتجدد وأقل إصابة.
ماذا يعني هذا للعلاج في المستقبل
بعبارة بسيطة، تكشف الدراسة سلسلة تحكّم حيث يُبقي Suv39h1 مساعد نمو قويًا، HMGB2، مغلقًا بإحكام. عندما يُرخى هذا القفل، يمكن لـ HMGB2 تشغيل العديد من الجينات التي تساعد خلايا الكبد على التكاثر واستبدال النسيج التالف. قد يدعم استهداف Suv39h1 بعناية، على الأرجح بأدوية أكثر أمانًا ودقة مما استُخدم هنا، يومًا ما تعافي الكبد لدى المرضى الذين تفشل قدرتهم التجددية، رغم أن هناك الكثير من العمل قبل أن يُختبر مثل هذا النهج في العيادة.
الاستشهاد: Lu, Y., Zhou, J., Miao, X. et al. Genetic and pharmaceutical manipulation of H3K9 methyltransferase Suv39h1 promotes liver regeneration by unleashing HMGB2 transcription. Exp Mol Med 58, 1158–1171 (2026). https://doi.org/10.1038/s12276-026-01677-4
الكلمات المفتاحية: تجدد الكبد, علم التخلق الجنيني اللاجيني (الإيبيجينيك), Suv39h1, HMGB2, chaetocin