Clear Sky Science · pt
Manipulação genética e farmacêutica da metiltransferase de H3K9 Suv39h1 promove a regeneração hepática ao liberar a transcrição de HMGB2
Por que isso importa para a saúde do fígado
Nossos fígados têm uma capacidade notável de regenerar-se após lesão, mas em muitos pacientes esse processo natural de reparo é fraco demais para evitar a insuficiência hepática. Este estudo faz uma pergunta simples com grandes implicações: existe um “freio” molecular que retém o crescimento do fígado e, em caso afirmativo, podemos aliviar esse freio com segurança para ajudar fígados danificados a se recuperar?
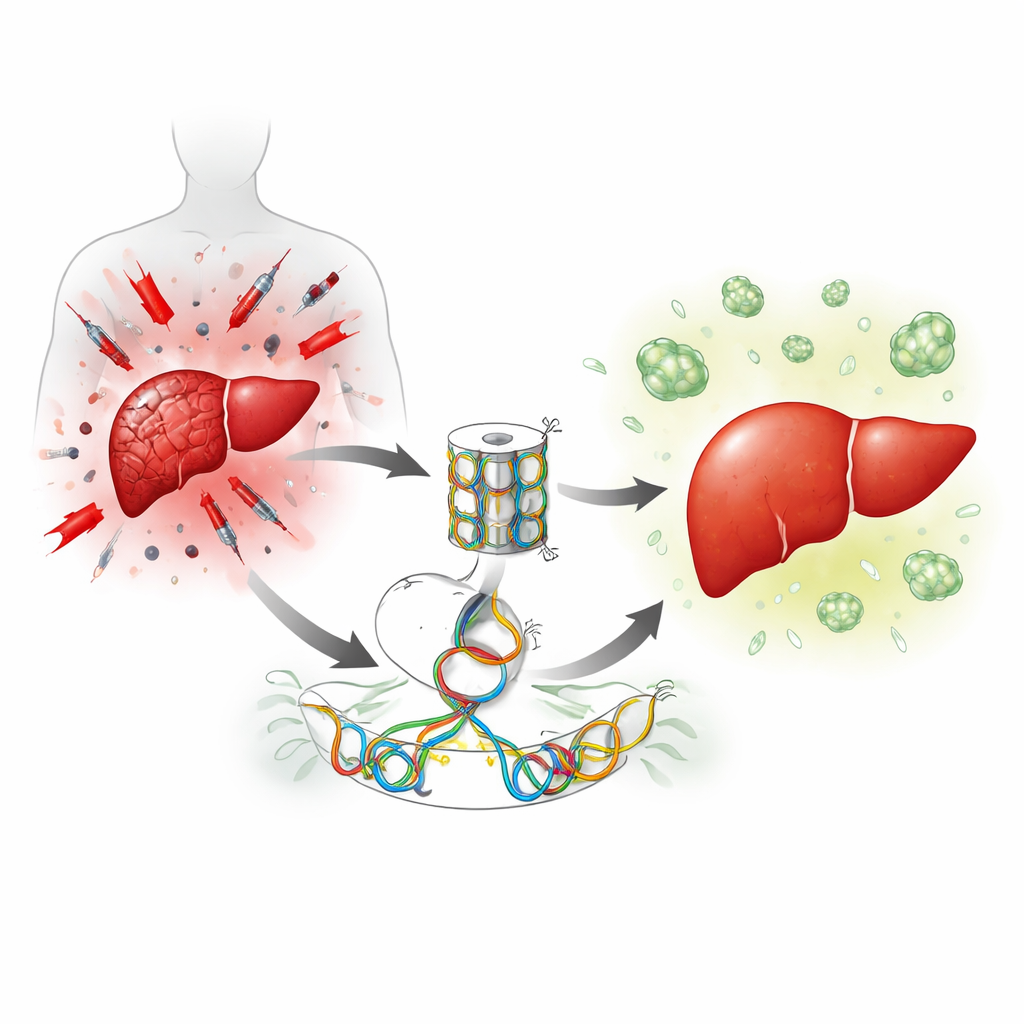
Um freio embutido no crescimento hepático
O fígado se repara principalmente pedindo que células hepáticas em repouso voltem a se dividir. Os autores focaram em uma enzima chamada Suv39h1 que ajuda a manter genes desligados ao condensar a embalagem do DNA. Após cirurgia hepática em camundongos, os níveis de Suv39h1 nas células do fígado caem brevemente, controlados por outra enzima que adiciona marcas químicas ao DNA. Isso sugeriu que Suv39h1 normalmente pode agir como um freio em genes necessários para a multiplicação das células hepáticas, e que liberar esse freio poderia acelerar a regeneração.
Removendo o freio em camundongos
Para testar essa ideia, a equipe usou camundongos nos quais o gene Suv39h1 foi eliminado em todo o organismo ou somente nas células do fígado. Em condições normais, esses animais pareciam como seus parentes saudáveis. Mas quando a maior parte do fígado foi removida cirurgicamente ou danificada com uma toxina, camundongos sem Suv39h1 regeneraram o tecido hepático mais rápido, tiveram mais células hepáticas em divisão e sobreviveram melhor a cirurgias severas. Esses benefícios pareceram ocorrer especificamente quando Suv39h1 foi perdido, já que excluir seu par próximo Suv39h2 não melhorou a recuperação do fígado.
Um gene ajudante escondido é liberado
Ao examinar quais genes eram ativados e desativados em células hepáticas em regeneração, os pesquisadores encontraram um protagonista de destaque: HMGB2, uma proteína que ajuda a moldar o DNA e controlar muitos outros genes. Quando Suv39h1 estava ausente, os níveis de HMGB2 aumentaram fortemente em resposta a sinais conhecidos de crescimento. Experimentos adicionais mostraram que Suv39h1 normalmente se localiza na região de controle do HMGB2 junto com uma marca química associada ao silenciamento gênico. Quando Suv39h1 e essa marca foram removidos, outro fator pôde se ligar e ativar o HMGB2. Bloquear o HMGB2 eliminou a vantagem de crescimento das células hepáticas deficientes em Suv39h1, e reduzir o HMGB2 em camundongos retardou a regeneração do fígado, mostrando que o HMGB2 é um ajudante crucial uma vez que o freio é liberado.
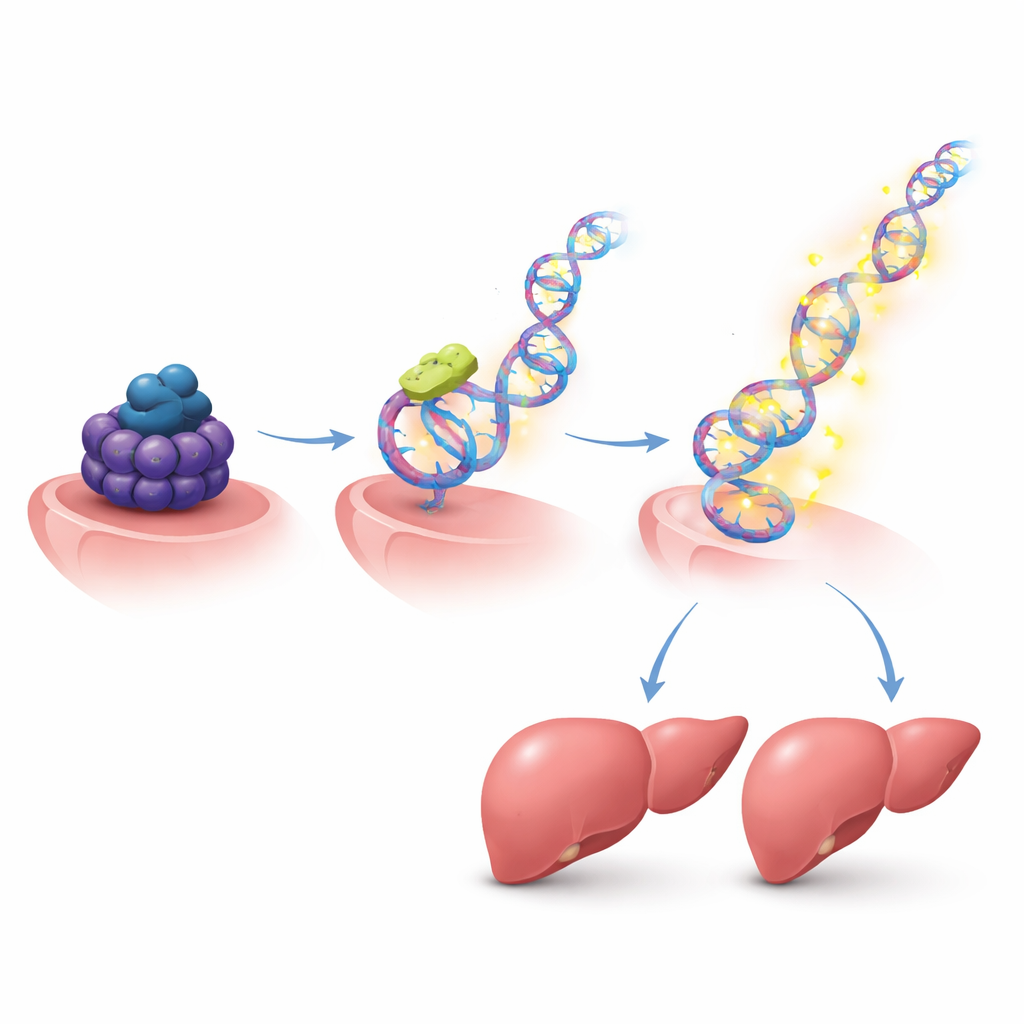
Reconfigurando circuitos de crescimento por muitos genes
Porque o próprio HMGB2 controla uma ampla rede de genes, os autores mapearam sua atividade pelo genoma. Em células hepáticas estimuladas a se dividir, o HMGB2 se concentrava nas regiões de controle de muitos genes relacionados ao ciclo celular e à regeneração. Quando o HMGB2 foi reduzido, uma grande coleção desses genes ligados ao crescimento alterou sua atividade, e as células hepáticas dividiram-se menos. Entre os alvos estavam participantes bem conhecidos na reparação hepática, incluindo moléculas de sinalização, receptores na superfície celular e fatores que impulsionam o ciclo celular. Isso sugere que, uma vez que Suv39h1 permite a elevação do HMGB2, o HMGB2 por sua vez ajusta todo um programa pró-crescimento.
Uma pista farmacológica e sinais em fígados humanos
A equipe então explorou se um fármaco poderia enfraquecer temporariamente o Suv39h1. Camundongos tratados com chaetocin, um composto que reduz a marca química específica que o Suv39h1 gera, apresentaram regeneração hepática mais forte, mais células em divisão e melhor sobrevivência após cirurgia extensa ou lesão por toxina. Finalmente, em amostras de fígado de pessoas com insuficiência hepática aguda, níveis mais altos de SUV39H1 estiveram associados a mais dano tecidual e menos células em divisão, enquanto níveis mais altos de HMGB2 e de vários de seus genes parceiros se correlacionaram com sinais melhores de regeneração e menos lesão.
O que isso significa para tratamentos futuros
Em termos simples, o estudo revela uma cadeia de controle em que Suv39h1 mantém um poderoso ajudante de crescimento, o HMGB2, firmemente trancado. Quando essa trava é afrouxada, o HMGB2 pode ativar muitos genes que ajudam as células hepáticas a multiplicar-se e substituir o tecido danificado. Alvo cuidadoso do Suv39h1, provavelmente com fármacos mais seguros e precisos do que os usados aqui, pode um dia apoiar a recuperação hepática em pacientes cuja capacidade regenerativa é insuficiente, embora muito trabalho ainda seja necessário antes que essa abordagem possa ser testada na clínica.
Citação: Lu, Y., Zhou, J., Miao, X. et al. Genetic and pharmaceutical manipulation of H3K9 methyltransferase Suv39h1 promotes liver regeneration by unleashing HMGB2 transcription. Exp Mol Med 58, 1158–1171 (2026). https://doi.org/10.1038/s12276-026-01677-4
Palavras-chave: regeneração do fígado, epigenética, Suv39h1, HMGB2, chaetocin