Clear Sky Science · de
Genetische und pharmakologische Manipulation der H3K9‑Methyltransferase Suv39h1 fördert die Leberregeneration durch Freisetzung der HMGB2‑Transkription
Warum das für die Lebergesundheit wichtig ist
Unsere Lebern verfügen über eine bemerkenswerte Fähigkeit zur Regeneration, doch bei vielen Patientinnen und Patienten reicht diese natürliche Reparatur nicht aus, um ein Leberversagen zu verhindern. Die Studie stellt eine einfache, aber weitreichende Frage: Gibt es eine molekulare „Bremse“, die das Nachwachsen der Leber bremst, und wenn ja, kann man diese Bremse sicher lösen, um geschädigten Lebern zu helfen?
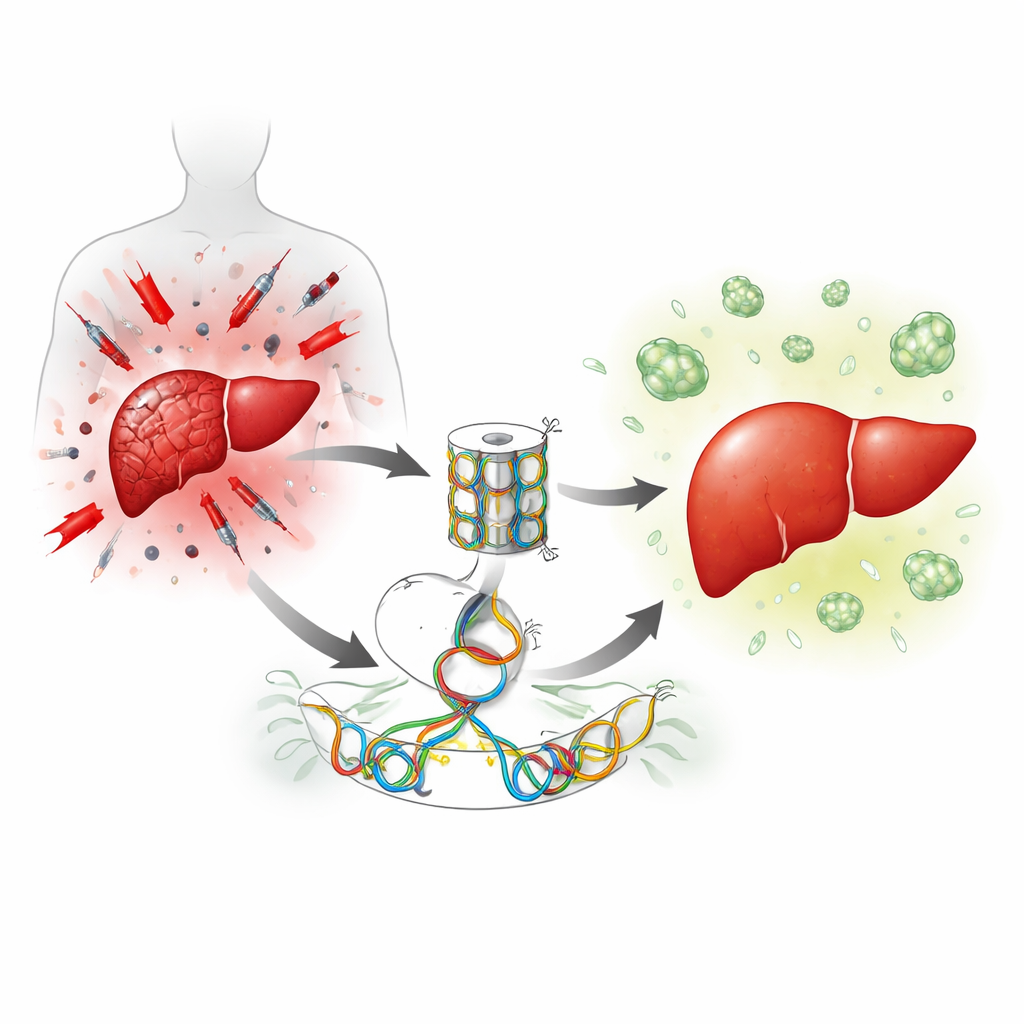
Eine eingebaute Bremse für das Leberwachstum
Die Leber repariert sich vor allem dadurch, dass ruhende Leberzellen zur erneuten Teilung aufgefordert werden. Die Autoren konzentrierten sich auf ein Enzym namens Suv39h1, das Gene durch Straffen der DNA‑Verpackung stumm hält. Nach Leberchirurgie bei Mäusen fallen die Suv39h1‑Spiegel in Leberzellen kurzzeitig ab, gesteuert von einem anderen Enzym, das chemische Markierungen an der DNA anbringt. Das deutete darauf hin, dass Suv39h1 normalerweise als Bremse für Gene wirkt, die für die Vermehrung von Leberzellen nötig sind, und dass das Lösen dieser Bremse die Regeneration beschleunigen könnte.
Die Bremse bei Mäusen entfernen
Um diese Idee zu prüfen, verwendete das Team Mäuse, bei denen das Suv39h1‑Gen entweder im ganzen Körper oder nur in Leberzellen entfernt wurde. Unter normalen Bedingungen wirkten diese Tiere wie ihre gesunden Wurfgeschwister. Wurde jedoch der Großteil der Leber chirurgisch entfernt oder durch ein Toxin geschädigt, wuchsen die Lebern der Suv39h1‑freien Mäuse schneller nach, es gab mehr teilende Leberzellen und sie überlebten schwere Eingriffe besser. Diese Vorteile traten spezifisch bei Verlust von Suv39h1 auf, da die Deletion seines nahen Verwandten Suv39h2 die Lebererholung nicht verbesserte.
Ein verborgenes Helfergen wird freigesetzt
Durch die Analyse der Gene, die in regenerierenden Leberzellen an‑ oder abgeschaltet wurden, identifizierten die Forschenden einen herausragenden Akteur: HMGB2, ein Protein, das die DNA‑Struktur mitprägt und viele andere Gene reguliert. Fehlt Suv39h1, steigen die HMGB2‑Spiegel stark als Antwort auf bekannte Wachstumssignale. Weitere Experimente zeigten, dass Suv39h1 normalerweise zusammen mit einer chemischen Markierung, die mit Genstille assoziiert ist, an der Kontrollregion von HMGB2 sitzt. Werden Suv39h1 und diese Markierung entfernt, kann ein anderer Faktor binden und HMGB2 aktivieren. Die Blockade von HMGB2 beseitigte den Wachstumsvorteil von Suv39h1‑defizienten Leberzellen, und die Reduktion von HMGB2 bei Mäusen verlangsamte die Leberregeneration, was zeigt, dass HMGB2 ein entscheidender Helfer ist, sobald die Bremse gelöst ist.
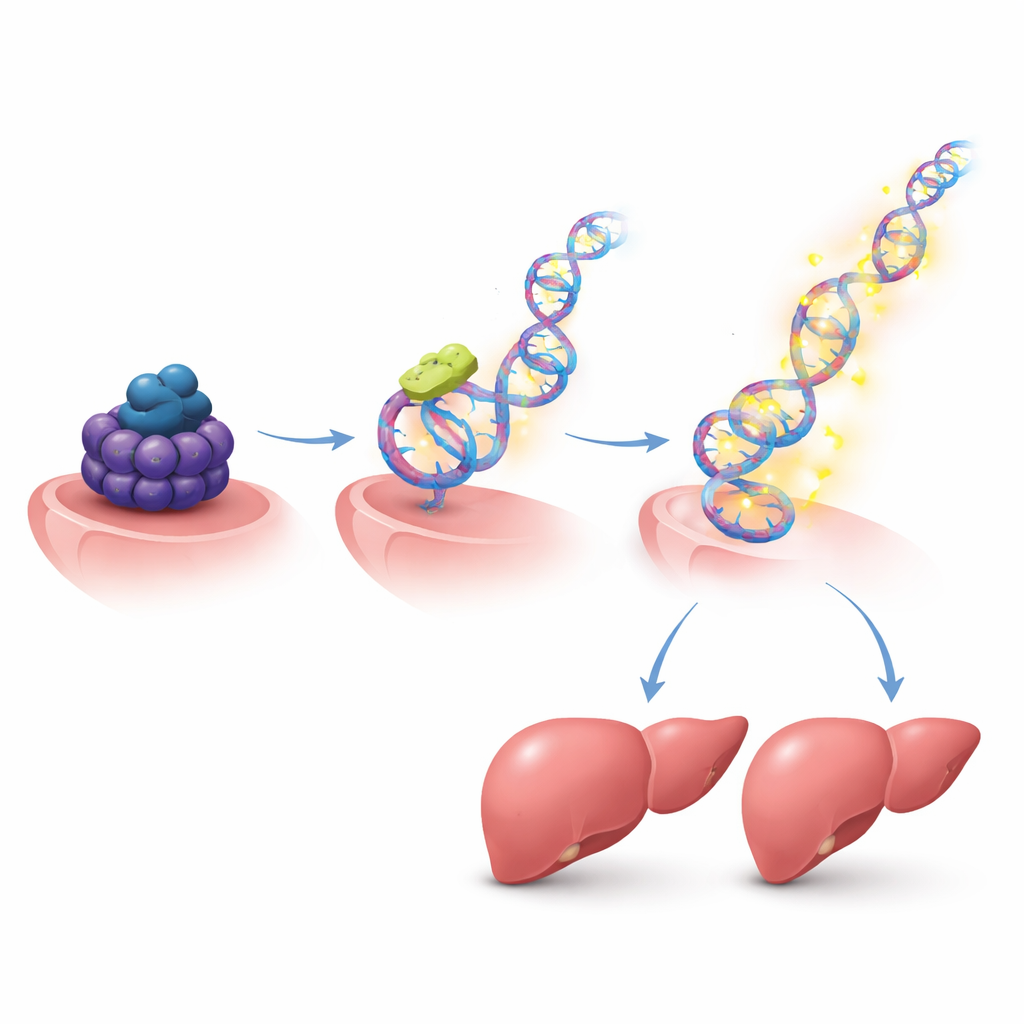
Umschalten von Wachstumsprogrammen über viele Gene
Da HMGB2 selbst ein weites Netzwerk von Genen kontrolliert, kartierten die Autoren seine Aktivität im ganzen Genom. In Leberzellen, die zur Teilung angeregt wurden, fand HMGB2 sich an Kontrollregionen vieler Gene, die mit Zellzyklus und Regeneration verbunden sind. Bei Reduktion von HMGB2 veränderte sich die Aktivität einer großen Gruppe dieser wachstumsbezogenen Gene, und Leberzellen teilten sich weniger. Unter den Zielgenen fanden sich bekannte Akteure der Leberreparatur, darunter Signalmoleküle, Rezeptoren an der Zelloberfläche und Faktoren, die den Zellzyklus antreiben. Das legt nahe, dass, sobald Suv39h1 das Ansteigen von HMGB2 zulässt, HMGB2 seinerseits ein komplettes pro‑Wachstumsprogramm einstellt.
Hinweis auf ein Medikament und Befunde in menschlichen Lebern
Das Team untersuchte dann, ob ein Medikament Suv39h1 vorübergehend abschwächen kann. Mäuse, die mit Chaetocin behandelt wurden — einer Verbindung, die die spezifische chemische Markierung senkt, die Suv39h1 erzeugt — zeigten stärkere Leberregeneration, mehr teilende Zellen und bessere Überlebensraten nach umfangreicher Operation oder Toxin‑Schädigung. Schließlich korrelierten in Lebergewebeproben von Menschen mit akutem Leberversagen höhere SUV39H1‑Spiegel mit mehr Gewebeschäden und weniger teilenden Zellen, während höhere HMGB2‑Werte und mehrere seiner Partnergene mit besseren Hinweisen auf Regeneration und weniger Schädigung verbunden waren.
Was das für zukünftige Therapien bedeutet
Kurz gesagt zeigt die Studie eine Kontrollkette, in der Suv39h1 einen mächtigen Wachstumshelfer, HMGB2, fest verschlossen hält. Wird dieses Schloss gelockert, kann HMGB2 viele Gene einschalten, die Leberzellen helfen, sich zu vermehren und beschädigtes Gewebe zu ersetzen. Eine gezielte Ansteuerung von Suv39h1, vermutlich mit sichereren und präziseren Wirkstoffen als den hier verwendeten, könnte eines Tages die Leberregeneration bei Patientinnen und Patienten unterstützen, deren eigene Regenerationskraft versagt — doch bis zu klinischen Prüfungen ist noch viel Arbeit nötig.
Zitation: Lu, Y., Zhou, J., Miao, X. et al. Genetic and pharmaceutical manipulation of H3K9 methyltransferase Suv39h1 promotes liver regeneration by unleashing HMGB2 transcription. Exp Mol Med 58, 1158–1171 (2026). https://doi.org/10.1038/s12276-026-01677-4
Schlüsselwörter: Leberregeneration, Epigenetik, Suv39h1, HMGB2, Chaetocin