Clear Sky Science · it
Manipolazione genetica e farmacologica della metiltransferasi H3K9 Suv39h1 favorisce la rigenerazione epatica sbloccando la trascrizione di HMGB2
Perché è importante per la salute del fegato
I nostri fegati hanno una notevole capacità di ricrescere dopo un danno, ma in molti pazienti questo processo naturale di riparazione è troppo debole per prevenire l'insufficienza epatica. Questo studio pone una domanda semplice ma dalle grandi implicazioni: esiste un "freno" molecolare che frena la ricrescita epatica e, in tal caso, possiamo allentare quel freno in modo sicuro per aiutare i fegati danneggiati a recuperare?
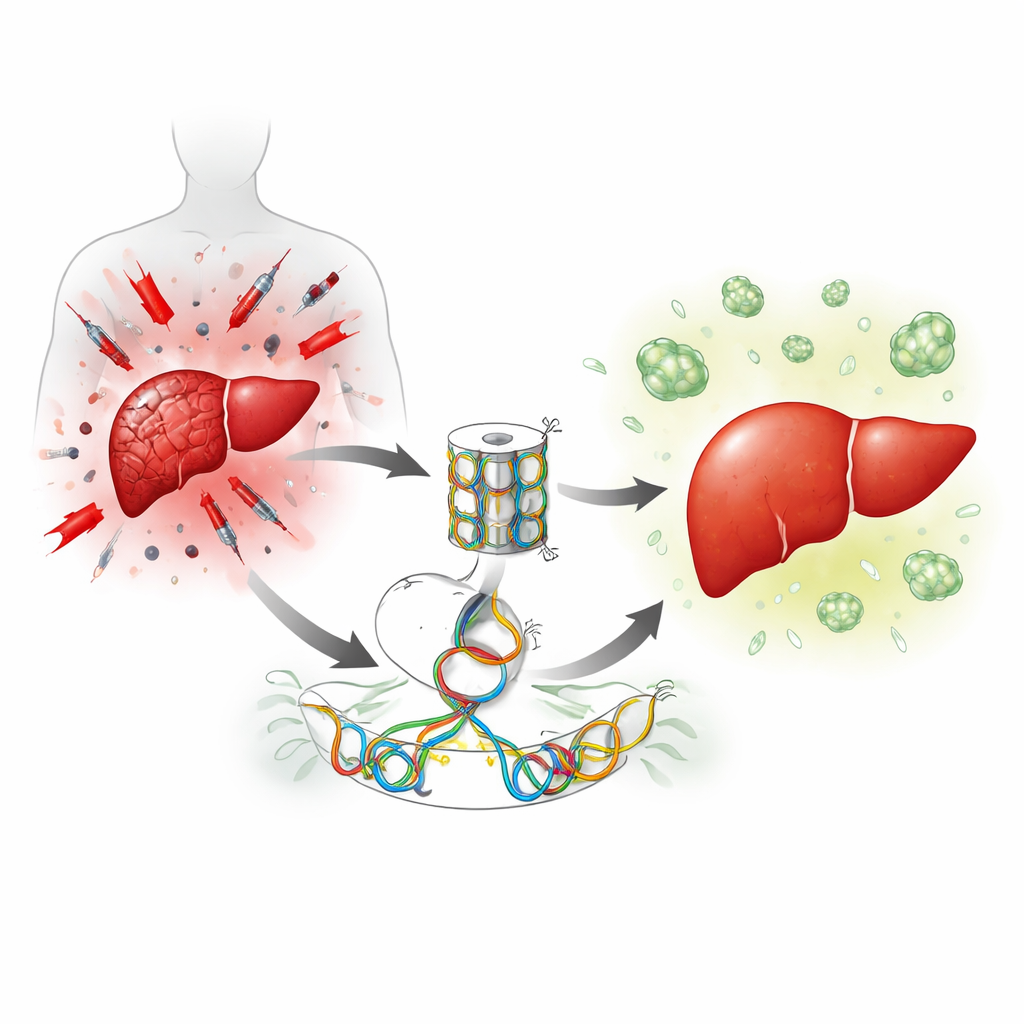
Un freno incorporato alla ricrescita epatica
Il fegato si ripara principalmente invitando le cellule epatiche in stato di quiescenza a ricominciare a dividersi. Gli autori si sono concentrati su un enzima chiamato Suv39h1 che contribuisce a mantenere i geni spenti compattando il modo in cui il DNA è impacchettato. Dopo un intervento chirurgico sul fegato nei topi, i livelli di Suv39h1 nelle cellule epatiche calano brevemente, sotto il controllo di un altro enzima che aggiunge marchi chimici al DNA. Questo ha suggerito che Suv39h1 possa normalmente agire come un freno sui geni necessari alla proliferazione delle cellule epatiche e che rilasciare questo freno potrebbe accelerare la rigenerazione.
Rimuovere il freno nei topi
Per testare l'idea, il gruppo ha usato topi in cui il gene Suv39h1 era stato eliminato o in tutto l'organismo o solo nelle cellule del fegato. In condizioni normali questi animali apparivano come i loro fratelli sani. Ma quando la maggior parte del fegato è stata asportata chirurgicamente o danneggiata con una tossina, i topi privi di Suv39h1 rigeneravano il tessuto epatico più rapidamente, presentavano più cellule epatiche in divisione e sopravvivevano meglio a interventi chirurgici gravi. Questi benefici si sono manifestati specificamente in assenza di Suv39h1, dato che la delezione del suo parente stretto Suv39h2 non migliorava il recupero epatico.
Un gene aiutante nascosto viene liberato
Analizzando quali geni venivano attivati o repressi nelle cellule epatiche in rigenerazione, i ricercatori hanno individuato un protagonista evidente: HMGB2, una proteina che aiuta a modellare il DNA e a controllare molti altri geni. Quando Suv39h1 era assente, i livelli di HMGB2 aumentavano fortemente in risposta ai segnali di crescita noti. Esperimenti aggiuntivi hanno mostrato che Suv39h1 si trova normalmente sulla regione di controllo di HMGB2 insieme a un marchio chimico associato al silenziamento genico. Quando Suv39h1 e questo marchio venivano rimossi, un altro fattore poteva legarsi e attivare HMGB2. Bloccare HMGB2 annullava il vantaggio proliferativo delle cellule epatiche carenti di Suv39h1, e abbassare HMGB2 nei topi rallentava la ricrescita epatica, dimostrando che HMGB2 è un aiutante cruciale una volta rilasciato il freno.
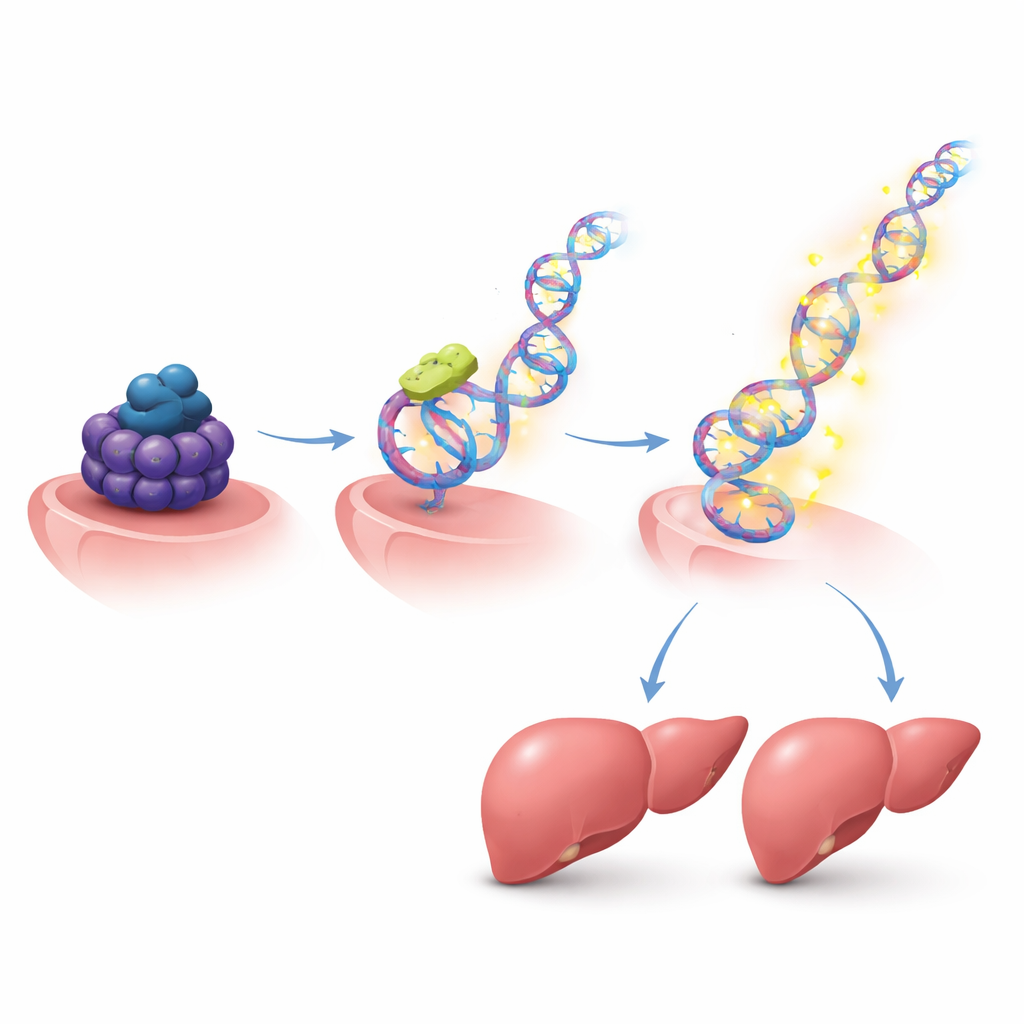
Riprogrammare i circuiti di crescita su molti geni
Poiché HMGB2 controlla a sua volta una vasta rete di geni, gli autori hanno mappato la sua attività nel genoma. Nelle cellule epatiche stimolate a dividersi, HMGB2 si concentrava sulle regioni di controllo di molti geni legati al ciclo cellulare e alla rigenerazione. Quando HMGB2 veniva ridotto, un ampio insieme di questi geni correlati alla crescita cambiava attività e le cellule epatiche si dividevano di meno. Tra i bersagli c'erano noti attori della riparazione epatica, inclusi molecole di segnalazione, recettori di superficie e fattori che guidano il ciclo cellulare. Ciò suggerisce che una volta che Suv39h1 permette l'aumento di HMGB2, HMGB2 a sua volta modula un intero programma pro-crescita.
Un indizio farmacologico e segni nei fegati umani
Il gruppo ha poi esplorato se un farmaco potesse indebolire temporaneamente Suv39h1. I topi trattati con la chaetocin, un composto che riduce il marchio chimico specifico creato da Suv39h1, mostravano una rigenerazione epatica più vigorosa, più cellule in divisione e una migliore sopravvivenza dopo ampie resezioni chirurgiche o danno da tossina. Infine, in campioni di fegato di persone con insufficienza epatica acuta, livelli più alti di SUV39H1 associavano a maggiore danno tissutale e a meno cellule in divisione, mentre livelli più alti di HMGB2 e di alcuni suoi geni partner correlavano con segni migliori di rigenerazione e con minor danno.
Cosa significa per i trattamenti futuri
In termini semplici, lo studio rivela una catena di controllo in cui Suv39h1 mantiene sotto stretta chiusura un potente aiuto alla crescita, HMGB2. Quando questa serratura viene allentata, HMGB2 può accendere molti geni che aiutano le cellule epatiche a moltiplicarsi e a sostituire il tessuto danneggiato. Mirare con attenzione a Suv39h1, probabilmente con farmaci più sicuri e precisi di quelli usati qui, potrebbe un giorno sostenere il recupero epatico in pazienti la cui capacità rigenerativa è insufficiente, sebbene rimanga molto lavoro prima che tale approccio possa essere testato in clinica.
Citazione: Lu, Y., Zhou, J., Miao, X. et al. Genetic and pharmaceutical manipulation of H3K9 methyltransferase Suv39h1 promotes liver regeneration by unleashing HMGB2 transcription. Exp Mol Med 58, 1158–1171 (2026). https://doi.org/10.1038/s12276-026-01677-4
Parole chiave: rigenerazione epatica, epigenetica, Suv39h1, HMGB2, chaetocin