Clear Sky Science · fr
La manipulation génétique et pharmacologique de la méthyltransférase H3K9 Suv39h1 favorise la régénération hépatique en libérant la transcription de HMGB2
Pourquoi cela compte pour la santé du foie
Nos foies ont une remarquable capacité à repousser après une blessure, mais chez de nombreux patients ce processus de réparation naturel est trop faible pour prévenir l'insuffisance hépatique. Cette étude pose une question simple aux grandes implications : existe-t-il un « frein » moléculaire qui limite la repousse du foie, et, le cas échéant, peut-on desserrer ce frein en toute sécurité pour aider les foies endommagés à récupérer ?
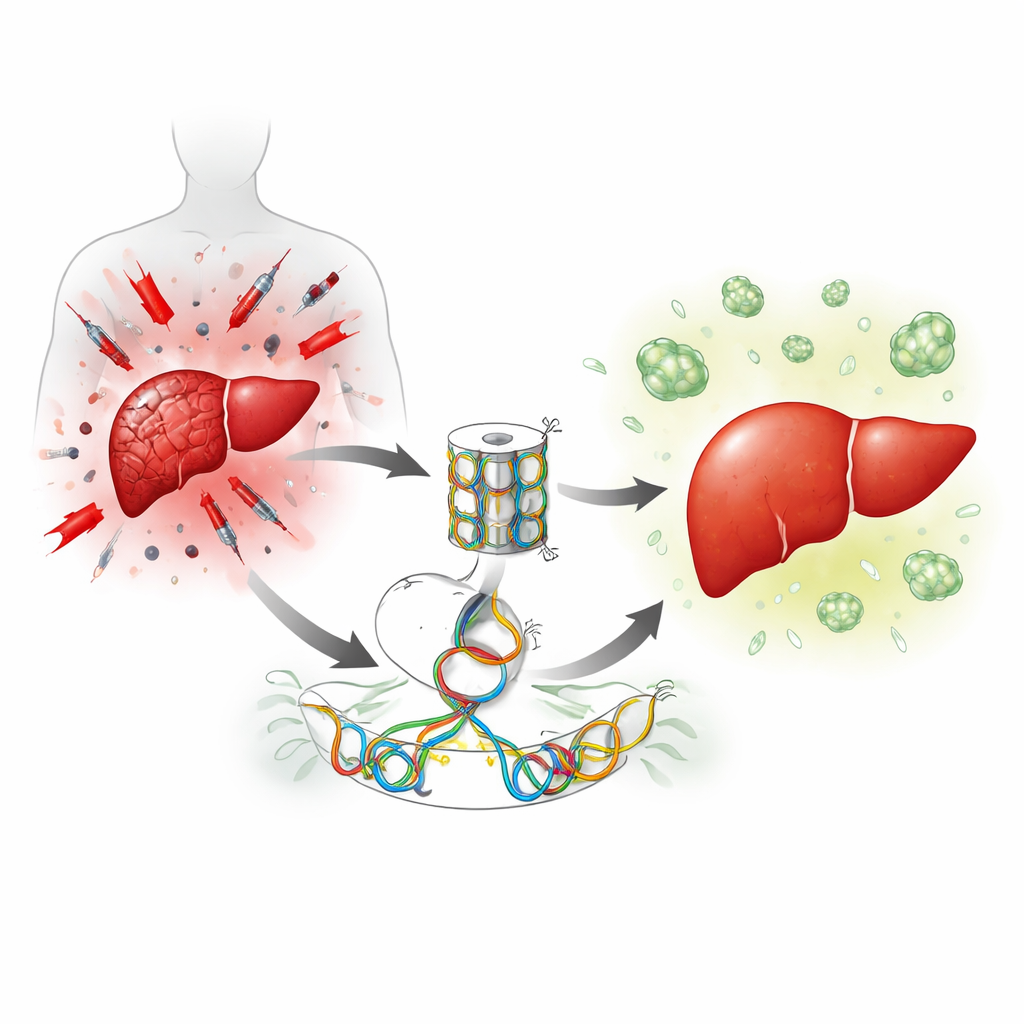
Un frein intégré à la repousse hépatique
Le foie se répare principalement en sollicitant des cellules hépatiques au repos pour qu'elles recommencent à se diviser. Les auteurs se sont intéressés à une enzyme appelée Suv39h1 qui aide à maintenir des gènes éteints en resserrant la façon dont l'ADN est empaqueté. Après une chirurgie du foie chez la souris, les niveaux de Suv39h1 dans les cellules hépatiques chutent brièvement, contrôlés par une autre enzyme qui ajoute des marques chimiques à l'ADN. Cela suggérait que Suv39h1 agit normalement comme un frein sur les gènes nécessaires à la prolifération des cellules hépatiques, et que relâcher ce frein pourrait accélérer la régénération.
Retirer le frein chez la souris
Pour tester cette idée, l'équipe a utilisé des souris dont le gène Suv39h1 avait été supprimé soit dans tout l'organisme, soit uniquement dans les cellules du foie. Dans des conditions normales, ces animaux ressemblaient à leurs congénères sains. Mais lorsque la majeure partie du foie était retirée chirurgicalement ou endommagée par une toxine, les souris dépourvues de Suv39h1 régénéraient le tissu hépatique plus rapidement, présentaient davantage de cellules hépatiques en division et survivaient mieux à une chirurgie lourde. Ces bénéfices semblaient spécifiques à la perte de Suv39h1, puisque la suppression de son homologue proche Suv39h2 n'améliorait pas la récupération hépatique.
Un gène assistant jusque-là caché est libéré
En examinant quels gènes s'activaient ou s'éteignaient dans les cellules hépatiques en régénération, les chercheurs ont identifié un acteur marquant : HMGB2, une protéine qui aide à façonner l'ADN et à contrôler de nombreux autres gènes. Lorsque Suv39h1 faisait défaut, les niveaux d'HMGB2 augmentaient fortement en réponse à des signaux de croissance connus. Des expériences supplémentaires ont montré que Suv39h1 se trouvait normalement sur la région de contrôle d'HMGB2, conjointement avec une marque chimique associée au silence génique. Quand Suv39h1 et cette marque étaient enlevés, un autre facteur pouvait se lier et activer HMGB2. Bloquer HMGB2 annulait l'avantage de croissance des cellules hépatiques déficientes en Suv39h1, et diminuer HMGB2 chez la souris ralentissait la repousse du foie, montrant qu'HMGB2 est un aide essentiel une fois le frein relâché.
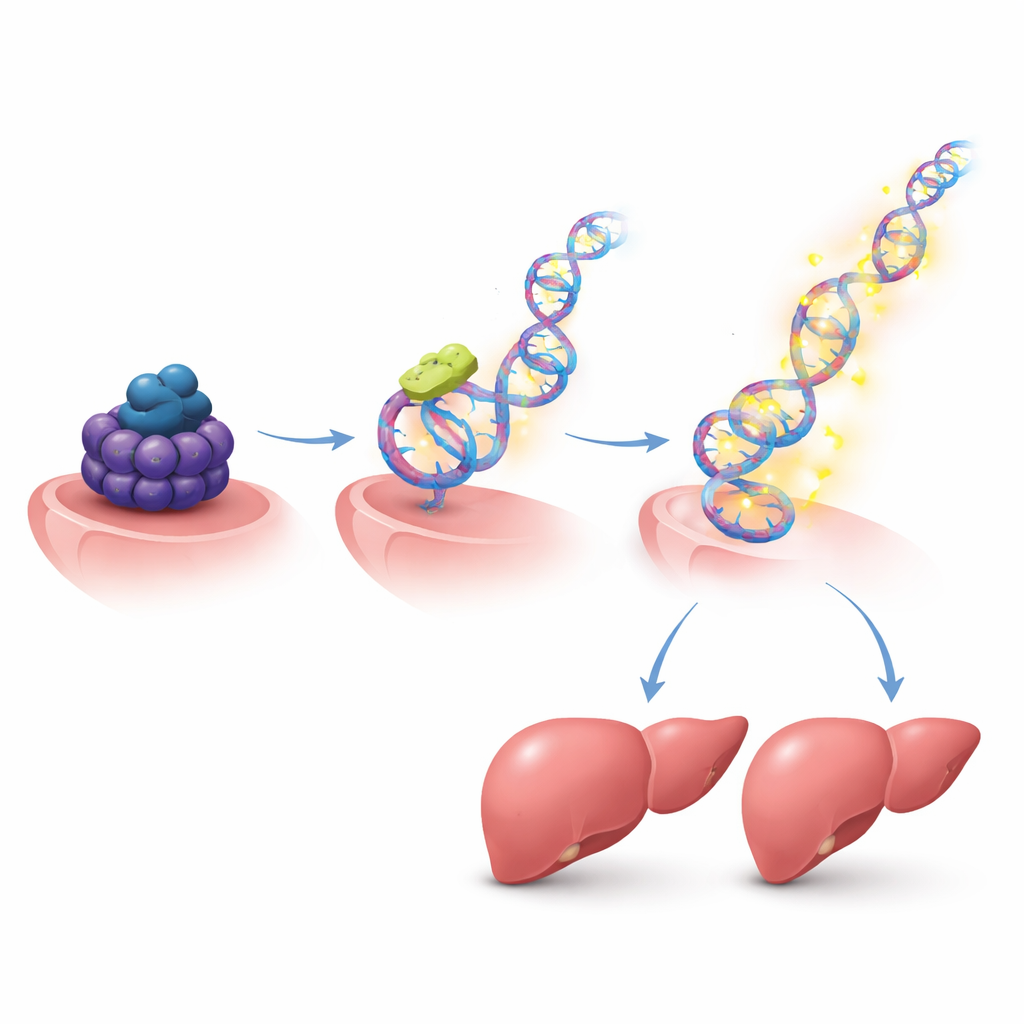
Reconfigurer les circuits de croissance sur de nombreux gènes
Parce qu'HMGB2 contrôle lui-même un large réseau de gènes, les auteurs ont cartographié son activité à l'échelle du génome. Dans des cellules hépatiques stimulées à se diviser, HMGB2 se rassemblait sur les régions de contrôle de nombreux gènes liés au cycle cellulaire et à la régénération. Lorsque HMGB2 était réduit, une grande partie de ces gènes associés à la croissance modifiaient leur activité, et les cellules hépatiques se divisaient moins. Parmi les cibles figuraient des acteurs bien connus de la réparation hépatique, y compris des molécules de signalisation, des récepteurs de surface et des facteurs qui pilotent le cycle cellulaire. Cela suggère qu'une fois que Suv39h1 permet l'élévation d'HMGB2, ce dernier règle à son tour tout un programme pro-croissance.
Un indice médicamenteux et des signes dans des foies humains
L'équipe a ensuite exploré si un médicament pouvait affaiblir temporairement Suv39h1. Des souris traitées par la chaetocin, un composé qui réduit la marque chimique spécifique créée par Suv39h1, ont montré une régénération hépatique plus forte, davantage de cellules en division et une meilleure survie après une chirurgie étendue ou une lésion toxique. Enfin, dans des échantillons de foie de personnes atteintes d'insuffisance hépatique aiguë, des niveaux plus élevés de SUV39H1 s'associaient à des lésions tissulaires plus importantes et à moins de cellules en division, tandis que des niveaux plus élevés d'HMGB2 et de plusieurs de ses gènes partenaires s'associaient à des signes de régénération meilleurs et à moins de dégâts.
Ce que cela signifie pour les traitements futurs
En termes simples, l'étude révèle une chaîne de contrôle dans laquelle Suv39h1 maintient sous clé un puissant assistant de croissance, HMGB2. Quand cette serrure est desserrée, HMGB2 peut activer de nombreux gènes qui aident les cellules hépatiques à se multiplier et à remplacer le tissu endommagé. Cibler soigneusement Suv39h1, probablement avec des médicaments plus sûrs et plus précis que ceux utilisés ici, pourrait un jour soutenir la récupération hépatique chez des patients dont le pouvoir régénératif est insuffisant, bien que beaucoup de travail reste à faire avant qu'une telle approche puisse être testée en clinique.
Citation: Lu, Y., Zhou, J., Miao, X. et al. Genetic and pharmaceutical manipulation of H3K9 methyltransferase Suv39h1 promotes liver regeneration by unleashing HMGB2 transcription. Exp Mol Med 58, 1158–1171 (2026). https://doi.org/10.1038/s12276-026-01677-4
Mots-clés: régénération hépatique, épigénétique, Suv39h1, HMGB2, chaetocin