Clear Sky Science · zh
内侧背侧前额叶皮层Microglia CR3介导的突触修剪促进通过谷氨能功能障碍产生和维持慢性肌肉疼痛
为何酸痛的肌肉会持续数月
我们大多数人都认为肌肉酸痛在休息几天后会消退。但对许多人来说,肌肉疼痛会成为持续数月的顽固伴侣,常伴随焦虑或情绪低落。本研究在大鼠中展开,视角超越了受伤的肌肉本身,转向大脑,探讨为何慢性肌肉痛会如此持久且令人情绪消耗。研究人员发现了一个令人意外的罪魁祸首:大脑中的微小免疫细胞,它们悄然重塑皮层中与疼痛相关区域的神经连接。
从短暂的疼痛到长期的痛苦
研究组首先建立了一个成熟的大鼠慢性肌肉痛模型,通过向小腿肌肉注射少量盐溶液诱发疼痛。起初,动物对触觉和热刺激反应强烈,这与受伤后的预期一致。但数周后,即使原始刺激本该消退,它们的疼痛敏感性仍然很高,活动减少并回避开放场中心——这些都是类焦虑行为的表现。脑成像和细胞标志物显示,名为背内侧前额叶皮层(dmPFC)的区域活动减少,该区域已知参与我们对疼痛的感受和反应的调控。
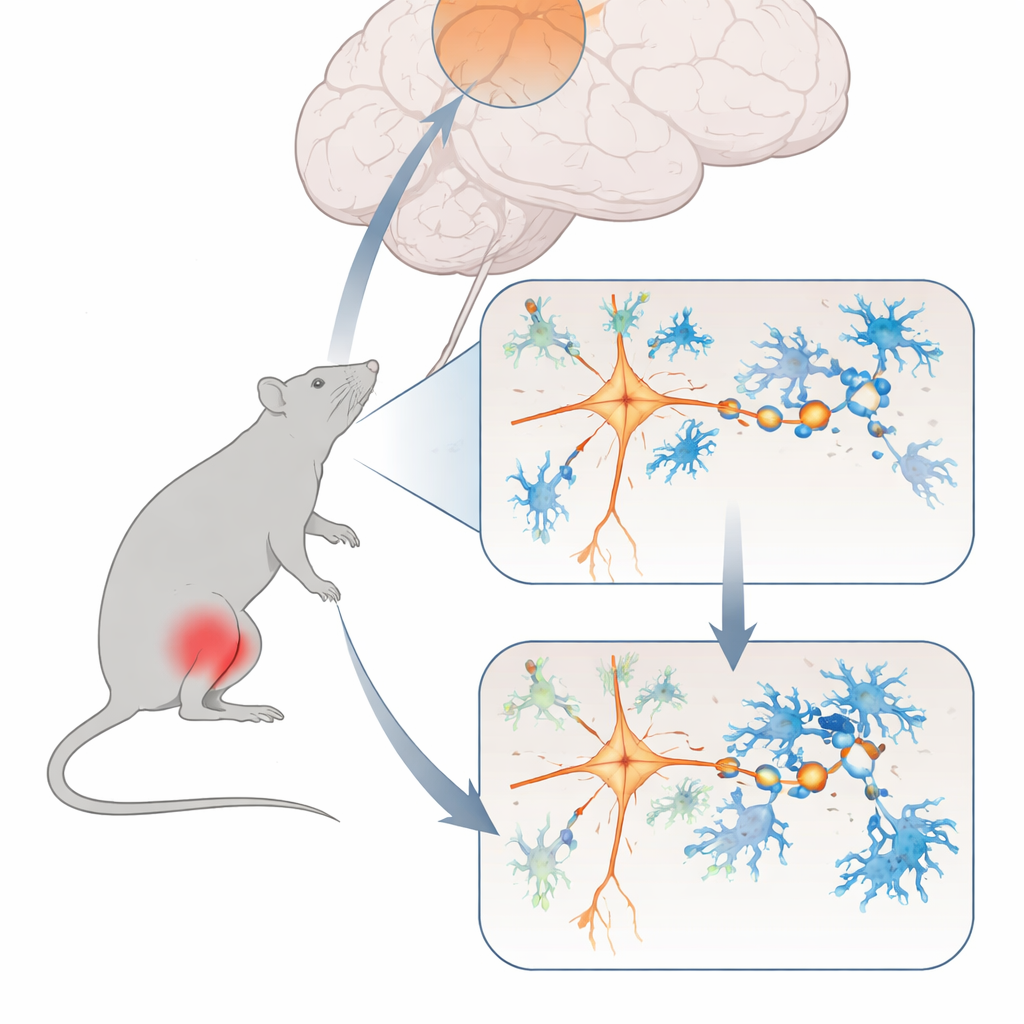
被压抑的疼痛控制中枢
为检验该脑区是否真正参与控制慢性肌肉疼痛,研究人员使用光遗传和化学遗传学工具像调光开关一样上调或下调该区的兴奋性神经元。当他们增强这些细胞的活动时,大鼠的机械痛敏降低,类焦虑行为减少;反之,抑制相同神经元即便在健康动物中也会诱发类似慢性疼痛的行为,同时脊髓中传递疼痛信号的中继区变得过度活跃。细致的电生理记录显示,在慢性疼痛状态下,受累皮层神经元放电减少,其兴奋性突触——在神经元之间传递信号的微小接触点——变得更弱且数量减少。
吞噬突触的大脑免疫细胞
是什么导致了这些健康连接的丧失?研究者关注了小胶质细胞——大脑的常驻免疫细胞,它们如同园丁般在发育和疾病中修剪突触。通过单细胞RNA测序,他们发现疼痛相关皮层中的小胶质细胞转向一种强烈促炎的状态,并在与突触修剪相关的基因上表现出高活性。其中一个分子——称为CR3的受体——在联结去除突触的通路中特别突出。显微镜与流式细胞术实验显示,随着疼痛进入慢性阶段,小胶质细胞增殖、聚集于活跃神经元周围,并越来越多地吞噬兴奋性突触的片段,而抑制性连接在很大程度上幸免。
阻断修剪即可恢复脑功能
为验证这些小胶质细胞是否真正驱动慢性疼痛,团队通过输注到脑脊液中的药物短暂抑制了它们。沉默小胶质细胞减轻了疼痛行为,恢复了皮层神经元对疼痛刺激的反应,并逆转了突触的结构性损伤。更进一步,科学家们采用靶向病毒方法特异性降低小胶质细胞中的CR3表达。这抑制了它们吞噬突触的行为,增加了兴奋性突触的数量与强度,并使皮层神经元重新变得更易兴奋。CR3减少的小胶质细胞大鼠表现出更高的疼痛阈值并更愿意探索,表明疼痛和焦虑均有所缓解。当研究者随后人为抑制相同的兴奋性神经元时,这些益处消失,证实了缓解依赖于恢复这些细胞的活动。
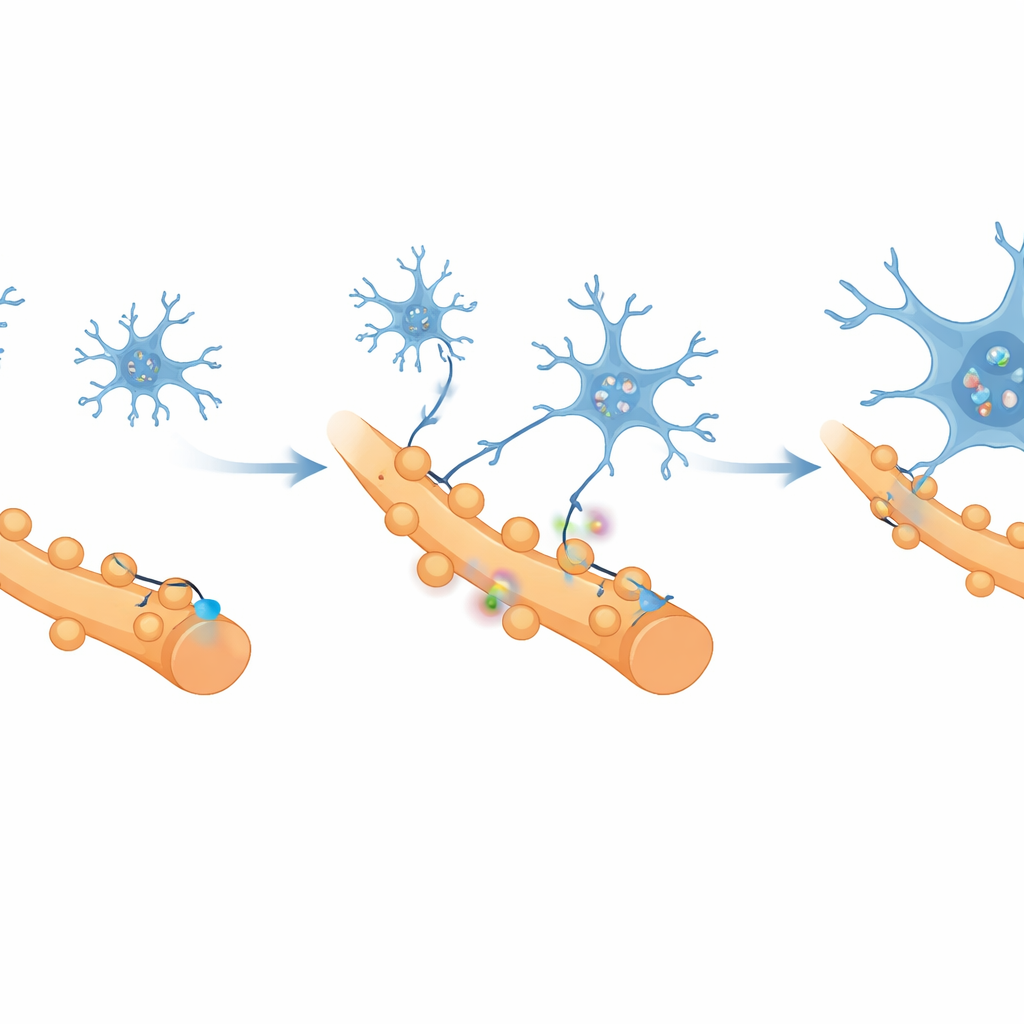
对慢性肌肉疼痛患者的意义
总体而言,这项工作描绘了这样一个图景:持续的肌肉疼痛不仅由身体持续的信号维持,还由经重塑的大脑回路维持。在该模型中,位于关键前额叶区域的小胶质细胞过度活跃,通过CR3依赖的修剪移除兴奋性突触,使该区域功能受损,降低了其抑制疼痛和焦虑的能力。通过阻断小胶质细胞或其CR3受体,研究人员能够逆转这些脑内变化并缓解大鼠的症状。尽管还需更多研究将这些发现转化为人类疗法,但结果提示未来治疗慢性肌肉疼痛的策略可能来自于平息或精细重塑大脑自身免疫细胞的活动,而非仅针对神经或肌肉本身。
引用: Luo, M., Wang, L., Liang, Y. et al. Microglial CR3-mediated synaptic pruning in the dmPFC promotes the generation and maintenance of chronic muscle pain via glutamatergic dysfunction. Exp Mol Med 58, 664–680 (2026). https://doi.org/10.1038/s12276-026-01666-7
关键词: 慢性肌肉疼痛, 小胶质细胞, 突触修剪, 前额叶皮层, 神经炎症