Clear Sky Science · es
La poda sináptica mediada por CR3 en microglía en la dmPFC promueve la generación y el mantenimiento del dolor muscular crónico mediante disfunción glutamatérgica
Por qué las agujetas pueden persistir durante meses
La mayoría esperamos que las molestias musculares desaparezcan tras unos días de reposo. Sin embargo, para muchas personas el dolor muscular se convierte en un compañero persistente que dura meses y con frecuencia se asocia a ansiedad o ánimo bajo. Este estudio en ratas mira más allá del músculo dolorido y se adentra en el cerebro para preguntar por qué el dolor muscular crónico puede volverse tan persistente y emocionalmente agotador. Los investigadores descubren un culpable sorprendente: diminutas células inmunitarias en el cerebro que silenciosamente remodelan las conexiones nerviosas en una región cortical relacionada con el dolor.
De una molestia breve a un dolor duradero
El equipo comenzó creando un modelo bien establecido de dolor muscular crónico en ratas, provocado por una pequeña inyección de solución salina en un músculo de la pantorrilla. Al principio, los animales reaccionaron con fuerza al tacto y al calor, como es de esperar tras una lesión. Pero incluso semanas después, cuando la irritación original debería haberse resuelto, su sensibilidad al dolor seguía elevada y se movían menos y evitaban el centro de un campo abierto —signos de un comportamiento similar a la ansiedad. Escáneres cerebrales y marcadores celulares apuntaron a una actividad reducida en una región llamada corteza prefrontal dorsomedial, un área conocida por modelar cómo sentimos y reaccionamos al dolor.
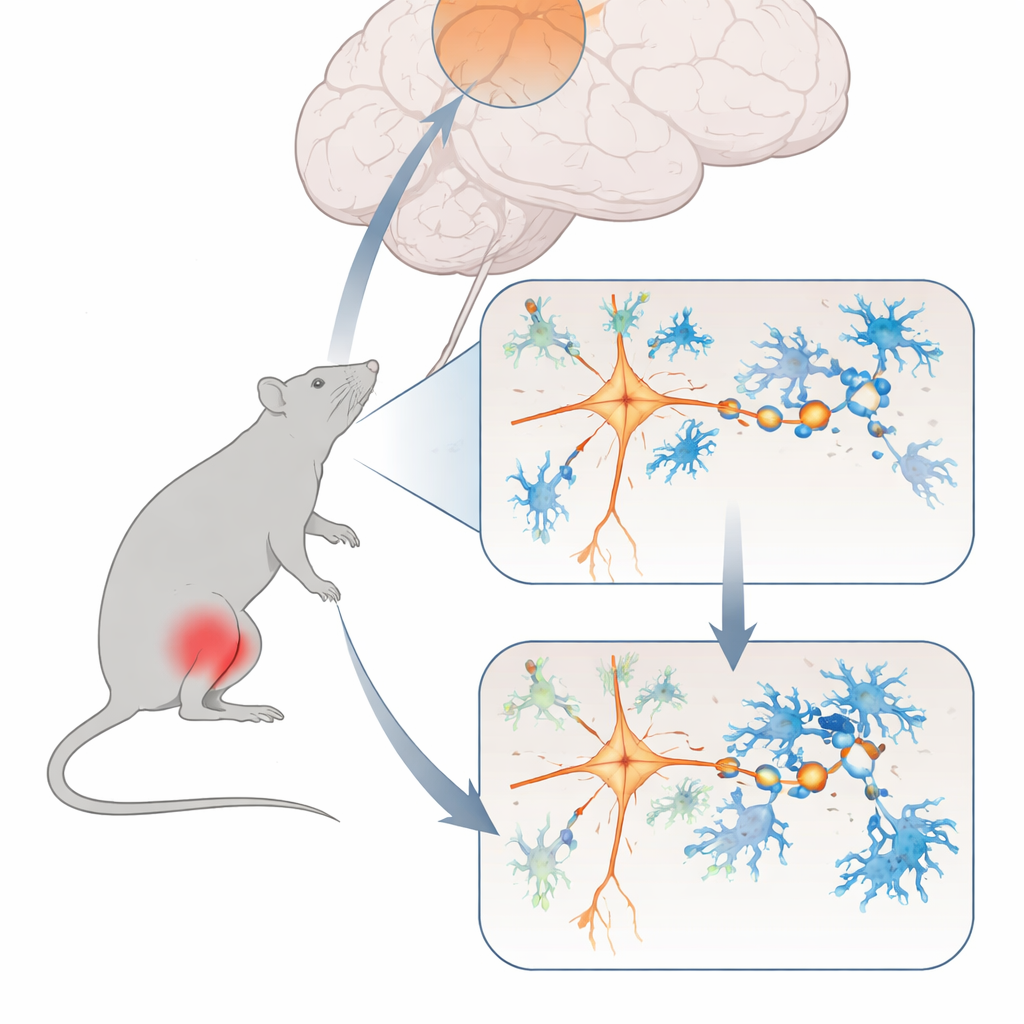
Un centro de control del dolor en el cerebro silenciado
Para comprobar si esta región cerebral realmente ayuda a controlar el dolor muscular crónico, los investigadores utilizaron herramientas genéticas basadas en luz y fármacos para aumentar o disminuir la actividad de sus neuronas excitadoras, como un regulador de intensidad. Cuando aumentaron la actividad de estas células, las ratas se volvieron menos sensibles al dolor mecánico y mostraron menos comportamientos similares a la ansiedad. Al inhibir las mismas neuronas, incluso animales sanos empezaron a comportarse más como quienes sufren dolor crónico, y una área de relevo en la médula espinal que transmite señales de dolor se volvió hiperactiva. Registros eléctricos detallados revelaron que, en el dolor crónico, las neuronas corticales afectadas disparaban menos y sus sinapsis excitadoras —pequeños puntos de contacto que transmiten señales entre neuronas— se debilitaban y disminuían en número.
Células inmunitarias cerebrales que devoran sinapsis
¿Qué causa esta pérdida de conexiones sanas? Los investigadores se fijaron en la microglía, las células inmunitarias residentes del cerebro, que actúan como jardineros que recortan sinapsis durante el desarrollo y en la enfermedad. Usando secuenciación de ARN a nivel de célula única, encontraron que la microglía en la corteza relacionada con el dolor cambiaba a un estado fuertemente proinflamatorio, mostrando alta actividad en genes vinculados a la poda sináptica. Una molécula, un receptor llamado CR3, destacó por su estrecha relación con las vías que eliminan sinapsis. Experimentos de microscopía y citometría de flujo mostraron que, a medida que el dolor se volvía crónico, la microglía se multiplicaba, se agrupaba alrededor de neuronas activas y cada vez engullía más fragmentos de sinapsis excitadoras, mientras que las conexiones inhibitorias quedaban mayormente preservadas.
Bloquear la poda rescata la función cerebral
Para ver si estas microglías eran realmente las responsables del dolor crónico, el equipo las suprimió temporalmente con un fármaco administrado en el líquido cerebral. Silenciar la microglía redujo los comportamientos de dolor, restauró las respuestas de las neuronas corticales a estímulos dolorosos y revirtió el daño estructural en las sinapsis. Yendo un paso más allá, los científicos emplearon un enfoque viral dirigido para reducir específicamente CR3 en la microglía. Esto redujo su conducta de devorar sinapsis, aumentó el número y la fuerza de las sinapsis excitadoras y volvió a hacer a las neuronas corticales más excitables. Las ratas con microglía con CR3 reducido mostraron umbrales de dolor más altos y exploraron más, lo que sugiere que tanto el dolor como la ansiedad habían mejorado. Cuando los investigadores luego silenciaron artificialmente esas mismas neuronas excitadoras, los beneficios desaparecieron, confirmando que el alivio depende de restaurar la actividad de estas células.
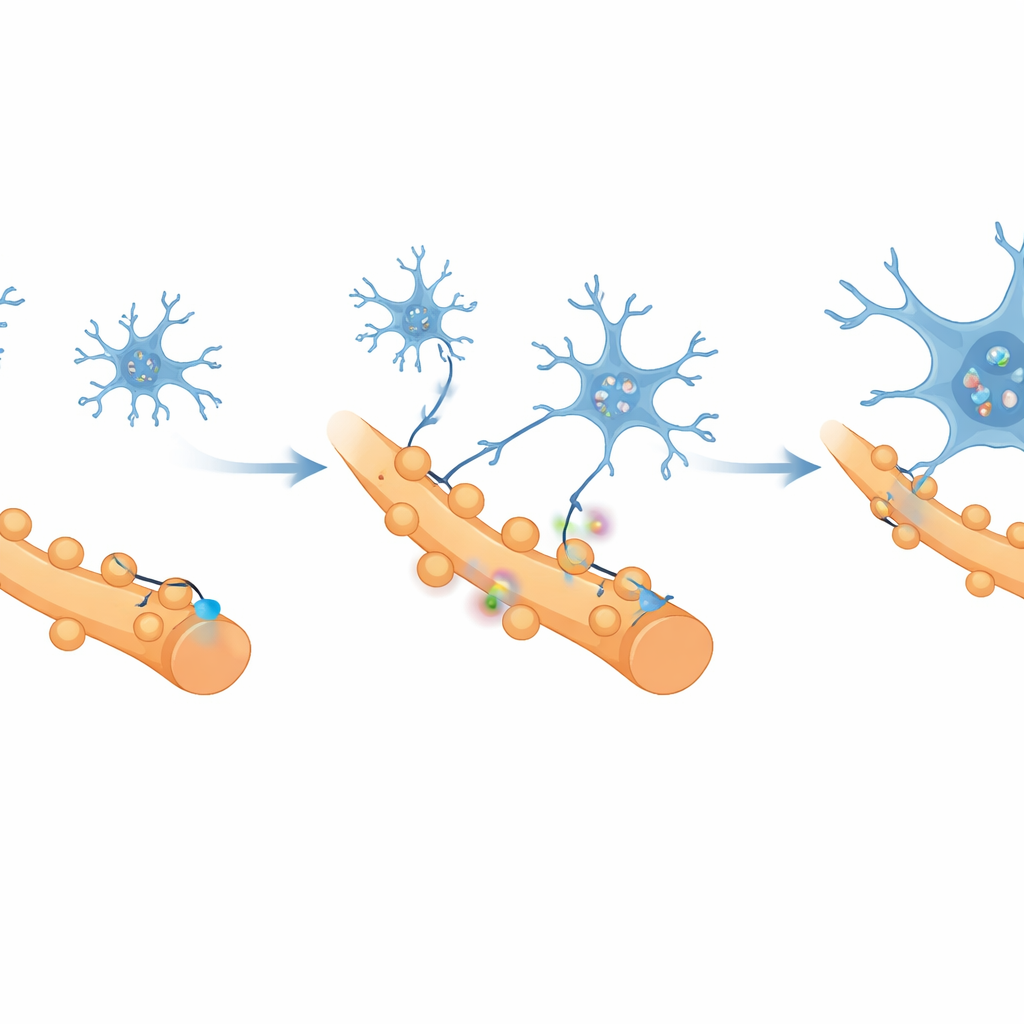
Qué significa esto para las personas con dolor muscular crónico
En conjunto, el trabajo dibuja un panorama en el que el dolor muscular persistente se mantiene no solo por señales continuas del cuerpo, sino por un circuito cerebral remodelado. En este modelo, la microglía hiperactiva en una zona prefrontal clave elimina sinapsis excitadoras mediante una poda dependiente de CR3, dejando la región debilitada y menos capaz de moderar el dolor y la ansiedad. Al bloquear la microglía o su receptor CR3, los investigadores pudieron revertir estos cambios cerebrales y aliviar los síntomas en ratas. Si bien hacen falta más estudios para trasladar esto a los humanos, los hallazgos sugieren que futuros tratamientos para el dolor muscular crónico podrían provenir de calmar, o reentrenar cuidadosamente, las propias células inmunitarias del cerebro en lugar de centrarse solo en los nervios o los músculos.
Cita: Luo, M., Wang, L., Liang, Y. et al. Microglial CR3-mediated synaptic pruning in the dmPFC promotes the generation and maintenance of chronic muscle pain via glutamatergic dysfunction. Exp Mol Med 58, 664–680 (2026). https://doi.org/10.1038/s12276-026-01666-7
Palabras clave: dolor muscular crónico, microglía, poda sináptica, corteza prefrontal, neuroinflamación