Clear Sky Science · it
La potatura sinaptica mediata da CR3 delle microglia nel dmPFC promuove la generazione e il mantenimento del dolore muscolare cronico tramite disfunzione glutamatergica
Perché i dolori muscolari possono protrarsi per mesi
La maggior parte di noi si aspetta che i dolori muscolari si attenuino dopo qualche giorno di riposo. Eppure per molte persone il dolore muscolare diventa un compagno ostinato che dura mesi ed è spesso associato ad ansia o tono dell’umore basso. Questo studio sui ratti guarda oltre il muscolo dolorante e nel cervello, chiedendosi perché il dolore muscolare cronico possa diventare così persistente e emotivamente logorante. I ricercatori individuano un colpevole sorprendente: piccole cellule immunitarie nel cervello che rimodellano silenziosamente le connessioni neuronali in una regione corticale legata al dolore.
Da un dolore passeggero a un dolore duraturo
Il gruppo ha iniziato creando un modello consolidato di dolore muscolare cronico nei ratti, indotto da una piccola iniezione di soluzione salina in un muscolo del polpaccio. All’inizio gli animali reagivano fortemente al tocco e al calore, come ci si aspetta dopo un trauma. Ma anche settimane dopo, quando l’irritazione originale avrebbe dovuto risolversi, la loro sensibilità al dolore rimaneva elevata e si muovevano meno evitando il centro di un’arena aperta — segni di comportamento simile all’ansia. Le scansioni cerebrali e i marcatori cellulari indicavano una ridotta attività in una regione chiamata corteccia prefrontale dorsomediale, un’area nota per modulare come percepiamo e reagiamo al dolore.
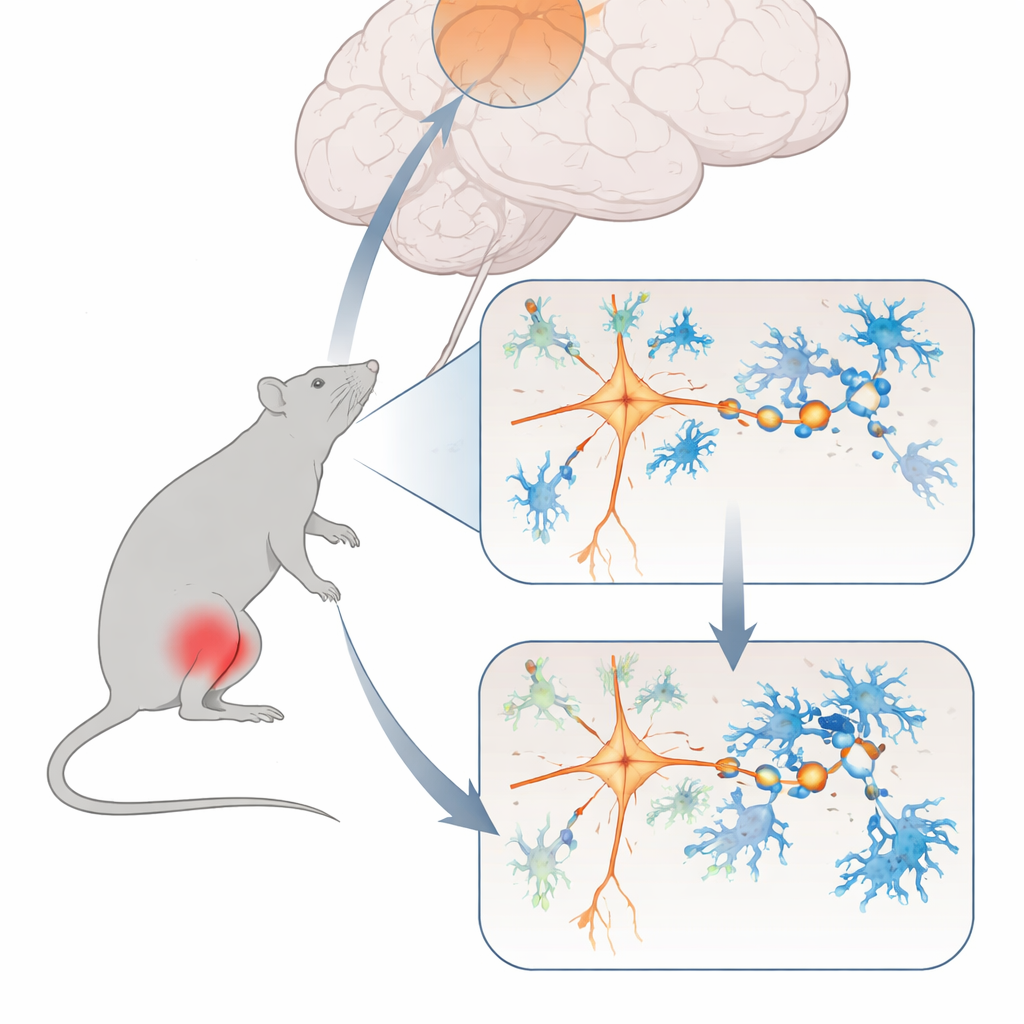
Un hub di controllo del dolore silenziato
Per verificare se questa regione cerebrale contribuiva effettivamente a controllare il dolore muscolare cronico, i ricercatori usarono strumenti genetici a base di luce e di farmaci per modulare le cellule nervose eccitatorie come un dimmer. Quando aumentarono l’attività di queste cellule, i ratti divennero meno sensibili al dolore meccanico e mostrarono comportamenti meno simili all’ansia. Quando invece attenuarono le stesse cellule, anche animali sani cominciarono a comportarsi più come soggetti con dolore cronico, e un’area di relay del midollo spinale che trasmette segnali di dolore risultò iperattiva. Registrazioni elettriche dettagliate rivelarono che, nel dolore cronico, i neuroni corticali interessati sparavano meno e le loro sinapsi eccitatorie — minuscoli punti di contatto che trasmettono segnali tra neuroni — diventavano più deboli e meno numerose.
Cellule immunitarie cerebrali che “mangiano” le sinapsi
Cosa causa questa perdita di connessioni sane? Gli investigatori si sono concentrati sulle microglia, le cellule immunitarie residenti del cervello, che agiscono come giardinieri che potano le sinapsi durante lo sviluppo e in condizioni patologiche. Utilizzando il sequenziamento dell’RNA a singola cellula, hanno scoperto che le microglia nella corteccia legata al dolore passavano a uno stato fortemente pro‑infiammatorio, con alta espressione di geni collegati alla potatura sinaptica. Una molecola, un recettore chiamato CR3, risaltava come strettamente associata alle vie che rimuovono le sinapsi. Esperimenti di microscopia e citometria a flusso mostrarono che, con la cronicizzazione del dolore, le microglia si moltiplicavano, si raccoglievano attorno ai neuroni attivi e inglobavano sempre più frammenti di sinapsi eccitatorie, mentre le connessioni inibitorie erano per lo più risparmiate.
Bloccare la potatura ripristina la funzione cerebrale
Per capire se queste microglia fossero effettivamente i driver del dolore cronico, il gruppo le ha temporaneamente soppresse con un farmaco somministrato nel fluido cerebrale. Silenziare le microglia ridusse i comportamenti legati al dolore, ripristinò le risposte dei neuroni corticali agli stimoli dolorosi e invertì i danni strutturali alle sinapsi. Facendo un passo ulteriore, gli scienziati usarono un approccio virale mirato per ridurre specificamente CR3 nelle microglia. Questo ridusse il loro comportamento di “mangiare” le sinapsi, aumentò il numero e la forza delle sinapsi eccitatorie e rese nuovamente più eccitabili i neuroni corticali. I ratti con microglia private di CR3 mostrarono soglie di dolore più alte e maggiore propensione all’esplorazione, suggerendo che sia il dolore sia l’ansia si erano attenuati. Quando i ricercatori poi sopressero artificialmente le stesse cellule eccitatorie, i benefici scomparvero, confermando che il sollievo dipende dal ripristino dell’attività di queste cellule.
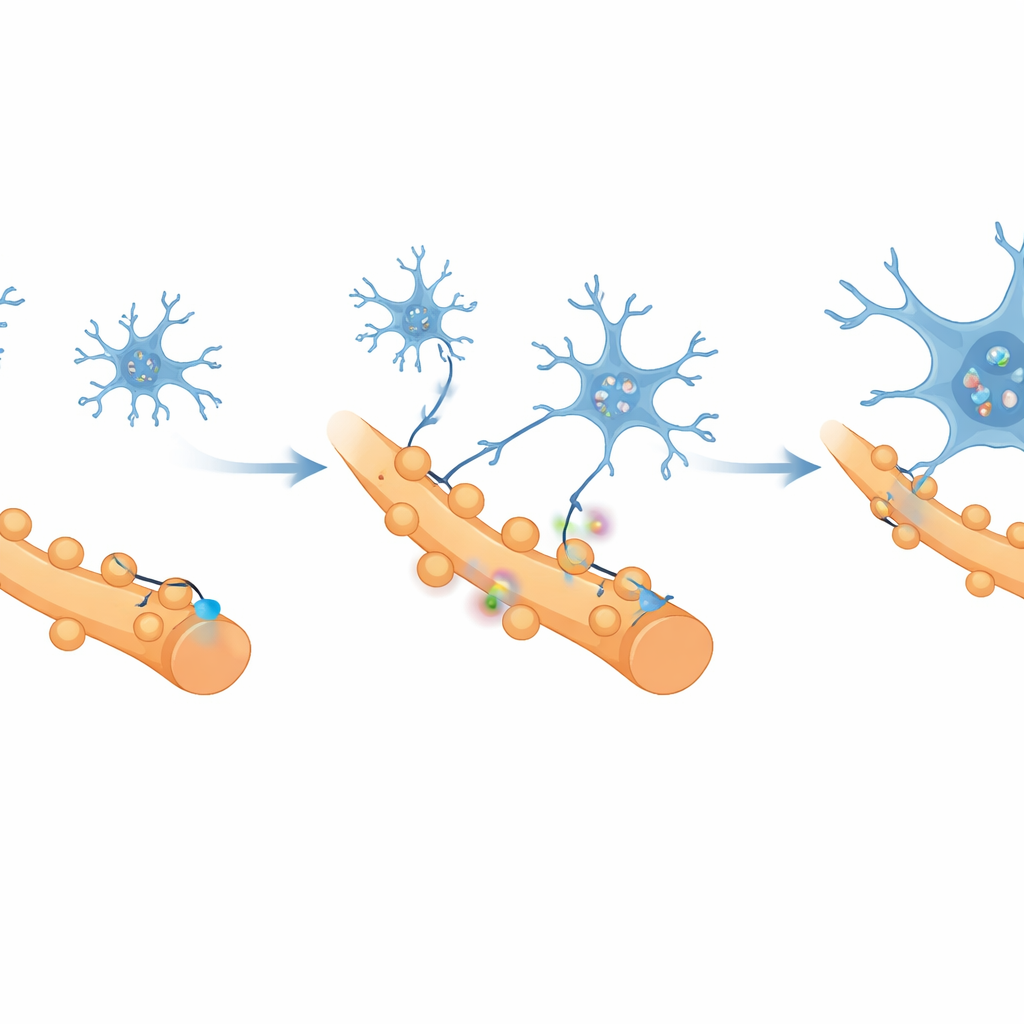
Cosa significa per le persone con dolore muscolare cronico
Nel complesso, il lavoro dipinge un quadro in cui il dolore muscolare persistente è mantenuto non solo da segnali corporei continui ma da un circuito cerebrale rimodellato. In questo modello, microglia iperattive in una zona prefrontale chiave spogliano le sinapsi eccitatorie tramite una potatura dipendente da CR3, lasciando la regione sottodimensionata e meno capace di attenuare dolore e ansia. Bloccando le microglia o il loro recettore CR3, i ricercatori sono riusciti a invertire questi cambiamenti cerebrali e alleviare i sintomi nei ratti. Sebbene siano necessari ulteriori studi per tradurre questi risultati nell’uomo, i risultati suggeriscono che trattamenti futuri per il dolore muscolare cronico potrebbero derivare dal calmare, o dal rieducare con attenzione, le cellule immunitarie del cervello piuttosto che mirare soltanto a nervi o muscoli.
Citazione: Luo, M., Wang, L., Liang, Y. et al. Microglial CR3-mediated synaptic pruning in the dmPFC promotes the generation and maintenance of chronic muscle pain via glutamatergic dysfunction. Exp Mol Med 58, 664–680 (2026). https://doi.org/10.1038/s12276-026-01666-7
Parole chiave: dolore muscolare cronico, microglia, potatura sinaptica, Corteccia prefrontale, neuroinfiammazione