Clear Sky Science · nl
Microgliale CR3-gemedieerde synaptische snoei in de dmPFC bevordert het ontstaan en behoud van chronische spierpijn via glutamaterge disfunctie
Waarom spierpijn maanden kan aanhouden
De meesten van ons verwachten dat spierpijn na een paar dagen rust verdwijnt. Voor veel mensen wordt spierpijn echter een hardnekkige metgezel die maanden blijft bestaan en vaak samengaat met angst of sombere stemming. Deze studie bij ratten kijkt voorbij de pijnlijke spier zelf en richt zich op de hersenen om te achterhalen waarom chronische spierpijn zo persistent en emotioneel uitputtend kan worden. De onderzoekers onthullen een verrassende dader: kleine immuuncellen in de hersenen die stilletjes zenuwverbindingen herschikken in een voor pijn relevante corticale regio.
Van kortstondige pijn naar langdurig lijden
Het team begon met het opzetten van een goedgekeurd model van chronische spierpijn bij ratten, veroorzaakt door een kleine injectie van een zoutoplossing in een kuitspier. In eerste instantie reageerden de dieren sterk op aanraking en warmte, zoals verwacht na weefselirritatie. Maar zelfs weken later, wanneer de oorspronkelijke irritatie voorbij had moeten zijn, bleef hun pijngevoeligheid hoog en bewogen ze minder en vermeden ze het midden van een open arena — tekenen van angstachtig gedrag. Hersenscans en cellulaire markers wezen op verminderde activiteit in een gebied dat dorsomediale prefrontale cortex heet, een regio die bekendstaat om zijn rol bij hoe we pijn ervaren en erop reageren.
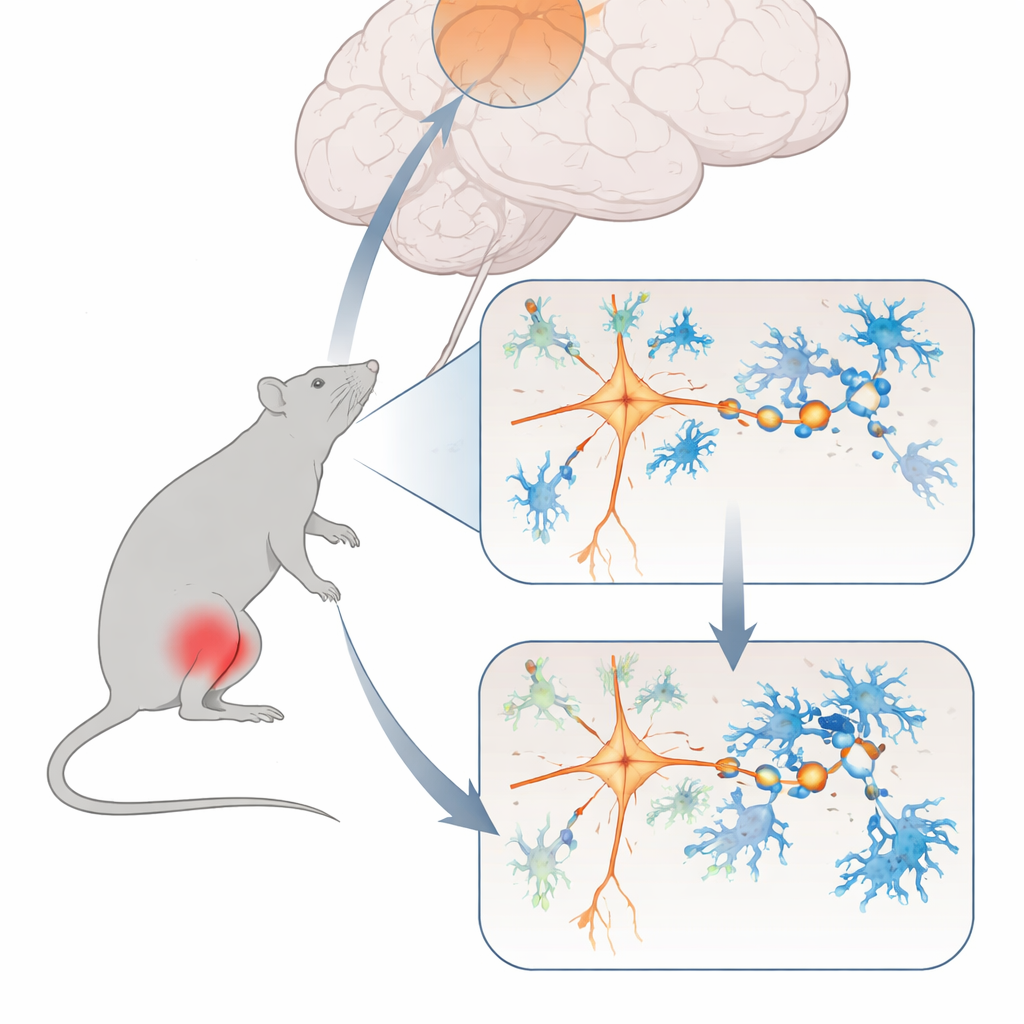
Een verzwakte pijnregelende hub in de hersenen
Om te testen of deze hersenregio daadwerkelijk helpt chronische spierpijn te beheersen, gebruikten de onderzoekers optische en farmacologische genetische middelen om de excitatoire neuronen daarin omhoog of omlaag te regelen als een dimmerschakelaar. Toen ze de activiteit van deze cellen verhoogden, werden de ratten minder gevoelig voor mechanische pijn en toonden ze minder angstachtig gedrag. Wanneer ze dezelfde cellen dempten, begonnen zelfs gezonde dieren zich meer als chronische pijnpatiënten te gedragen en raakte een relaisgebied in het ruggenmerg dat pijnsignalen doorgeeft overactief. Gedetailleerde elektrische opnames toonden aan dat bij chronische pijn de getroffen corticale neuronen minder vuurden en hun excitatoire synapsen — kleine contactpunten die signalen tussen zenuwcellen doorgeven — zwakker en minder talrijk werden.
Hersenimmuuncellen die synapsen ‘opeten’
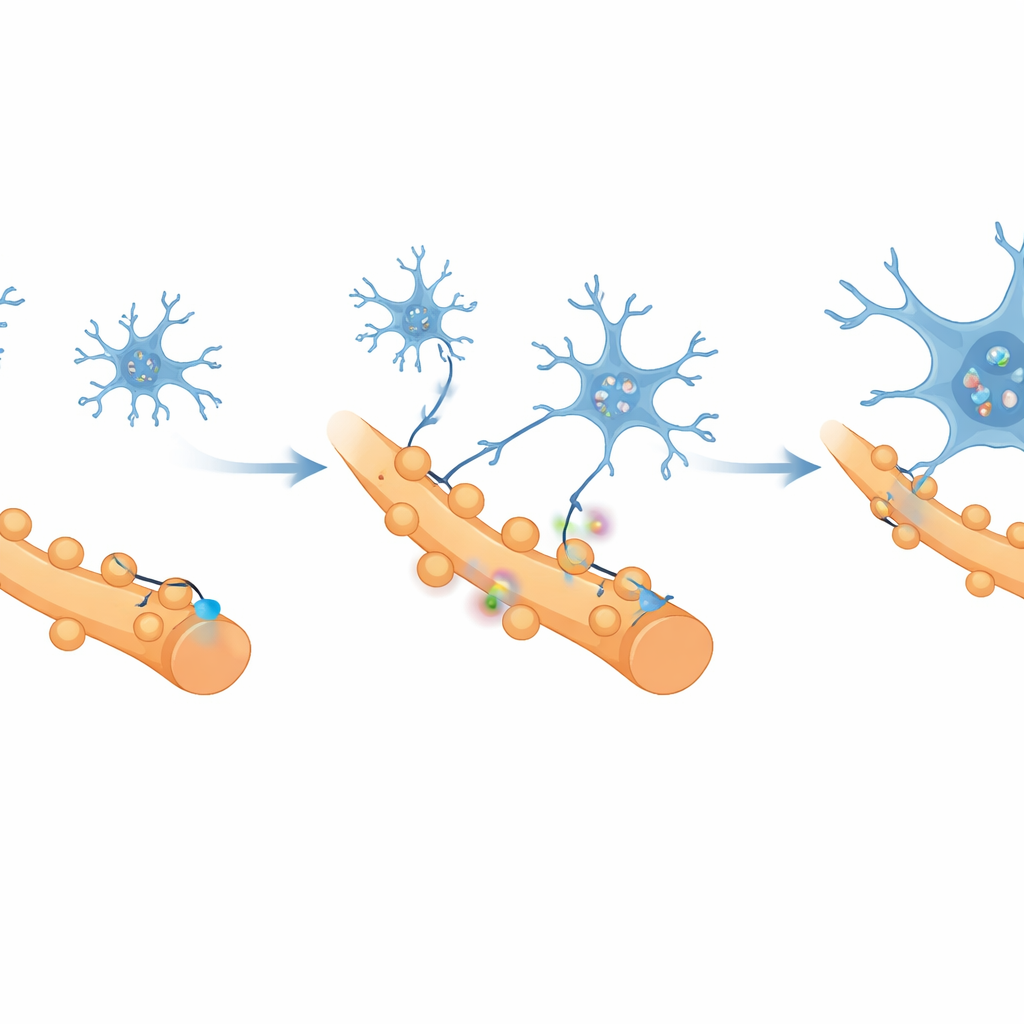
Wat veroorzaakt dit verlies van gezonde verbindingen? De onderzoekers zochten naar microglia, de residentiële immuuncellen van de hersenen, die fungeren als tuinmannen die synapsen snoeien tijdens ontwikkeling en ziekte. Met single-cell RNA-sequencing ontdekten ze dat microglia in de pijngerelateerde cortex overgingen in een sterk pro-inflammatoire staat, met hoge activiteit in genen die verbonden zijn met synaptische snoei. Eén molecuul, een receptor die CR3 heet, viel op omdat het nauw gekoppeld was aan pathways die synapsen verwijderen. Microscopen en flowcytometrie-experimenten toonden aan dat, naarmate pijn chronisch werd, microglia vermenigvuldigden, zich ophoopten rond actieve neuronen en steeds vaker stukjes van excitatoire synapsen insloten, terwijl inhibitorische verbindingen grotendeels gespaard bleven.
Het blokkeren van snoei herstelt hersenfunctie
Om te zien of deze microglia daadwerkelijk chronische pijn aandrijven, onderdrukte het team ze tijdelijk met een medicijn dat in het hersenvocht werd toegediend. Het stilleggen van microglia verminderde pijnachtig gedrag, herstelde de reactie van corticale neuronen op pijnlijke prikkels en keerde structurele schade aan synapsen om. Verder gebruikten de wetenschappers een gerichte virale aanpak om CR3 specifiek in microglia te verminderen. Dit verminderde hun synaps-etend gedrag, verhoogde het aantal en de sterkte van excitatoire synapsen en maakte corticale neuronen opnieuw prikkelbaarder. Ratten met verminderde CR3 in microglia vertoonden hogere pijndrempels en waren meer bereid te verkennen, wat suggereert dat zowel pijn als angst afnamen. Toen de onderzoekers vervolgens dezelfde excitatoire neuronen kunstmatig uitschakelden, verdwenen de voordelen, wat bevestigt dat het herstel afhankelijk is van het terugbrengen van de activiteit van deze cellen.
Wat dit betekent voor mensen met chronische spierpijn
Samengevat schetst het werk een beeld waarin aanhoudende spierpijn niet alleen in stand wordt gehouden door voortdurende signalen uit het lichaam, maar door een hersencircuit dat is herschikt. In dit model nemen overactieve microglia in een cruciaal prefrontaal gebied excitatoire synapsen weg via CR3-afhankelijke snoei, waardoor de regio verzwakt raakt en minder in staat is pijn en angst te dempen. Door microglia of hun CR3-receptor te blokkeren, konden de onderzoekers deze hersenveranderingen omkeren en symptomen bij ratten verlichten. Hoewel meer onderzoek nodig is om dit naar mensen te vertalen, suggereren de bevindingen dat toekomstige behandelingen voor chronische spierpijn mogelijk gericht zijn op het tot rust brengen of zorgvuldig hertrainen van de eigen immuuncellen van de hersenen in plaats van alleen op zenuwen of spieren te mikken.
Bronvermelding: Luo, M., Wang, L., Liang, Y. et al. Microglial CR3-mediated synaptic pruning in the dmPFC promotes the generation and maintenance of chronic muscle pain via glutamatergic dysfunction. Exp Mol Med 58, 664–680 (2026). https://doi.org/10.1038/s12276-026-01666-7
Trefwoorden: chronische spierpijn, microglia, synaptische snoei, prefrontale cortex, neuroinflammatie