Clear Sky Science · fr
Le rôle du CR3 microglial dans l'élagage synaptique du dmPFC favorise la génération et le maintien de la douleur musculaire chronique via une dysfonction glutamatergique
Pourquoi les courbatures peuvent persister pendant des mois
La plupart d'entre nous s'attendent à ce que les douleurs musculaires disparaissent après quelques jours de repos. Pourtant, pour de nombreuses personnes, la douleur musculaire devient une compagne tenace qui dure des mois et s'accompagne souvent d'anxiété ou d'humeur basse. Cette étude chez le rat explore au‑delà du muscle endolori et se tourne vers le cerveau pour comprendre pourquoi la douleur musculaire chronique peut devenir si persistante et émotionnellement épuisante. Les chercheurs identifient un coupable surprenant : de petites cellules immunitaires du cerveau qui remodèlent discrètement les connexions nerveuses dans une région corticale liée à la douleur.
D'une douleur passagère à une douleur durable
L'équipe a commencé par établir un modèle bien connu de douleur musculaire chronique chez le rat, provoqué par une petite injection de solution saline dans le muscle du mollet. Au départ, les animaux réagissaient fortement au toucher et à la chaleur, comme attendu après une lésion. Mais même des semaines plus tard, alors que l'irritation initiale aurait dû se calmer, leur sensibilité à la douleur restait élevée et ils bougeaient moins et évitaient le centre d'une arène ouverte—des signes de comportement de type anxieux. Des examens cérébraux et des marqueurs cellulaires ont montré une activité réduite dans une région appelée cortex préfrontal dorsomédial, une zone connue pour influencer la façon dont nous ressentons et réagissons à la douleur.
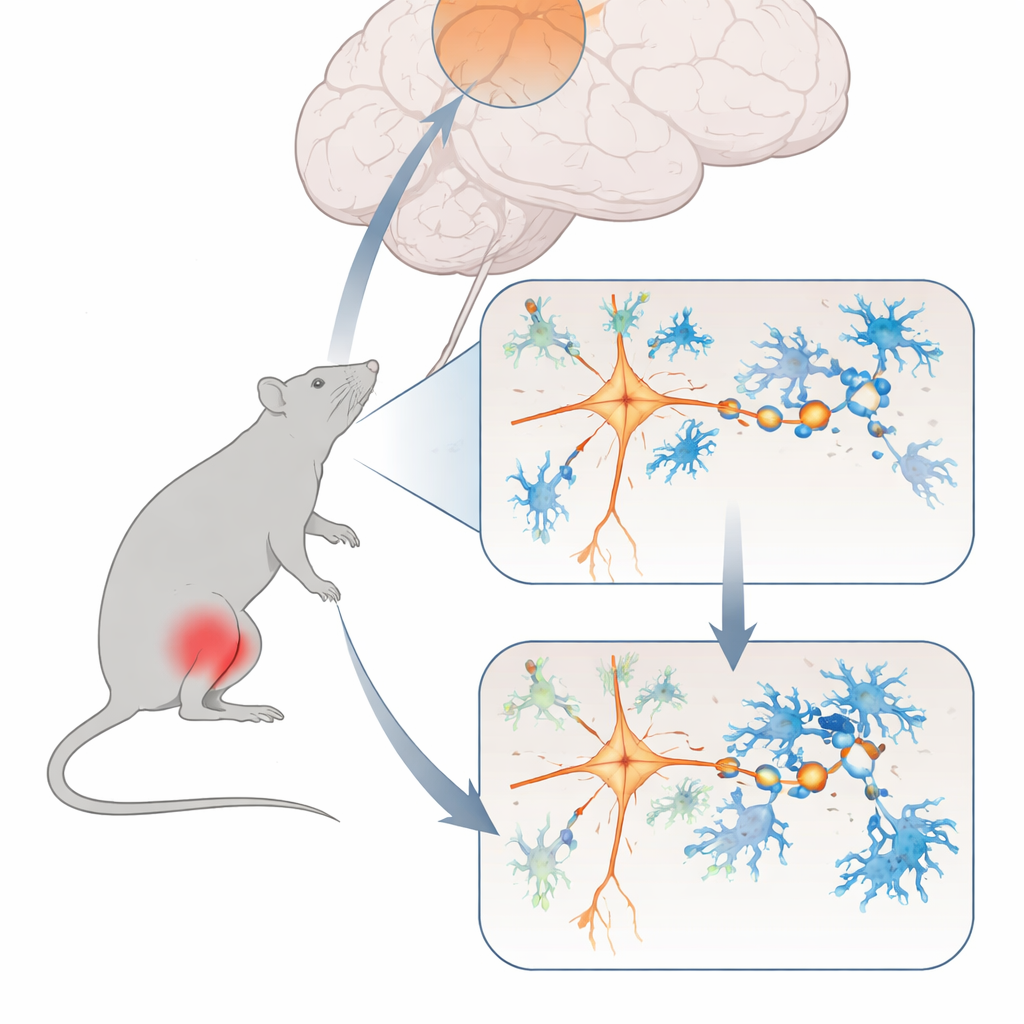
Un centre de contrôle de la douleur mis au silence
Pour vérifier si cette région cérébrale participe réellement au contrôle de la douleur musculaire chronique, les chercheurs ont utilisé des outils génétiques activés par la lumière et par des médicaments pour augmenter ou diminuer l'activité de ses neurones excitateurs, comme un variateur d'intensité. Lorsqu'ils ont renforcé l'activité de ces cellules, les rats sont devenus moins sensibles à la douleur mécanique et ont montré moins de comportements de type anxieux. Lorsqu'ils ont réduit l'activité des mêmes cellules, des animaux sains ont commencé à se comporter davantage comme des sujets souffrant de douleur chronique, et une zone relais de la moelle épinière qui transmet les signaux de douleur est devenue hyperactive. Des enregistrements électriques détaillés ont révélé que, dans la douleur chronique, les neurones corticaux affectés tiraient moins et que leurs synapses excitatrices—ces points de contact minuscules qui transmettent les signaux entre neurones—s'affaiblissaient et diminuaient en nombre.
Les cellules immunitaires cérébrales qui « mangent » les synapses
Qu'est‑ce qui provoque cette perte de connexions saines ? Les chercheurs se sont tournés vers les microglies, les cellules immunitaires résidentes du cerveau, qui agissent comme des jardiniers en élaguant les synapses pendant le développement et en cas de maladie. En utilisant le séquençage ARN single‑cell, ils ont observé que les microglies dans le cortex lié à la douleur basculaient vers un état fortement pro‑inflammatoire, avec une forte expression de gènes associés à l'élagage synaptique. Une molécule, un récepteur appelé CR3, s'est distinguée comme étroitement liée aux voies d'élimination des synapses. Des expériences de microscopie et de cytométrie en flux ont montré que, à mesure que la douleur devenait chronique, les microglies se multipliaient, se rassemblaient autour des neurones actifs et engloutissaient de plus en plus des fragments de synapses excitatrices, tandis que les connexions inhibitrices étaient largement épargnées.
Bloquer l'élagage restaure la fonction cérébrale
Pour savoir si ces microglies étaient réellement à l'origine de la douleur chronique, l'équipe les a temporairement supprimées avec un médicament administré dans le liquide cérébro‑spinal. L'inhibition des microglies a réduit les comportements liés à la douleur, restauré les réponses des neurones corticaux aux stimuli douloureux et inversé les dommages structurels au niveau des synapses. Allant plus loin, les scientifiques ont utilisé une approche virale ciblée pour réduire spécifiquement le CR3 dans les microglies. Cela a diminué leur comportement « mangeur » de synapses, augmenté le nombre et la force des synapses excitatrices, et rendu les neurones corticaux de nouveau plus excitable. Les rats avec des microglies à CR3 réduit montraient des seuils de douleur plus élevés et exploraient davantage, suggérant que la douleur et l'anxiété s'étaient atténuées. Lorsque les chercheurs ont ensuite éteint artificiellement ces mêmes neurones excitateurs, les bénéfices ont disparu, confirmant que le soulagement dépend de la restauration de l'activité de ces cellules.
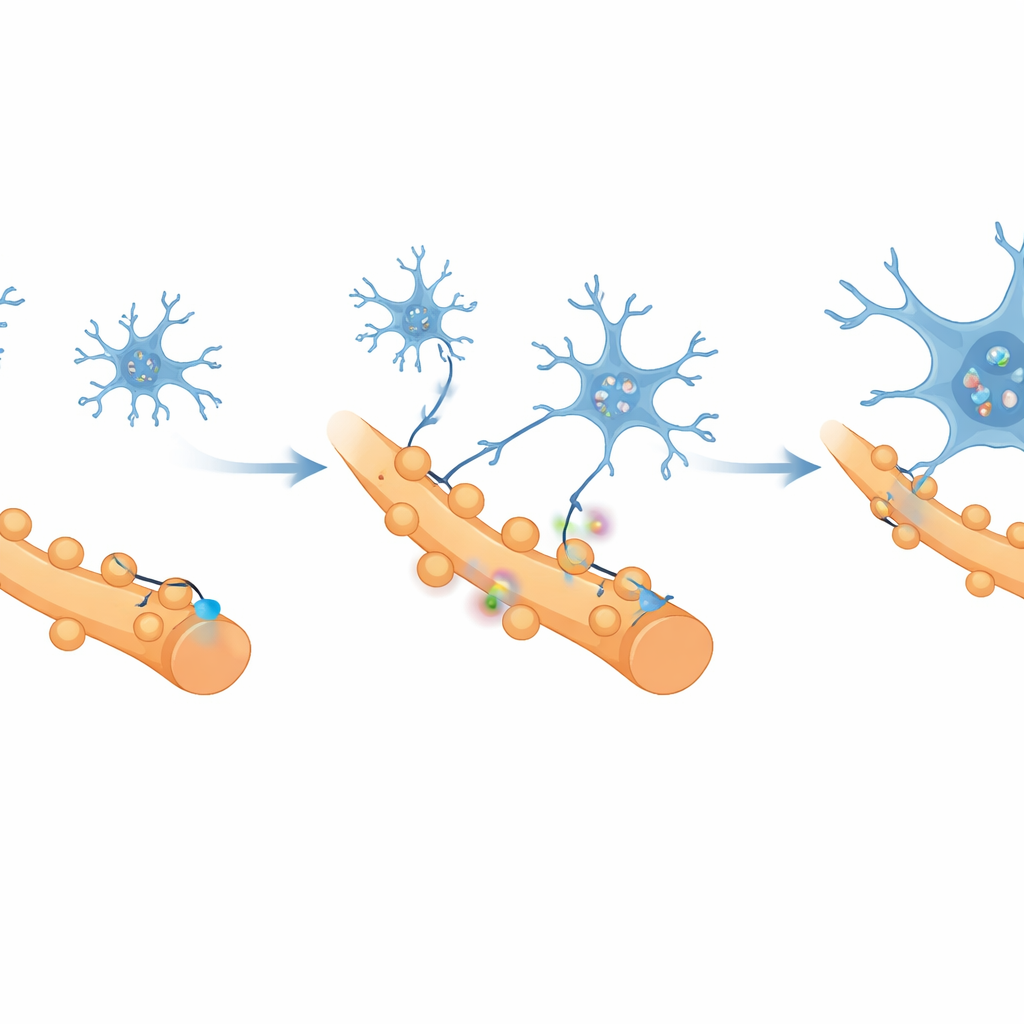
Ce que cela signifie pour les personnes souffrant de douleur musculaire chronique
Dans l'ensemble, le travail dessine un scénario dans lequel la douleur musculaire persistante est entretenue non seulement par des signaux corporels continus mais par un circuit cérébral remodelé. Dans ce modèle, des microglies hyperactives dans une aire préfrontale clé suppriment les synapses excitatrices via un élagage dépendant de CR3, laissant la région sous‑puissante et moins capable d'atténuer la douleur et l'anxiété. En bloquant les microglies ou leur récepteur CR3, les chercheurs ont pu inverser ces changements cérébraux et soulager les symptômes chez le rat. Bien que des études supplémentaires soient nécessaires pour traduire ces résultats chez l'humain, ces découvertes suggèrent que de futurs traitements de la douleur musculaire chronique pourraient viser à calmer, ou à reprogrammer avec prudence, les propres cellules immunitaires du cerveau plutôt que de cibler uniquement les nerfs ou les muscles.
Citation: Luo, M., Wang, L., Liang, Y. et al. Microglial CR3-mediated synaptic pruning in the dmPFC promotes the generation and maintenance of chronic muscle pain via glutamatergic dysfunction. Exp Mol Med 58, 664–680 (2026). https://doi.org/10.1038/s12276-026-01666-7
Mots-clés: douleur musculaire chronique, microglie, élagage synaptique, cortex préfrontal, neuroinflammation