Clear Sky Science · ar
إزالة التشابك المشبكي بواسطة المستقبل CR3 في الخلايا الدقيقة في القشرة الجبهية الوسطى الظهرية تعزز نشوء واستمرار ألم العضلات المزمن عبر خلل غلوتاماتي
لماذا قد تستمر آلام العضلات لأشهر
معظمنا يتوقع أن تزول آلام العضلات بعد أيام قليلة من الراحة. ومع ذلك، بالنسبة لكثير من الأشخاص يصبح ألم العضلات رفيقًا مزعجًا يستمر لشهور وغالبًا ما يرتبط بالقلق أو المزاج المنخفض. تدرس هذه الدراسة على الجرذان ما وراء العضلة المؤلمة نفسها وفي داخل الدماغ، سائلة لماذا يمكن أن يصبح ألم العضلات المزمن مستمرًا ومجهدًا عاطفيًا للغاية. يكشف الباحثون عن متهم مفاجئ: خلايا مناعية صغيرة في الدماغ تعيد تشكيل الاتصالات العصبية بهدوء في منطقة قشرية مرتبطة بالألم.
من ألم عابر إلى ألم طويل الأمد
بدأ الفريق بإنشاء نموذج راسخ لألم العضلات المزمن في الجرذان، ناجم عن حقنة صغيرة من محلول ملحي في عضلة الساق. في البداية، تفاعل الحيوانان بقوة مع اللمس والحرارة، كما هو متوقع بعد الإصابة. لكن حتى بعد أسابيع، عندما كان من المفترض أن يهدأ التهيج الأصلي، بقيت حساسيتهم للألم مرتفعة وحركتهم انخفضت وتجنبوا مركز ساحة مفتوحة — علامات سلوك تشبه القلق. أشارت فحوصات الدماغ والمؤشرات الخلوية إلى انخفاض النشاط في منطقة تُسمى القشرة الجبهية الوسطى الظهرية، وهي منطقة معروفة بتشكيل كيفية شعورنا ورد فعلنا تجاه الألم.
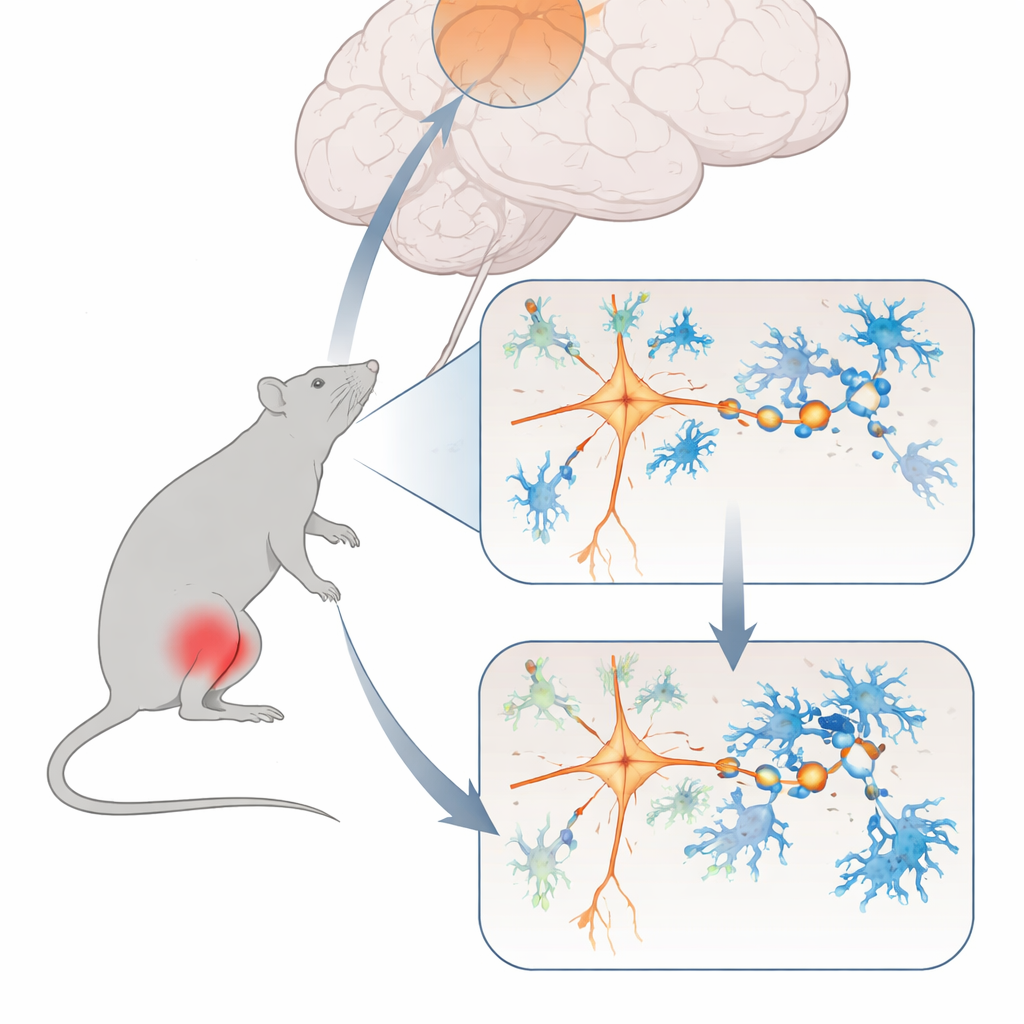
مركز ضبط الألم في الدماغ أصبح هادئًا
لاختبار ما إذا كانت هذه المنطقة الدماغية تساعد فعلاً في ضبط ألم العضلات المزمن، استخدم الباحثون أدوات جينية تعتمد على الضوء والأدوية لزيادة أو خفض نشاط خلاياها التحفيزية كما لو كان مفتاحًا متدرجًا. عندما عززوا نشاط هذه الخلايا، أصبحت الجرذان أقل حساسية للألم الميكانيكي وأظهرت سلوكيات تشبه القلق أقل. وعندما كبحوا نفس الخلايا، بدأت الحيوانات الصحية أيضًا تتصرف أكثر مثل مصابي الألم المزمن، وأظهرت منطقة ناقلة في الحبل الشوكي التي تنقل إشارات الألم نشاطًا مفرطًا. كشفت تسجيلات كهربائية مفصلة أنه، في حالة الألم المزمن، كانت الخلايا القشرية المتأثرة تطلق شحنات أقل وكانت مشابكها التحفيزية — نقاط الاتصال الصغيرة التي تمرر الإشارات بين الخلايا العصبية — أضعف وعددها أقل.
خلايا مناعية دماغية تأكل المشابك
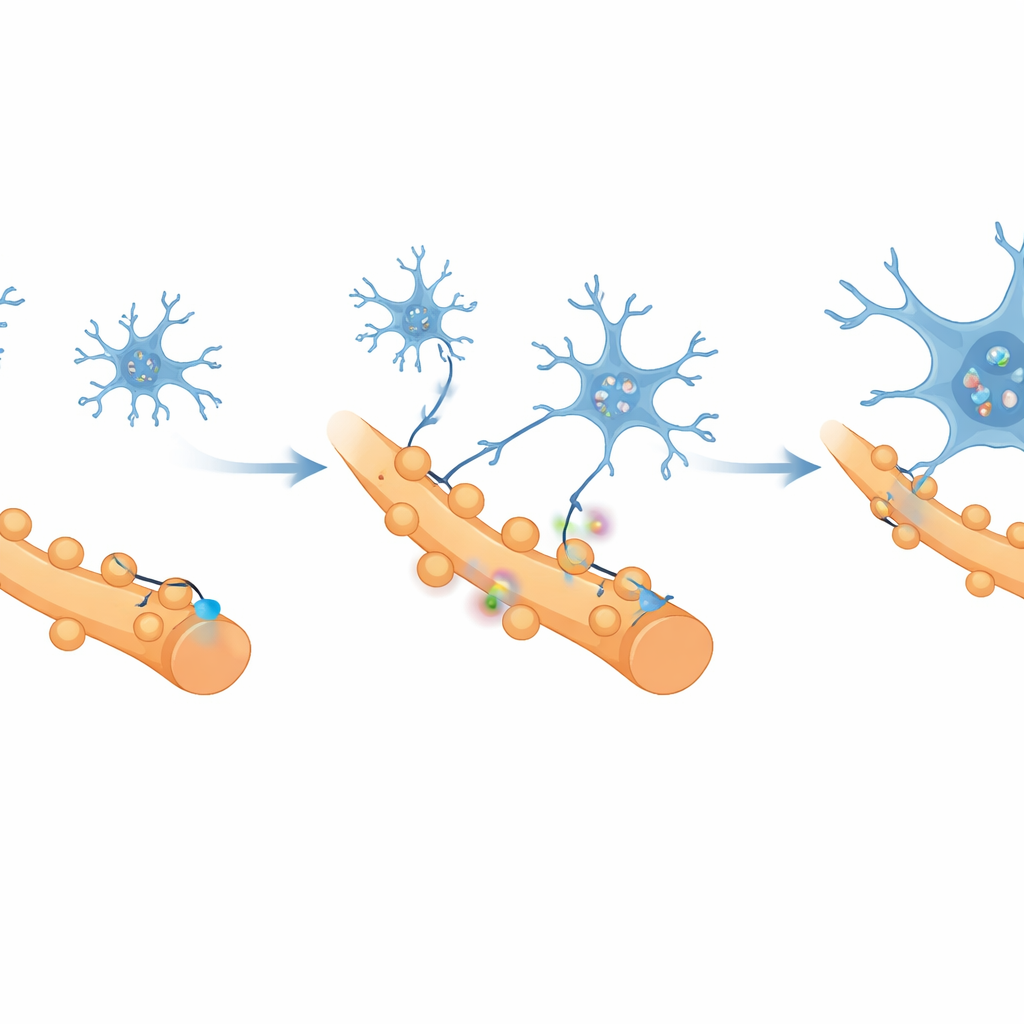
ما الذي يسبب فقدان هذه الاتصالات الصحية؟ توجه الباحثون إلى الخلايا الدقيقة، الخلايا المناعية المقيمة في الدماغ، التي تعمل كالبستانيين الذين يقلمون المشابك أثناء التطور وفي المرض. باستخدام تسلسل RNA لكل خلية على حدة، وجدوا أن الخلايا الدقيقة في القشرة المرتبطة بالألم تحولت إلى حالة التهابية شديدة، مظهرة نشاطًا عاليًا في جينات مرتبطة بتقليم المشابك. برزت جزيئة واحدة، مستقبل يُدعى CR3، كعلاقة وثيقة بالمسارات التي تزيل المشابك. أظهرت تجارب المجهر وتحليل التدفق الخلوي أنه مع تحول الألم إلى حالة مزمنة، تضاعفت الخلايا الدقيقة، وتجمعت حول الخلايا العصبية النشطة، وابتلعت بشكل متزايد أجزاء من المشابك التحفيزية، في حين ظلت الاتصالات المثبطة إلى حد كبير دون مساس.
منع التقليم يعيد وظيفة الدماغ
للتحقق مما إذا كانت هذه الخلايا الدقيقة هي السبب الفعلي للألم المزمن، كبت الفريق نشاطها مؤقتًا بواسطة دواء يُعطى في سائل الدماغ. أدى إسكات الخلايا الدقيقة إلى تقليل سلوكيات الألم، واستعادة استجابات الخلايا القشرية إلى المحفزات المؤلمة، وعكس التلف البنيوي في المشابك. خطوة أبعد، استخدم العلماء نهجًا فيروسيًا مستهدفًا لتقليل CR3 تحديدًا في الخلايا الدقيقة. قلل هذا من سلوكها في أكل المشابك، وزاد عدد وقوة المشابك التحفيزية، وجعل الخلايا القشرية أكثر قابلية للاشتعال مرة أخرى. أظهرت الجرذان ذات الخلايا الدقيقة منخفضة CR3 عتبات ألم أعلى وكانت أكثر استعدادًا للاستكشاف، مما يشير إلى تراجع كل من الألم والقلق. عندما أوقف الباحثون بعد ذلك نفس الخلايا العصبية التحفيزية اصطناعيًا، اختفت الفوائد، مما يؤكد أن التخفيف يعتمد على استعادة نشاط هذه الخلايا.
ماذا يعني هذا للأشخاص المصابين بألم عضلات مزمن
بشكل عام، يرسم العمل صورة يكون فيها الألم العضلي المستمر مدعومًا ليس فقط بإشارات مستمرة من الجسم بل بدائرة دماغية مُعاد تشكيلها. في هذا النموذج، تزيل الخلايا الدقيقة المفرطة النشاط في منطقة أمامية حاسمة المشابك التحفيزية عبر تقليم يعتمد على CR3، مما يترك المنطقة ضعيفة وأقل قدرة على كبح الألم والقلق. من خلال حجب الخلايا الدقيقة أو مستقبل CR3 الخاص بها، استطاع الباحثون عكس هذه التغيرات الدماغية وتخفيف الأعراض في الجرذان. وبينما هناك حاجة لمزيد من الدراسات لترجمة هذا إلى البشر، تشير النتائج إلى أن العلاجات المستقبلية لألم العضلات المزمن قد تأتي من تهدئة، أو إعادة تدريب بحذر، خلايا الدماغ المناعية نفسها بدلًا من استهداف الأعصاب أو العضلات وحدها.
الاستشهاد: Luo, M., Wang, L., Liang, Y. et al. Microglial CR3-mediated synaptic pruning in the dmPFC promotes the generation and maintenance of chronic muscle pain via glutamatergic dysfunction. Exp Mol Med 58, 664–680 (2026). https://doi.org/10.1038/s12276-026-01666-7
الكلمات المفتاحية: ألم العضلات المزمن, الخلايا الدقيقة, تقليم المشابك, قشرة أمامية, الالتهاب العصبي