Clear Sky Science · de
CR3-vermittelte synaptische Ausdünnung durch Mikroglia im dmPFC fördert Entstehung und Aufrechterhaltung chronischer Muskelschmerzen durch glutamaterge Dysfunktion
Warum Muskelschmerzen monatelang anhalten können
Die meisten von uns erwarten, dass Muskelkater nach einigen Tagen Ruhe nachlässt. Für viele Menschen jedoch wird Muskelschmerz zu einem hartnäckigen Begleiter, der monatelang anhält und oft mit Angst oder gedrückter Stimmung einhergeht. Diese Studie an Ratten blickt über das schmerzende Muskelgewebe hinaus ins Gehirn und fragt, warum chronische Muskelschmerzen so persistent und emotional belastend werden können. Die Forschenden identifizieren einen überraschenden Übeltäter: winzige Immunzellen im Gehirn, die still und leise Nervenkontakte in einer schmerzrelevanten Kortikalsregion umgestalten.
Vom kurzen Ziehen zum langanhaltenden Schmerz
Das Team erzeugte zunächst ein etabliertes Modell chronischer Muskelschmerzen bei Ratten durch eine kleine Injektion einer Kochsalzlösung in die Wadenmuskulatur. Zunächst reagierten die Tiere erwartungsgemäß stark auf Berührung und Wärme. Doch selbst Wochen später, wenn die ursprüngliche Reizung abgeklungen sein sollte, blieb ihre Schmerzempfindlichkeit hoch; sie bewegten sich weniger und mieden das Zentrum einer offenen Arena – Anzeichen für angstähnliches Verhalten. Hirnscans und zelluläre Marker wiesen auf eine reduzierte Aktivität in einer Region namens dorsomedialer präfrontaler Kortex hin, einem Gebiet, das bekannt dafür ist, wie wir Schmerz empfinden und darauf reagieren.
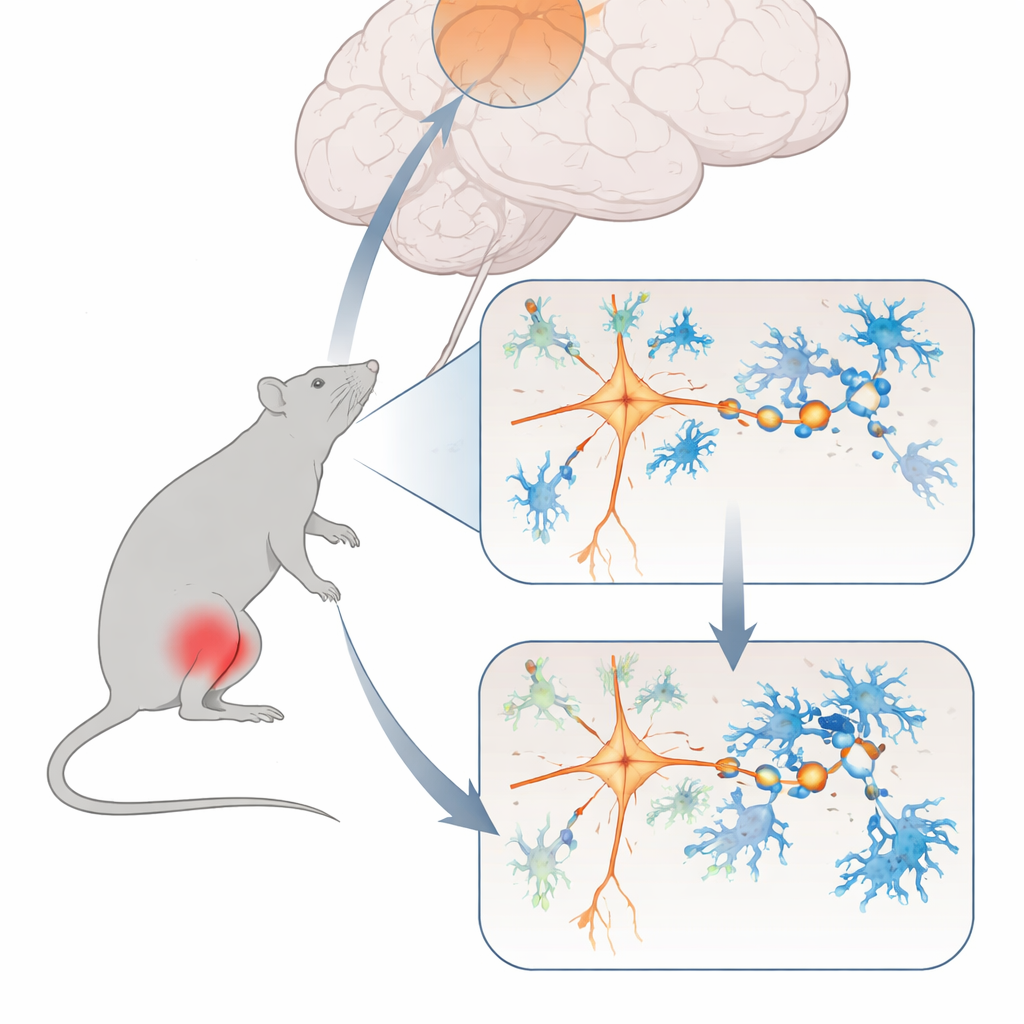
Ein gedämpfter Schmerzkontrollknoten im Gehirn
Um zu prüfen, ob diese Hirnregion tatsächlich die Kontrolle über chronische Muskelschmerzen beeinflusst, nutzten die Forschenden lichtbasierte und pharmakogenetische Werkzeuge, um ihre exzitatorischen Nervenzellen wie einen Dimmer hoch- oder herunterzudrehen. Als sie die Aktivität dieser Zellen erhöhten, wurden die Ratten weniger empfindlich gegenüber mechanischem Schmerz und zeigten weniger angstähnliches Verhalten. Als sie dieselben Zellen dämpften, begannen selbst gesunde Tiere, sich wie Chronisch-Schmerz-Patienten zu verhalten, und eine Schaltstelle im Rückenmark, die Schmerzsignale weiterleitet, wurde überaktiv. Detaillierte elektrische Aufzeichnungen zeigten, dass die betroffenen kortikalen Neurone bei chronischem Schmerz weniger feuerten und ihre exzitatorischen Synapsen – winzige Kontaktpunkte, die Signale zwischen Nervenzellen weitergeben – schwächer und seltener wurden.
Hirn-Immunzellen, die Synapsen „fressen“
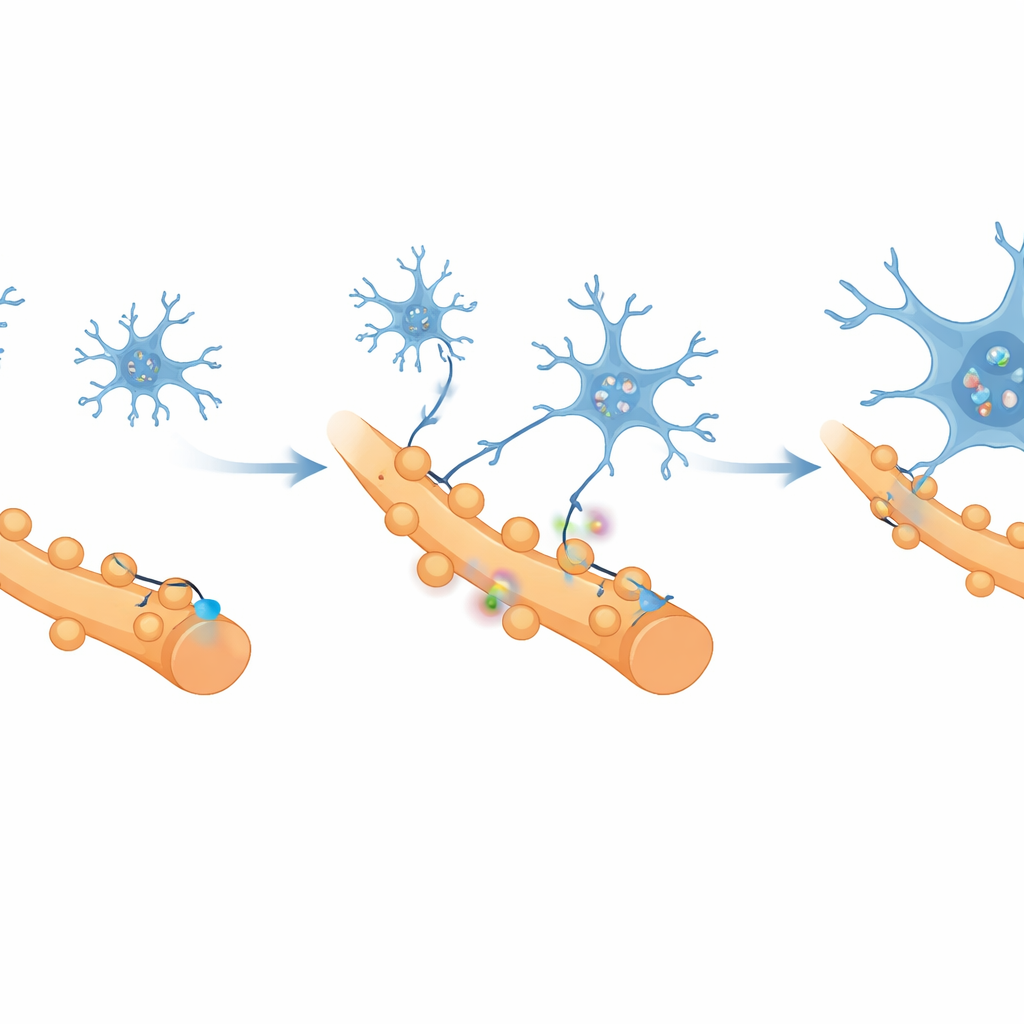
Was verursacht diesen Verlust gesunder Verbindungen? Die Forschenden richteten ihren Blick auf Mikroglia, die residenten Immunzellen des Gehirns, die während der Entwicklung und bei Krankheiten Synapsen beschneiden wie Gärtner. Mittels Einzelzell-RNA-Sequenzierung fanden sie, dass Mikroglia in der schmerzrelevanten Kortikalisregion in einen stark proinflammatorischen Zustand wechselten und eine hohe Aktivität von Genen zeigten, die mit Synapsen-Pruning verknüpft sind. Ein Molekül, der Rezeptor CR3, fiel als eng mit Signalwegen zur Entfernung von Synapsen verbunden auf. Mikroskopie- und Durchflusszytometrie-Experimente zeigten, dass Mikroglia mit zunehmender Chronizität vermehrt auftraten, sich um aktive Neurone sammelten und vermehrt Teile exzitatorischer Synapsen verschlangen, während inhibitorische Verbindungen weitgehend verschont blieben.
Das Blockieren des Prunings stellt Gehirnfunktion wieder her
Um zu prüfen, ob diese Mikroglia tatsächlich chronischen Schmerz antreiben, unterdrückte das Team sie vorübergehend mit einem in die Hirnflüssigkeit verabreichten Medikament. Das Stummschalten der Mikroglia reduzierte Schmerzverhalten, stellte kortikale Neuronenreaktionen auf schmerzhafte Reize wieder her und kehrte strukturelle Schäden an Synapsen um. Einen Schritt weiter nutzten die Wissenschaftler eine gezielte virale Methode, um CR3 spezifisch in Mikroglia zu verringern. Das reduzierte ihr synapsenfressendes Verhalten, erhöhte Anzahl und Stärke exzitatorischer Synapsen und machte kortikale Neurone wieder erregbarer. Ratten mit CR3-reduzierten Mikroglia zeigten höhere Schmerzschwellen und erkundeten mutiger – beides Hinweise darauf, dass sowohl Schmerz als auch Angst nachließen. Wenn die Forschenden anschließend künstlich dieselben exzitatorischen Neurone abschalteten, verschwanden die Vorteile, was bestätigte, dass die Linderung von der Wiederherstellung der Aktivität dieser Zellen abhängt.
Was das für Menschen mit chronischem Muskelschmerz bedeutet
Insgesamt zeichnet die Arbeit das Bild, dass anhaltender Muskelschmerz nicht nur durch fortdauernde Signale aus dem Körper aufrechterhalten wird, sondern durch eine umgestaltete Hirnschaltung. In diesem Modell entfernen überaktive Mikroglia in einer Schlüsselregion des präfrontalen Kortex exzitatorische Synapsen über CR3‑abhängiges Pruning, wodurch die Region unterversorgt bleibt und weniger in der Lage ist, Schmerz und Angst zu dämpfen. Durch das Blockieren von Mikroglia oder ihres CR3-Rezeptors konnten die Forschenden diese Gehirnveränderungen umkehren und Symptome bei Ratten lindern. Obwohl weitere Studien nötig sind, um das auf Menschen zu übertragen, deuten die Befunde darauf hin, dass zukünftige Therapien für chronische Muskelschmerzen eher darauf abzielen könnten, die Immunzellen des Gehirns zu beruhigen oder gezielt umzuschulen, statt nur Nerven oder Muskeln anzugehen.
Zitation: Luo, M., Wang, L., Liang, Y. et al. Microglial CR3-mediated synaptic pruning in the dmPFC promotes the generation and maintenance of chronic muscle pain via glutamatergic dysfunction. Exp Mol Med 58, 664–680 (2026). https://doi.org/10.1038/s12276-026-01666-7
Schlüsselwörter: chronischer Muskelschmerz, Mikroglia, synaptische Ausdünnung, präfrontaler Kortex, Neuroinflammation