Clear Sky Science · zh
肠道微生物调控表观遗传靶点EHMT2:Lacticaseibacillus rhamnosus Fb7-311 调控肾细胞癌细胞凋亡与转移
为什么你的肠道可能与肾癌相关
研究人员正发现肠道内细菌与远端器官癌症之间存在令人惊讶的关联。本研究探讨了一种特定肠道微生物与肾癌细胞内的分子“开关”如何协同决定肿瘤是生长还是自我毁灭。理解这种联系可能为将精准药物与精心挑选的益生菌相结合的新型治疗开辟道路。
一种亟需新疗法的致命肾癌
肾细胞癌是最常见的肾癌类型,一旦扩散到肾脏以外往往致命。手术、放疗、免疫疗法和靶向药物能帮助部分患者,但许多人在疾病已经转移时仍面临较差的预后。作者将注意力集中在细胞内的一种蛋白EHMT2上,该蛋白帮助更紧密地包装DNA并沉默某些基因。通过分析大型公共癌症数据库和患者组织样本,他们发现肾脏肿瘤中EHMT2的表达显著高于正常肾组织,且EHMT2水平较高的患者往往生存期较短。
触发肿瘤细胞内的死亡开关
为探明EHMT2在肾癌中的实际作用,研究组在两种人类肾癌细胞系中通过基因学方法和一种名为BIX-01294的小分子抑制剂降低其水平。在两种情况下,阻断EHMT2都减慢了细胞增殖,诱导细胞自杀(凋亡),并降低了癌细胞的迁移与侵袭能力,这些行为与转移相关。研究人员将这些效应追溯到另一种蛋白DDIT3,该蛋白通常被维持在低水平,但在应激下被激活时可驱动细胞走向程序性死亡。他们证明EHMT2在DDIT3基因附近的DNA包装上留下化学标记以保持其沉默;当EHMT2被去除或抑制时,这些标记减弱,DDIT3水平上升,癌细胞被推动走向自我毁灭。
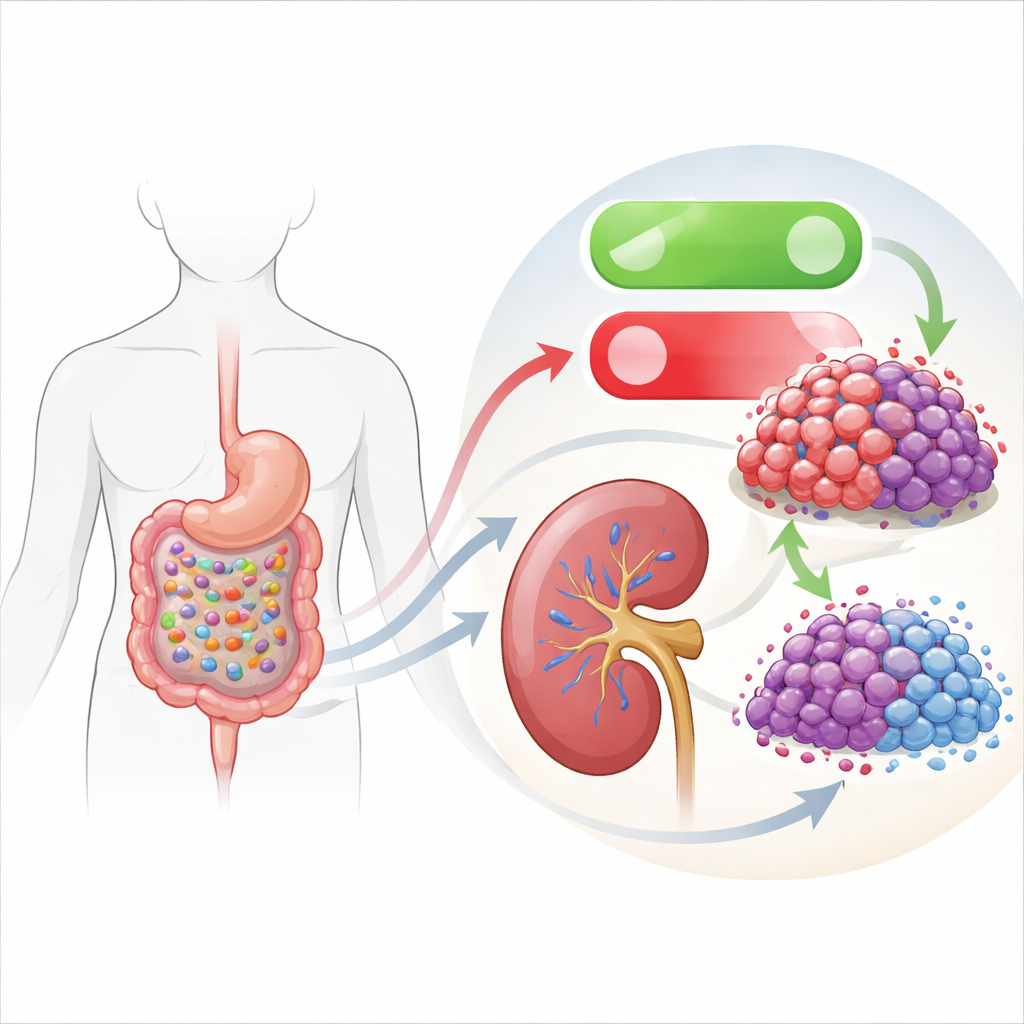
肠道细菌如何模拟精准药物作用
工作中最有趣的部分将这一内部死亡开关与肠道微生物群联系了起来。研究组筛选了多种肠道细菌的培养上清,发现来自一株名为Lacticaseibacillus rhamnosus Fb7-311的菌株的培养液能显著抑制肾癌细胞生长。当肿瘤细胞暴露于该菌株上清时,出现了与直接抑制EHMT2相同的模式:EHMT2下降、DDIT3上升、更多的生化凋亡标志以及迁移与侵袭减少。作者证实DDIT3基因附近的化学标记减少,表明细菌产物以间接方式松动了EHMT2对这一关键促死基因的控制。
聚焦一种抗癌微生物分子
为确定在细菌培养液中究竟是哪种物质负责作用,研究人员对上清进行了详细的化学分析,并与既往关于抗癌代谢物的研究进行比对。他们将候选物缩小到六种并逐一在肾癌细胞上测试。一个化合物——吲哚-3-甲酰(indole-3-carbinol)——脱颖而出。这种分子已知存在于十字花科蔬菜及某些微生物代谢途径中,不仅抑制细胞生长,还降低EHMT2水平并提升DDIT3,复制了该细菌本身触发的核心分子模式。这提示由Fb7-311产生的吲哚-3-甲酰可能是通过表观遗传改变将肿瘤细胞重编程为走向死亡的关键信使。
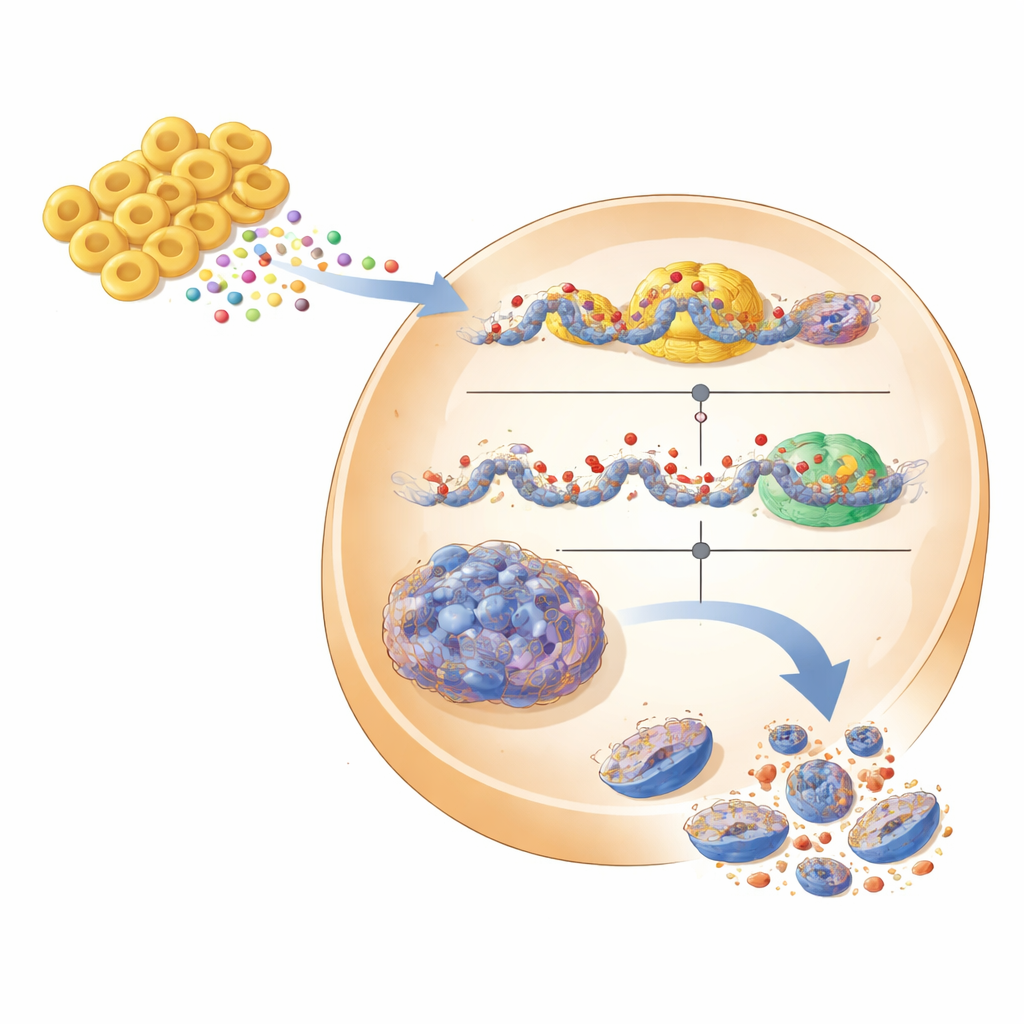
从实验模型走向未来疗法
为更接近真实条件,研究组在更能模拟实体瘤的三维肿瘤球模型和携带人类肾癌移植瘤的小鼠中测试了他们的假设。在肿瘤球中,敲低EHMT2、用抑制剂处理或添加Fb7-311上清均导致致密的肿瘤球解体,伴随DDIT3升高和更强的细胞死亡信号。在小鼠中,EHMT2抑制剂使肿瘤缩小且未见明显体重下降或重大毒性,处理组肿瘤显示更多DDIT3。尽管仍有许多障碍——例如证明Fb7-311可在患者体内安全定植、其在人体肠道中是否产生相同代谢物以及这些代谢物是否能完整到达肾脏——该研究勾画出一条引人注目的路径。它将EHMT2定位为肾细胞癌中有前景的分子靶点,并暗示定制益生菌或其纯化代谢物未来或可作为药物的补充,以在肾脏肿瘤中开启内在的促死程序。
引用: Lee, J., Lee, J., Tae, I.H. et al. Gut microbiota modulation of epigenetic target EHMT2: Lacticaseibacillus rhamnosus Fb7-311 regulated renal cell carcinoma apoptosis and metastasis. Exp Mol Med 58, 739–754 (2026). https://doi.org/10.1038/s12276-026-01659-6
关键词: 肾细胞癌, 表观遗传治疗, 肠道微生物组, 益生菌抗癌疗法, 吲哚-3-甲酰