Clear Sky Science · ar
تعديل ميكروبيوم الأمعاء للمستهدف فوق الجيني EHMT2: Lacticaseibacillus rhamnosus Fb7-311 ينظم موت الخلايا وانتشار سرطان الخلايا الكلوية
لماذا قد يكون جهاز أمعائك مهمًا لسرطان الكلى
يكشف الباحثون عن روابط مفاجئة بين البكتيريا التي تعيش في أمعائنا والأورام في أعضاء بعيدة. تتناول هذه الدراسة كيف يعمل ميكروب أمعائي محدد ومفتاح جزيئي داخل خلايا سرطان الكلى معًا للتحكم فيما إذا كانت الأورام تنمو أو تنهار ذاتيًا. قد يفتح فهم هذا الاتصال الباب لعلاجات جديدة تجمع بين أدوية دقيقة وبروبيوتيك مختار بعناية.
سرطان كلوي قاتل بحاجة إلى خيارات جديدة
سرطان الخلايا الكلوية هو الشكل الأكثر شيوعًا لسرطان الكلى وغالبًا ما يكون مميتًا بمجرد انتشاره خارج الكلية. تساعد الجراحة والإشعاع والعلاجات المناعية والأدوية الموجهة بعض المرضى، لكن كثيرين ما يزالون يواجهون توقعات سيئة، خصوصًا عندما تكون المرض قد نُقِل. ركز المؤلفون على بروتين داخل الخلايا يُسمى EHMT2، الذي يساعد على تضييق حزم الحمض النووي وإسكات جينات معينة. من خلال تحليل مجموعات بيانات سرطان عامة كبيرة وعينات أنسجة المرضى، وجدوا أن الأورام الكلوية تنتج كمية أكبر بكثير من EHMT2 مقارنة بأنسجة الكلية الطبيعية، وأن المرضى ذوي المستويات الأعلى من هذا البروتين يميلون إلى قصر عمر البقاء.
قلب مفتاح الموت داخل الخلايا الورمية
ليروا ما يفعله EHMT2 فعليًا في سرطان الكلى، قلل الفريق مستوياته في سطرين خلويين بشريين لسرطان الكلى باستخدام أدوات وراثية ودواء مثبط جزيئي صغير يعرف باسم BIX-01294. في كلتا الحالتين، أدى حجب EHMT2 إلى إبطاء نمو الخلايا، وإحداث انتحار خلوي مبرمج (موت مبرمج)، وتقليل قدرة خلايا السرطان على الحركة والغزو، وهي سلوكيات مرتبطة بالنقائل. تتبع الباحثون هذه التأثيرات إلى بروتين آخر هو DDIT3، الذي عادةً ما يكون منخفضًا لكنه قادر على دفع الخلايا نحو الموت المبرمج عند تنشيطه تحت الضغط. أظهروا أن EHMT2 يعلّم كيميائيًا حزم الحمض النووي قرب جين DDIT3 بطريقة تبقيه مطفأ؛ عندما يُزال EHMT2 أو يُثبط، تتلاشى هذه العلامات، وترتفع مستويات DDIT3، وتدفع خلايا السرطان نحو الانتحار الخلوي.
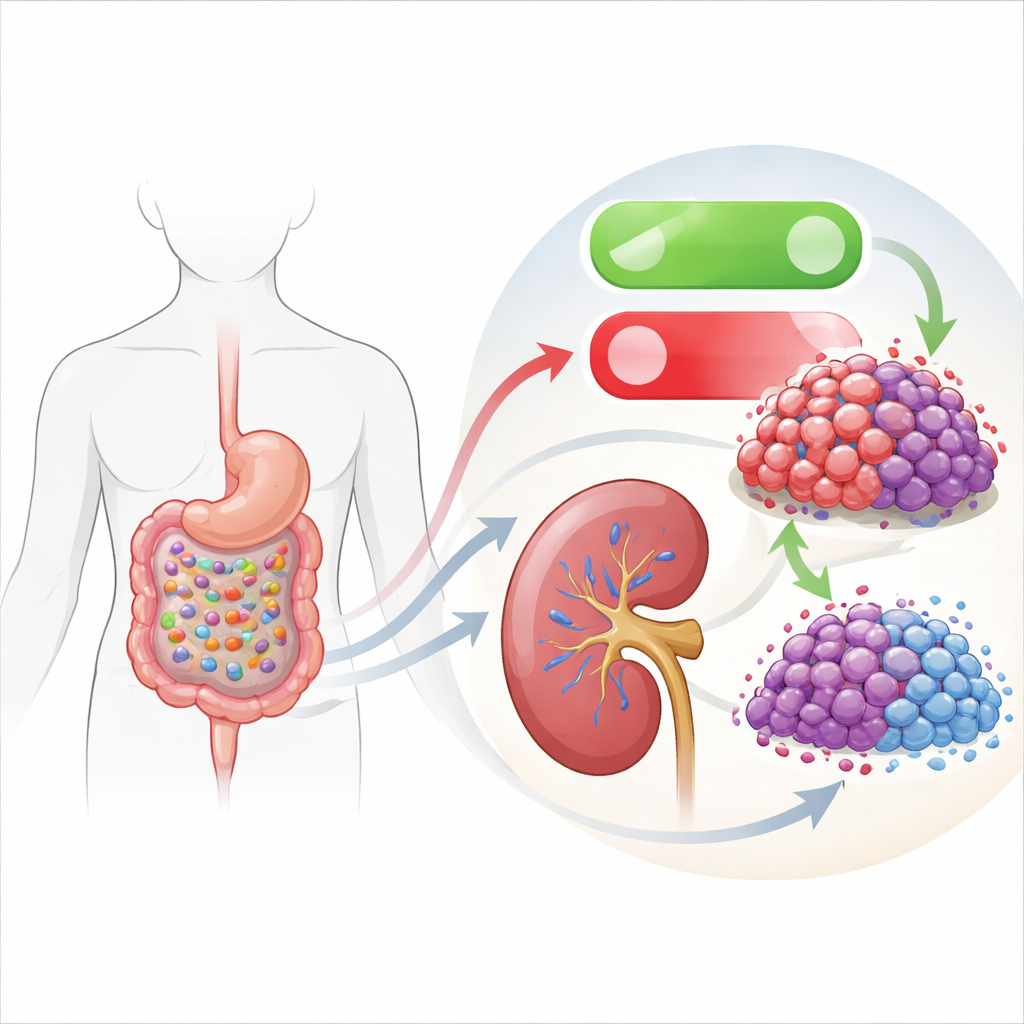
كيف يقلد ميكروب أمعائي دواءً دقيقًا
أكثر أجزاء العمل إثارة يربط مفتاح الموت الداخلي هذا بميكروبيوم الأمعاء. فحص الفريق مرق الزرع من بكتيريا معوية مختلفة واكتشف أن السائل من سلالة تسمى Lacticaseibacillus rhamnosus Fb7-311 أبطأ بشدة نمو خلايا سرطان الكلى. عندما تعرَّضت الخلايا الورمية لهذا المستحلب البكتيري، أظهرت نفس النمط المرصود مع تثبيط EHMT2 المباشر: انخفاض EHMT2، وارتفاع DDIT3، ومزيد من العلامات الكيميائية الحيوية للموت المبرمج، وقلة الهجرة والغزو. أكد المؤلفون أن العلامات الكيميائية قرب جين DDIT3 تقلصت، مما يشير إلى أن منتجات البكتيريا كانت تخفف بصورة غير مباشرة قبضة EHMT2 على هذا الجين المحفز للموت.
التدقيق في جزيء ميكروبي مكافحة للسرطان
لتحديد ما كان مسؤولًا في مرق البكتيريا، أجرى الباحثون تحليلاً كيميائيًا مفصلاً للمستحلب ووفقوه مع دراسات سابقة للوسائط المضادة للسرطان. قلصوا القائمة إلى ستة مرشحين واختبروهم فرديًا على خلايا سرطان الكلى. برز مركب واحد هو الإندول-3-كاربينول—جزيء معروف بالفعل من الخضراوات الصليبية وبعض المسارات الميكروبية. لم يقم هذا المركب فقط بكبح نمو الخلايا بل خفض أيضًا مستويات EHMT2 وعزز DDIT3، مكررًا النمط الجزيئي الأساسي الذي تثيره البكتيريا نفسها. هذا يشير إلى أن الإندول-3-كاربينول، المنتج بواسطة Fb7-311، قد يكون رسولًا رئيسيًا يعيد برمجة الخلايا الورمية نحو الموت عبر تغييرات فوق جينية.
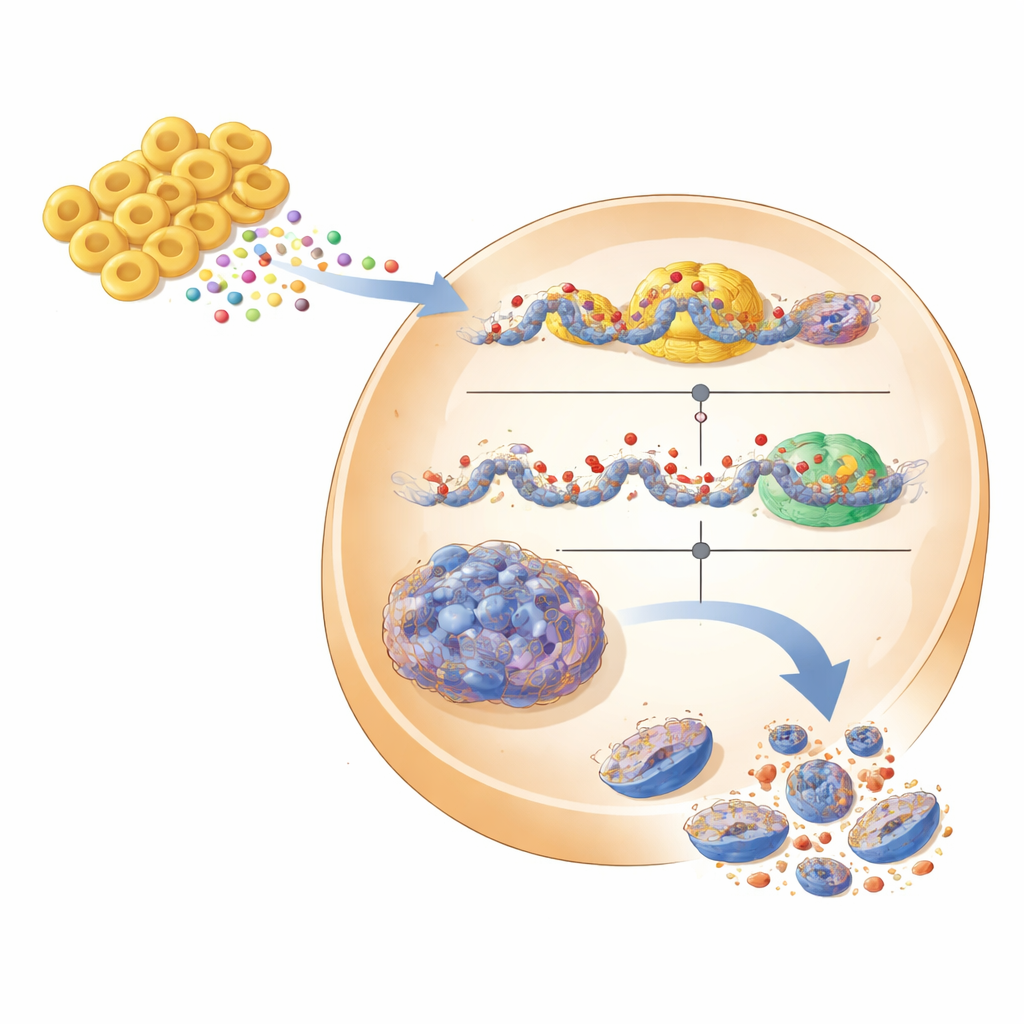
من نماذج المختبر نحو علاجات مستقبلية
للاقتراب من الظروف الحقيقية، اختبر الفريق أفكارهم في كريات ورمية ثلاثية الأبعاد، التي تحاكي الأورام الصلبة بشكل أفضل، وفي فئران تحمل زراعة سرطان كلى بشرية. في الكريات، أدى خفض EHMT2 أو المعالجة بالمثبط الدوائي أو إضافة مستحلب Fb7-311 كلها إلى تفكيك الكريات الورمية المدمجة، مع ارتفاع DDIT3 وإشارات موت خلوي أقوى. في الفئران، قلص مثبط EHMT2 الأورام بدون فقدان وزن واضح أو سمية كبيرة، وأظهرت الأورام المعالجة المزيد من DDIT3. بينما لا تزال هناك عقبات كثيرة—مثل إثبات أن Fb7-311 يمكن أن يستعمر المرضى بأمان، وأنه ينتج نفس المستقلبات في أمعاء الإنسان وأن هذه المركبات تصل إلى الكلية دون تغيير—توفر الدراسة مسارًا مقنعًا. تضع EHMT2 كهدف جزيئي واعد في سرطان الخلايا الكلوية وتقترح أن بروبيوتيك مخصصًا أو مستقلباته المنقاة قد يكمل الأدوية يومًا ما لتشغيل برامج موت مدمجة في أورام الكلى.
الاستشهاد: Lee, J., Lee, J., Tae, I.H. et al. Gut microbiota modulation of epigenetic target EHMT2: Lacticaseibacillus rhamnosus Fb7-311 regulated renal cell carcinoma apoptosis and metastasis. Exp Mol Med 58, 739–754 (2026). https://doi.org/10.1038/s12276-026-01659-6
الكلمات المفتاحية: سرطان الخلايا الكلوية, العلاج فوق الجيني, ميكروبيوم الأمعاء, علاج السرطان بالخمائر المفيدة, إندول-3-كاربينول