Clear Sky Science · pt
Modulação da microbiota intestinal do alvo epigenético EHMT2: Lacticaseibacillus rhamnosus Fb7-311 regulou apoptose e metástase de carcinoma de células renais
Por que seu intestino pode importar para o câncer de rim
Pesquisadores vêm descobrindo conexões surpreendentes entre as bactérias que habitam nosso intestino e cânceres em órgãos distantes. Este estudo investiga como um microrganismo intestinal específico e um “interruptor” molecular dentro das células do câncer renal atuam juntos para controlar se os tumores crescem ou se autodestruem. Compreender essa conexão pode abrir caminho para novos tratamentos que combinem medicamentos de precisão com probióticos cuidadosamente selecionados.
Um câncer renal letal que precisa de novas opções
O carcinoma de células renais é a forma mais comum de câncer de rim e costuma ser letal quando se espalha além do órgão. Cirurgia, radiação, imunoterapias e medicamentos-alvo ajudam alguns pacientes, mas muitos ainda enfrentam um prognóstico ruim, sobretudo quando a doença já metastatizou. Os autores focaram em uma proteína dentro das células, chamada EHMT2, que contribui para compactar o DNA e silenciar certos genes. Ao analisar grandes bases públicas de dados sobre câncer e amostras de tecido de pacientes, eles descobriram que tumores renais produzem muito mais EHMT2 do que o tecido renal normal e que pacientes com níveis mais altos dessa proteína tendem a ter sobrevivência mais curta.
Virando o interruptor da morte dentro das células tumorais
Para ver o que a EHMT2 realmente faz no câncer renal, a equipe reduziu seus níveis em duas linhagens humanas de câncer renal usando ferramentas genéticas e um inibidor de pequena molécula conhecido como BIX-01294. Em ambos os casos, bloquear a EHMT2 retardou o crescimento celular, desencadeou suicídio celular (apoptose) e reduziu a capacidade das células cancerosas de se mover e invadir — comportamentos associados à metástase. Os pesquisadores rastrearam esses efeitos até outra proteína, DDIT3, que normalmente é mantida em níveis baixos mas pode conduzir as células à morte programada quando ativada sob estresse. Eles mostraram que a EHMT2 marca quimicamente a embalagem do DNA nas proximidades do gene DDIT3 de modo a mantê-lo desligado; quando a EHMT2 é removida ou inibida, essas marcas desaparecem, os níveis de DDIT3 aumentam e as células cancerosas são impulsionadas à autodestruição.
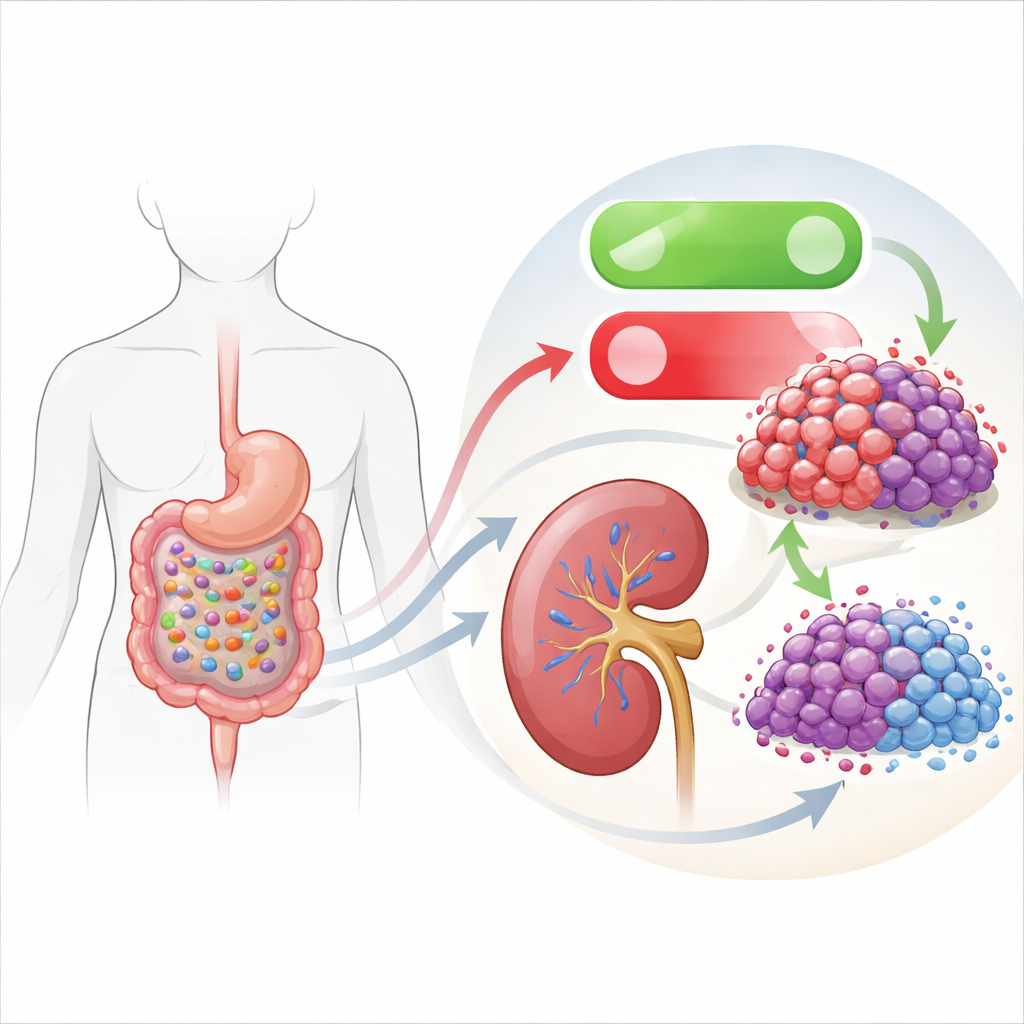
Como uma bactéria intestinal imita um medicamento de precisão
A parte mais intrigante do trabalho liga esse interruptor interno de morte à microbiota intestinal. A equipe triou caldos de cultura de várias bactérias intestinais e descobriu que o sobrenadante de uma linhagem chamada Lacticaseibacillus rhamnosus Fb7-311 retardou fortemente o crescimento das células de câncer renal. Quando as células tumorais foram expostas a esse sobrenadante bacteriano, elas exibiram o mesmo padrão visto com a inibição direta da EHMT2: menor EHMT2, maior DDIT3, mais sinais bioquímicos de apoptose e menos migração e invasão. Os autores confirmaram que as marcas químicas nas proximidades do gene DDIT3 foram reduzidas, indicando que os produtos bacterianos estavam indiretamente afrouxando o controle da EHMT2 sobre esse gene chave promotor da morte.
Aproximando-se de uma molécula microbiana que combate o câncer
Para identificar o que no caldo bacteriano era responsável, os pesquisadores realizaram um perfil químico detalhado do sobrenadante e o confrontaram com estudos prévios de metabólitos anticancerígenos. Eles reduziram a lista a seis candidatos e os testaram individualmente em células de câncer renal. Um composto, indol-3-carbinol — uma molécula já conhecida por estar em vegetais crucíferos e em algumas vias microbianas — destacou-se. Ele não apenas suprimiu o crescimento celular, como também reduziu os níveis de EHMT2 e elevou o DDIT3, reproduzindo o padrão molecular central desencadeado pela própria bactéria. Isso sugere que o indol-3-carbinol, produzido por Fb7-311, pode ser uma mensagem chave que reprograma células tumorais em direção à morte por meio de alterações epigenéticas.
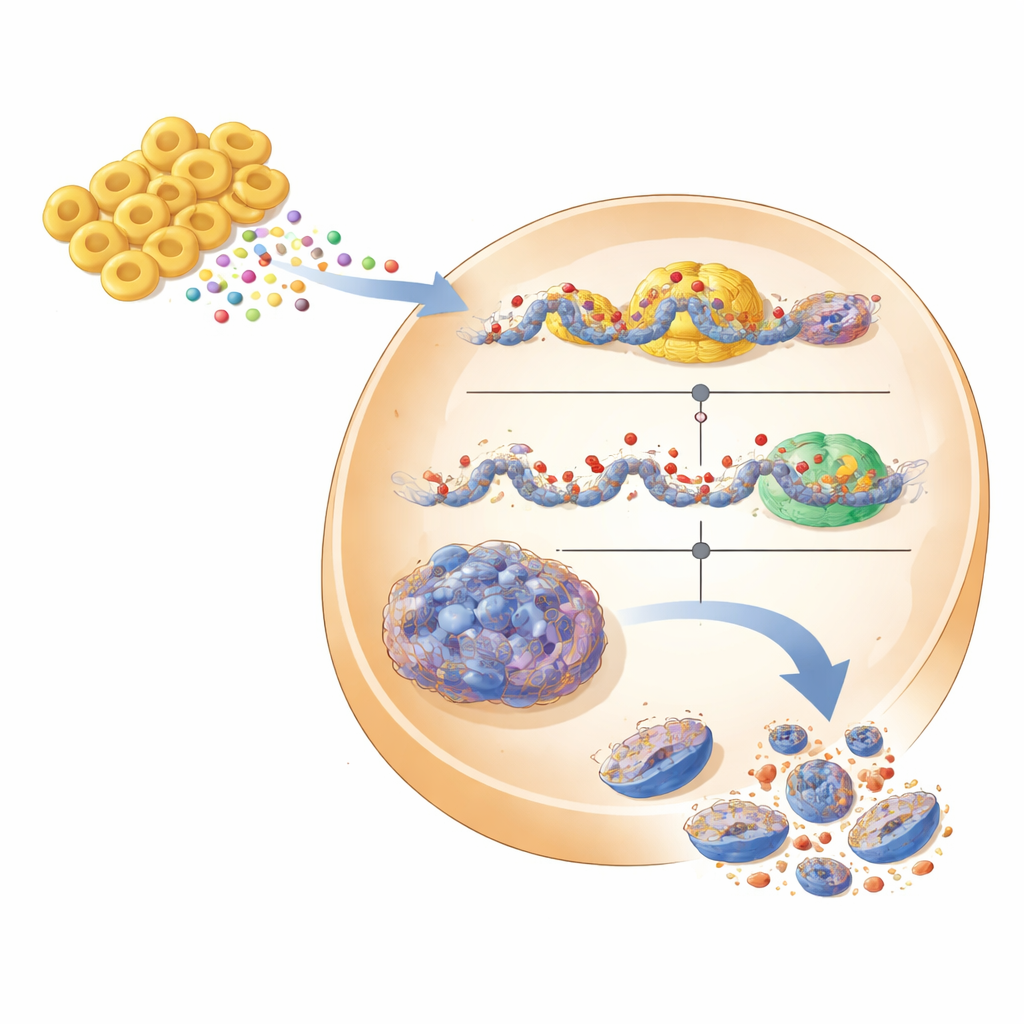
De modelos de laboratório rumo a futuras terapias
Para se aproximar de condições do mundo real, a equipe testou suas ideias em esferoides tumorais tridimensionais, que imitam melhor tumores sólidos, e em camundongos com enxertos de câncer renal humano. Nos esferoides, reduzir a EHMT2, tratar com o inibidor ou adicionar o sobrenadante de Fb7-311 fez as bolas tumorais compactas se desagregarem, acompanhadas por maior DDIT3 e sinais mais fortes de morte celular. Em camundongos, o inibidor de EHMT2 encolheu os tumores sem perda de peso óbvia ou toxicidade importante, e os tumores tratados exibiram mais DDIT3. Embora muitos obstáculos permaneçam — como provar que Fb7-311 pode colonizar pacientes com segurança, que produz os mesmos metabólitos no intestino humano e que estes alcançam o rim intactos — o trabalho delineia um caminho convincente. Posiciona a EHMT2 como um alvo molecular promissor no carcinoma de células renais e sugere que um probiótico sob medida ou seus metabólitos purificados possam, no futuro, complementar medicamentos para ativar programas internos de morte em tumores renais.
Citação: Lee, J., Lee, J., Tae, I.H. et al. Gut microbiota modulation of epigenetic target EHMT2: Lacticaseibacillus rhamnosus Fb7-311 regulated renal cell carcinoma apoptosis and metastasis. Exp Mol Med 58, 739–754 (2026). https://doi.org/10.1038/s12276-026-01659-6
Palavras-chave: carcinoma de células renais, terapia epigenética, microbioma intestinal, tratamento do câncer com probióticos, indol-3-carbinol