Clear Sky Science · it
La modulazione del microbiota intestinale dell'epigenetico bersaglio EHMT2: Lacticaseibacillus rhamnosus Fb7-311 regola l'apoptosi e la metastasi del carcinoma renale
Perché il tuo intestino potrebbe contare nel cancro al rene
I ricercatori stanno scoprendo collegamenti sorprendenti tra i batteri che vivono nell'intestino e i tumori in organi distanti. Questo studio esplora come un microbo intestinale specifico e un «interruttore» molecolare all'interno delle cellule del carcinoma renale collaborino per controllare se i tumori crescono o si autodistruggono. Comprendere questa connessione potrebbe aprire la strada a nuovi trattamenti che combinano farmaci di precisione con probiotici selezionati con cura.
Un carcinoma renale letale che necessita di nuove opzioni
Il carcinoma a cellule renali è la forma più comune di cancro al rene ed è spesso mortale una volta che si è diffuso oltre il rene. Chirurgia, radioterapia, terapie immunitarie e farmaci mirati aiutano alcuni pazienti, ma molti affrontano ancora una prognosi sfavorevole, soprattutto quando la malattia ha già dato metastasi. Gli autori si sono concentrati su una proteina all'interno delle cellule, chiamata EHMT2, che contribuisce a compattare il DNA e a silenziare determinati geni. Analizzando ampi dataset pubblici sul cancro e campioni tissutali di pazienti, hanno riscontrato che i tumori renali producono molto più EHMT2 rispetto al tessuto renale normale e che i pazienti con livelli più alti di questa proteina tendono ad avere una sopravvivenza più breve.
Attivare l'interruttore della morte dentro le cellule tumorali
Per vedere cosa fa realmente EHMT2 nel carcinoma renale, il team ne ha ridotto i livelli in due linee cellulari umane di carcinoma renale usando strumenti genetici e un inibitore di piccola molecola noto come BIX-01294. In entrambi i casi, bloccare EHMT2 rallentava la crescita cellulare, innescava il suicidio cellulare (apoptosi) e riduceva la capacità delle cellule tumorali di muoversi e invadere, comportamenti associati alla metastasi. I ricercatori hanno ricondotto questi effetti a un'altra proteina, DDIT3, che normalmente è mantenuta bassa ma può spingere le cellule verso la morte programmata quando attivata sotto stress. Hanno dimostrato che EHMT2 marca chimicamente l'impacchettamento del DNA vicino al gene DDIT3 in modo da tenerlo spento; quando EHMT2 viene rimosso o inibito, questi marchi si attenuano, i livelli di DDIT3 aumentano e le cellule tumorali vengono spinte all'autodistruzione.
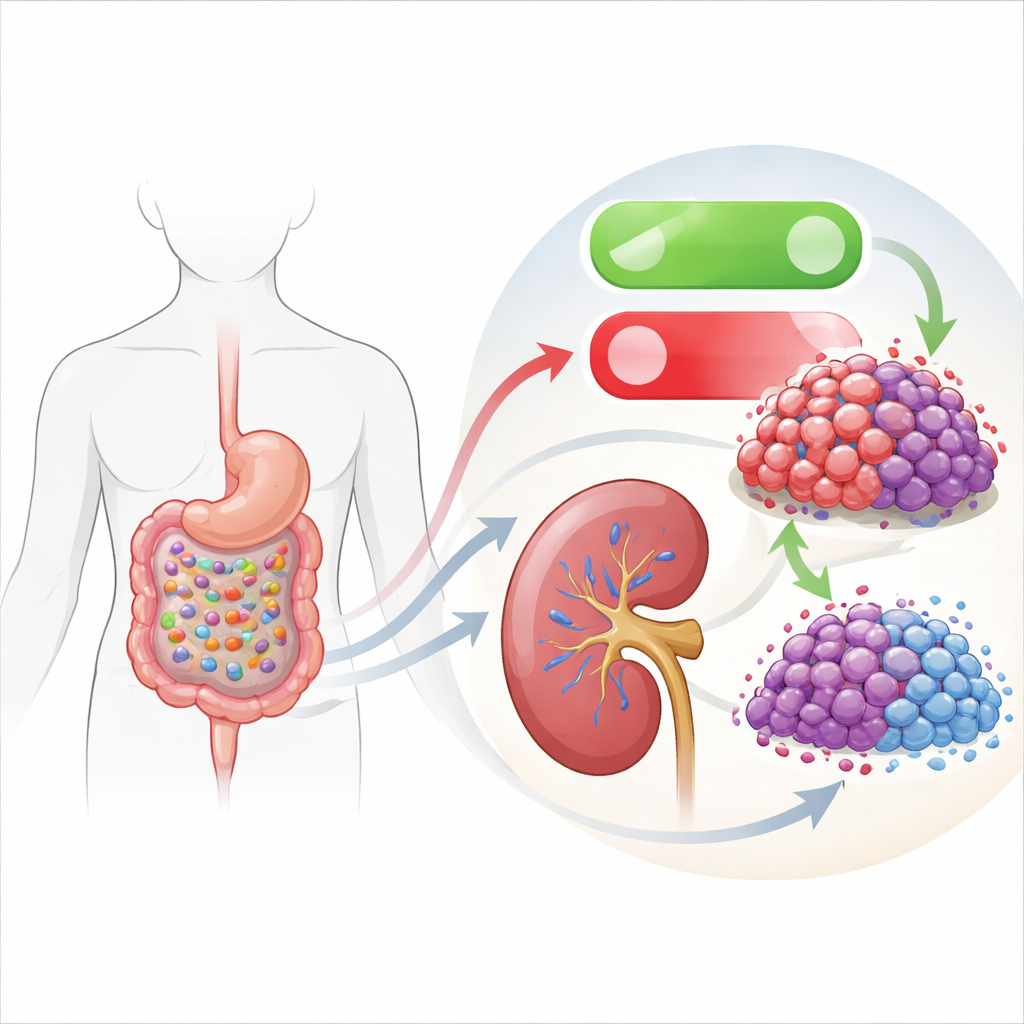
Come un batterio intestinale imita un farmaco di precisione
La parte più intrigante del lavoro collega questo interruttore interno della morte al microbiota intestinale. Il team ha esaminato i brodi di coltura di vari batteri intestinali e ha scoperto che il liquido di una ceppo chiamato Lacticaseibacillus rhamnosus Fb7-311 rallentava fortemente la crescita delle cellule di carcinoma renale. Quando le cellule tumorali venivano esposte a questo soprannatante batterico, mostrano lo stesso schema osservato con l'inibizione diretta di EHMT2: EHMT2 ridotto, DDIT3 aumentato, più segni biochimici di apoptosi e minore migrazione e invasione. Gli autori hanno confermato che i marchi chimici vicino al gene DDIT3 erano ridotti, indicando che i prodotti batterici stavano allentando indirettamente la presa di EHMT2 su questo gene chiave promotore della morte.
Avvicinarsi a una molecola microbica antitumorale
Per identificare cosa nel brodo batterico fosse responsabile, i ricercatori hanno eseguito un profilo chimico dettagliato del soprannatante e lo hanno incrociato con studi precedenti sui metaboliti anticancro. Hanno ristretto la lista a sei candidati e li hanno testati individualmente su cellule di carcinoma renale. Una molecola, l'indolo-3-carbinolo—una sostanza già nota dalle crucifere e da alcuni percorsi microbici—è emersa in modo significativo. Non solo sopprimeva la crescita cellulare, ma abbassava anche i livelli di EHMT2 e aumentava DDIT3, riproducendo il modello molecolare centrale indotto dal batterio stesso. Questo suggerisce che l'indolo-3-carbinolo, prodotto da Fb7-311, possa essere un messaggero chiave che riprogramma le cellule tumorali verso la morte tramite cambiamenti epigenetici.
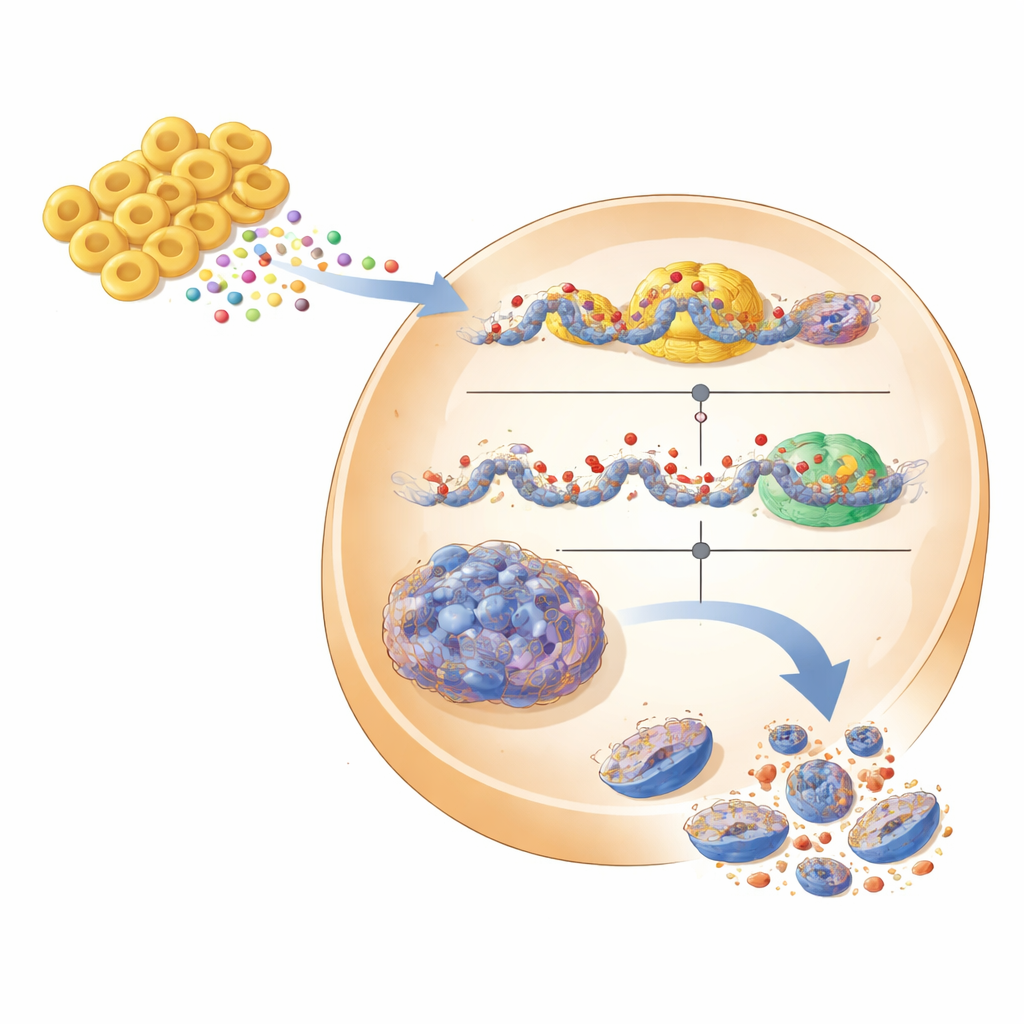
Dai modelli di laboratorio verso terapie future
Per avvicinarsi a condizioni più realistiche, il team ha testato le loro idee in sfere tumorali tridimensionali, che imitano meglio i tumori solidi, e in topi portatori di innesti umani di carcinoma renale. Nelle sfere, il silenziamento di EHMT2, il trattamento con l'inibitore o l'aggiunta del soprannatante Fb7-311 causarono lo scioglimento delle masse tumorali compatte, accompagnato da DDIT3 aumentato e segnali di morte cellulare più intensi. Nei topi, l'inibitore di EHMT2 ridusse le dimensioni dei tumori senza perdita di peso evidente o tossicità importante, e i tumori trattati mostrarono più DDIT3. Pur rimanendo molti ostacoli—come dimostrare che Fb7-311 possa colonizzare i pazienti in modo sicuro, che produca gli stessi metaboliti nell'intestino umano e che questi raggiungano il rene intatti—il lavoro delinea un percorso convincente. Pone EHMT2 come un promettente bersaglio molecolare nel carcinoma a cellule renali e suggerisce che un probiotico su misura o i suoi metaboliti purificati potrebbero un giorno affiancare i farmaci per attivare i programmi di morte intrinseci nei tumori renali.
Citazione: Lee, J., Lee, J., Tae, I.H. et al. Gut microbiota modulation of epigenetic target EHMT2: Lacticaseibacillus rhamnosus Fb7-311 regulated renal cell carcinoma apoptosis and metastasis. Exp Mol Med 58, 739–754 (2026). https://doi.org/10.1038/s12276-026-01659-6
Parole chiave: carcinoma renale, terapia epigenetica, microbioma intestinale, trattamento oncologico probiotico, indolo-3-carbinolo