Clear Sky Science · fr
Modulation du microbiote intestinal de la cible épigénétique EHMT2 : Lacticaseibacillus rhamnosus Fb7-311 régule l’apoptose et les métastases du carcinome rénal
Pourquoi votre intestin pourrait avoir de l’importance pour le cancer du rein
Les chercheurs découvrent des liens surprenants entre les bactéries vivant dans nos intestins et des cancers situés dans des organes distants. Cette étude explore comment un microbe intestinal spécifique et un « interrupteur » moléculaire à l’intérieur des cellules du cancer rénal coopèrent pour contrôler si les tumeurs croissent ou s’autodétruisent. Comprendre cette connexion pourrait ouvrir la voie à de nouveaux traitements combinant des médicaments de précision et des probiotiques choisis avec soin.
Un cancer rénal mortel qui a besoin de nouvelles options
Le carcinome rénal est la forme la plus courante de cancer du rein et est souvent mortel une fois qu’il s’est propagé au-delà du rein. La chirurgie, la radiothérapie, les immunothérapies et les médicaments ciblés aident certains patients, mais beaucoup ont encore un pronostic défavorable, surtout lorsque la maladie a déjà métastasé. Les auteurs se sont concentrés sur une protéine intracellulaire, appelée EHMT2, qui participe au compactage de l’ADN et à la répression de certains gènes. En analysant de grands jeux de données publics sur le cancer et des échantillons de tissus de patients, ils ont constaté que les tumeurs rénales produisent beaucoup plus d’EHMT2 que le tissu rénal normal, et que les patients présentant des niveaux élevés de cette protéine tendent à avoir une survie plus courte.
Activer l’interrupteur de mort à l’intérieur des cellules tumorales
Pour déterminer ce que fait réellement EHMT2 dans le cancer rénal, l’équipe a réduit ses niveaux dans deux lignées cellulaires humaines de cancer rénal en utilisant des outils génétiques et un inhibiteur de petite molécule connu sous le nom de BIX-01294. Dans les deux cas, le blocage d’EHMT2 a ralenti la croissance cellulaire, déclenché le suicide cellulaire (apoptose) et réduit la capacité des cellules cancéreuses à migrer et envahir, comportements liés aux métastases. Les chercheurs ont relié ces effets à une autre protéine, DDIT3, normalement maintenue à bas niveau mais capable de pousser les cellules vers la mort programmée lorsqu’elle est activée en situation de stress. Ils ont montré qu’EHMT2 marque chimiquement le conditionnement de l’ADN proche du gène DDIT3 de façon à le maintenir éteint ; lorsque EHMT2 est éliminé ou inhibé, ces marques s’estompent, les niveaux de DDIT3 augmentent et les cellules cancéreuses sont poussées vers l’autodestruction.
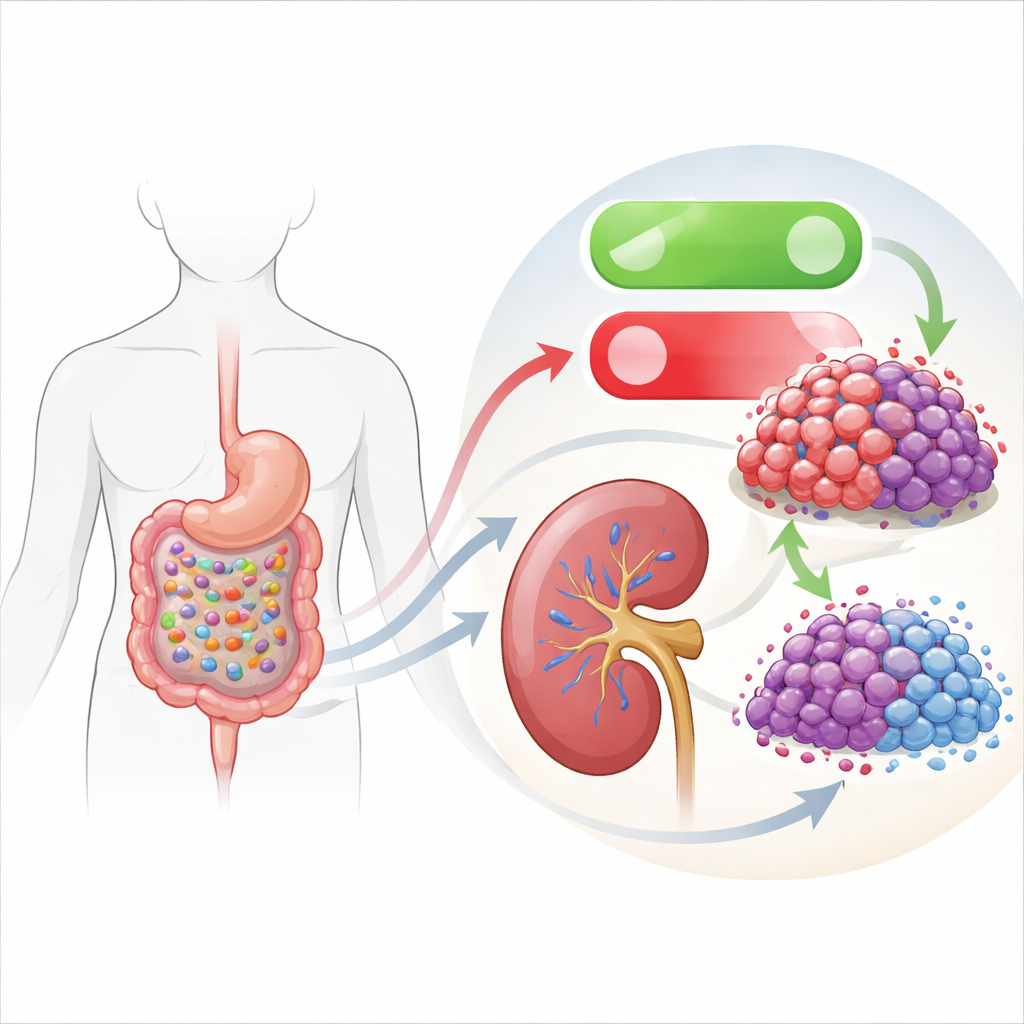
Comment une bactérie intestinale mime un médicament de précision
La partie la plus intrigante du travail relie cet interrupteur de mort interne au microbiote intestinal. L’équipe a criblé des bouillons de culture issus de diverses bactéries intestinales et a découvert que le liquide d’une souche appelée Lacticaseibacillus rhamnosus Fb7-311 ralentissait fortement la croissance des cellules de cancer rénal. Lorsque les cellules tumorales ont été exposées à ce surnageant bactérien, elles ont présenté le même schéma observé avec l’inhibition directe d’EHMT2 : moins d’EHMT2, plus de DDIT3, davantage de signes biochimiques d’apoptose et moins de migration et d’invasion. Les auteurs ont confirmé que les marques chimiques près du gène DDIT3 étaient réduites, indiquant que les produits bactériens desserraient indirectement l’emprise d’EHMT2 sur ce gène clé promoteur de la mort.
Se concentrer sur une molécule microbienne anticancéreuse
Pour identifier ce qui, dans le bouillon bactérien, en était responsable, les chercheurs ont réalisé un profilage chimique détaillé du surnageant et l’ont recoupé avec des études antérieures sur les métabolites anticancéreux. Ils ont réduit la liste à six candidats et les ont testés individuellement sur des cellules de cancer rénal. Un composé, l’indole-3-carbinol — molécule déjà connue présente dans les crucifères et certaines voies microbiennes — s’est distingué. Il n’a pas seulement supprimé la croissance cellulaire, il a aussi diminué les niveaux d’EHMT2 et augmenté ceux de DDIT3, reproduisant le motif moléculaire central déclenché par la bactérie elle‑même. Cela suggère que l’indole-3-carbinol, produit par Fb7-311, pourrait être un messager clé qui reprogramme les cellules tumorales vers la mort via des changements épigénétiques.
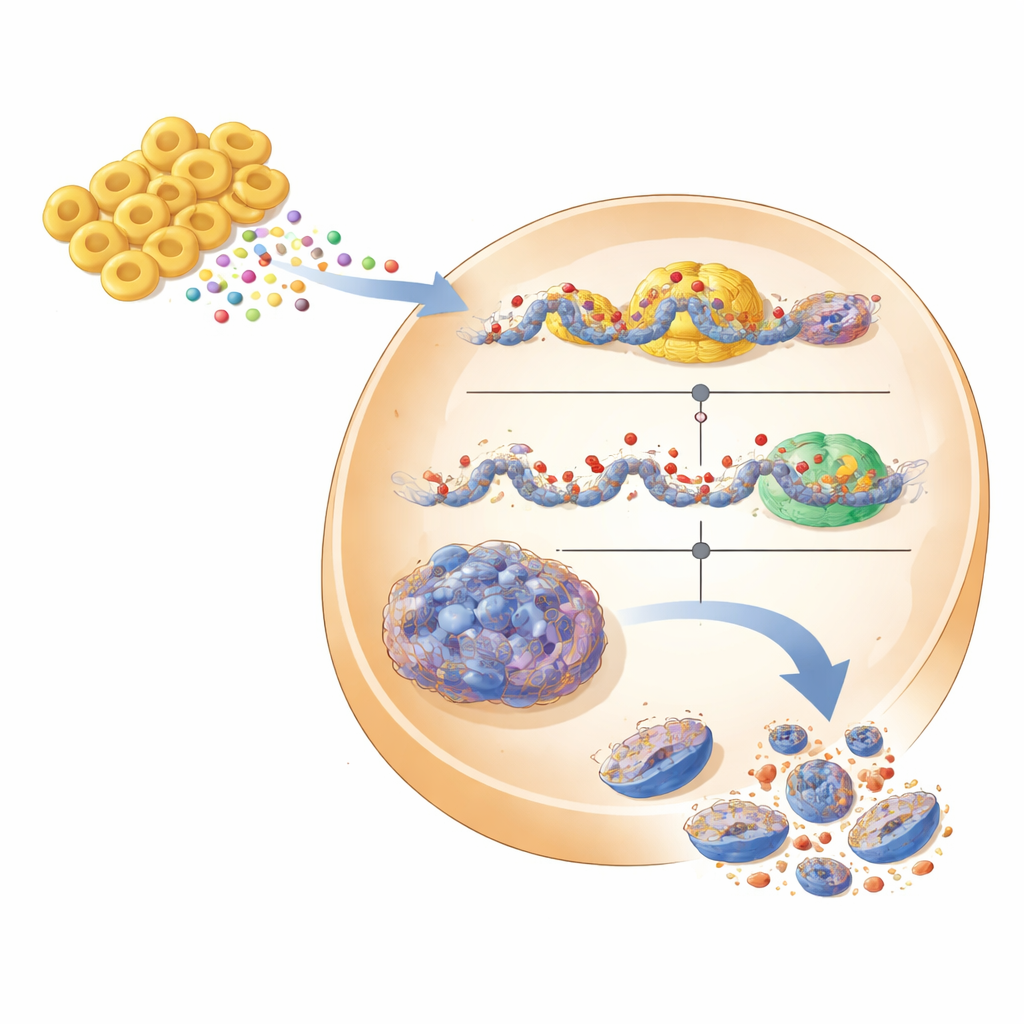
Des modèles de laboratoire vers des thérapies futures
Pour se rapprocher de conditions réelles, l’équipe a testé ses hypothèses dans des sphéroïdes tumoraux tridimensionnels, qui reproduisent mieux les tumeurs solides, et chez des souris porteuses de greffons de cancer rénal humain. Dans les sphéroïdes, l’inhibition d’EHMT2, le traitement par l’inhibiteur ou l’ajout du surnageant Fb7-311 ont tous conduit à la désintégration des amas tumoraux compacts, accompagnée d’une augmentation de DDIT3 et d’un renforcement des signaux de mort cellulaire. Chez la souris, l’inhibiteur d’EHMT2 a réduit la taille des tumeurs sans perte de poids évidente ni toxicité majeure, et les tumeurs traitées présentaient davantage de DDIT3. Bien que de nombreux obstacles restent à franchir — comme prouver que Fb7-311 peut coloniser les patients en toute sécurité, qu’il produit les mêmes métabolites dans l’intestin humain et que ceux-ci atteignent le rein intacts — cette étude décrit une voie convaincante. Elle positionne EHMT2 comme une cible moléculaire prometteuse dans le carcinome rénal et suggère qu’un probiotique sur mesure ou ses métabolites purifiés pourraient un jour compléter les médicaments pour déclencher les programmes de mort intrinsèques des tumeurs rénales.
Citation: Lee, J., Lee, J., Tae, I.H. et al. Gut microbiota modulation of epigenetic target EHMT2: Lacticaseibacillus rhamnosus Fb7-311 regulated renal cell carcinoma apoptosis and metastasis. Exp Mol Med 58, 739–754 (2026). https://doi.org/10.1038/s12276-026-01659-6
Mots-clés: carcinome rénal, thérapie épigénétique, microbiome intestinal, traitement probiotiques du cancer, indole-3-carbinol