Clear Sky Science · es
Modulación de la microbiota intestinal del objetivo epigenético EHMT2: Lacticaseibacillus rhamnosus Fb7-311 reguló la apoptosis y la metástasis del carcinoma de células renales
Por qué tu intestino podría importar para el cáncer de riñón
Investigadores están descubriendo vínculos sorprendentes entre las bacterias que viven en nuestros intestinos y los cánceres en órganos distantes. Este estudio explora cómo un microbio intestinal concreto y un "interruptor" molecular dentro de las células del cáncer de riñón actúan conjuntamente para controlar si los tumores crecen o se autodestruyen. Comprender esta conexión podría abrir la puerta a nuevos tratamientos que combinen fármacos de precisión con probióticos seleccionados con cuidado.
Un cáncer renal letal que necesita nuevas opciones
El carcinoma de células renales es la forma más común de cáncer de riñón y con frecuencia resulta mortal una vez que se disemina fuera del riñón. La cirugía, la radiación, las inmunoterapias y los fármacos dirigidos ayudan a algunos pacientes, pero muchos siguen afrontando un pronóstico desfavorable, especialmente cuando la enfermedad ya ha metastatizado. Los autores se centraron en una proteína dentro de las células, llamada EHMT2, que ayuda a compactar el ADN y silenciar ciertos genes. Al analizar grandes conjuntos de datos públicos sobre cáncer y muestras de tejido de pacientes, encontraron que los tumores renales producen mucho más EHMT2 que el tejido renal normal, y que los pacientes con niveles más altos de esta proteína tienden a tener una supervivencia más corta.
Activar el interruptor de la muerte dentro de las células tumorales
Para ver qué hace realmente EHMT2 en el cáncer renal, el equipo redujo sus niveles en dos líneas celulares humanas de cáncer renal usando herramientas genéticas y un inhibidor de pequeña molécula conocido como BIX-01294. En ambos casos, bloquear EHMT2 ralentizó el crecimiento celular, desencadenó la autodestrucción celular (apoptosis) y redujo la capacidad de las células cancerosas para desplazarse e invadir, comportamientos relacionados con la metástasis. Los investigadores atribuyeron estos efectos a otra proteína, DDIT3, que normalmente se mantiene baja pero puede empujar a las células hacia la muerte programada cuando se activa bajo estrés. Mostraron que EHMT2 marca químicamente el empaquetamiento del ADN cerca del gen DDIT3 de una forma que lo mantiene apagado; cuando EHMT2 se elimina o inhibe, esas marcas disminuyen, los niveles de DDIT3 aumentan y las células cancerosas se encaminan hacia la autodestrucción.
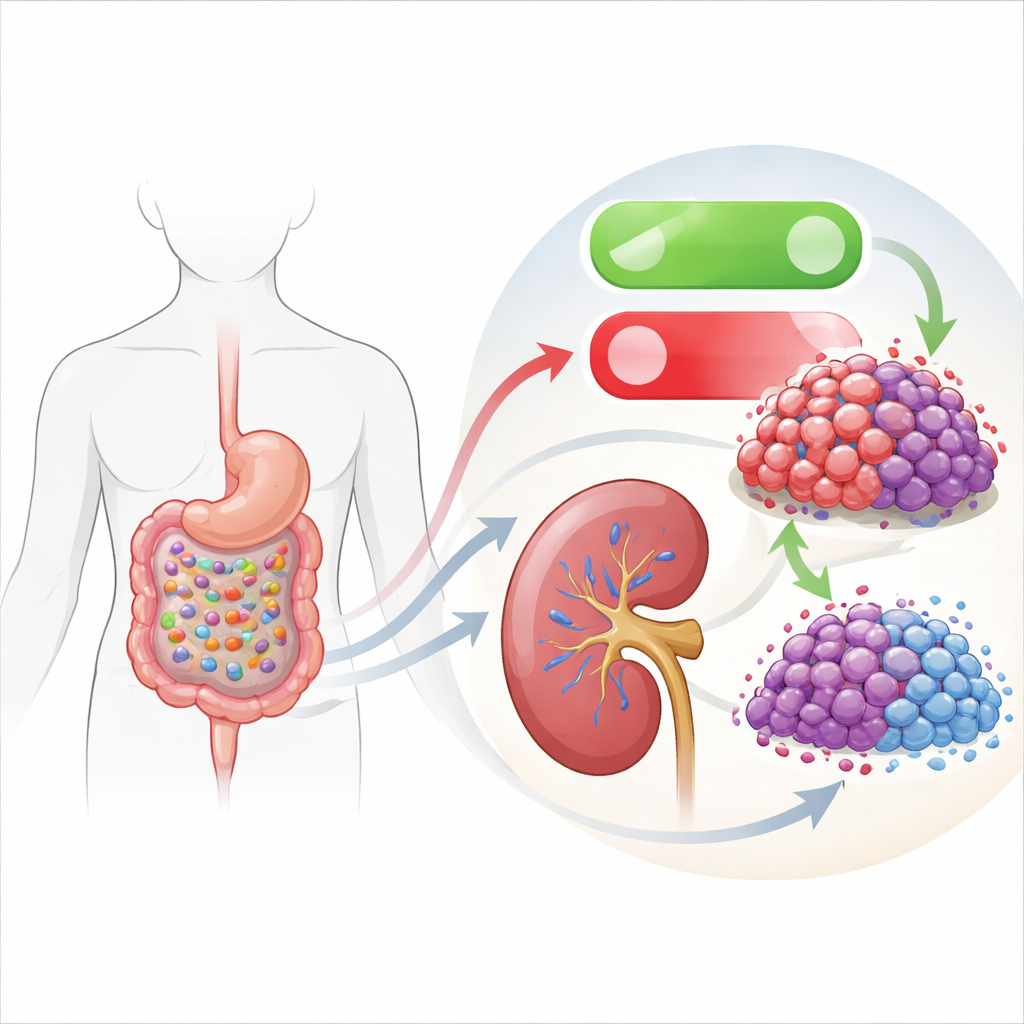
Cómo una bacteria intestinal imita a un fármaco de precisión
La parte más intrigante del trabajo conecta este interruptor interno de muerte con la microbiota intestinal. El equipo cribó caldos de cultivo de varias bacterias intestinales y descubrió que el líquido de una cepa llamada Lacticaseibacillus rhamnosus Fb7-311 ralentizaba con fuerza el crecimiento de las células del cáncer renal. Cuando las células tumorales se expusieron a este sobrenadante bacteriano, mostraron el mismo patrón observado con la inhibición directa de EHMT2: menor EHMT2, mayor DDIT3, más señales bioquímicas de apoptosis y menos migración e invasión. Los autores confirmaron que las marcas químicas cerca del gen DDIT3 estaban reducidas, lo que indica que los productos bacterianos aflojaban indirectamente el control de EHMT2 sobre este gen clave promotor de la muerte.
Detrás de la molécula microbiana que combate el cáncer
Para identificar qué había en el caldo bacteriano que era responsable, los investigadores realizaron un perfil químico detallado del sobrenadante y lo cotejaron con estudios previos sobre metabolitos anticancerígenos. Redujeron la lista a seis candidatos y los probaron individualmente en células de cáncer renal. Un compuesto, el indol-3-carbinol —una molécula ya conocida por su presencia en vegetales crucíferos y en algunas vías microbianas— destacó. No solo suprimió el crecimiento celular, sino que también redujo los niveles de EHMT2 y aumentó DDIT3, reproduciendo el patrón molecular central desencadenado por la propia bacteria. Esto sugiere que el indol-3-carbinol, producido por Fb7-311, podría ser un mensajero clave que reprograme las células tumorales hacia la muerte mediante cambios epigenéticos.
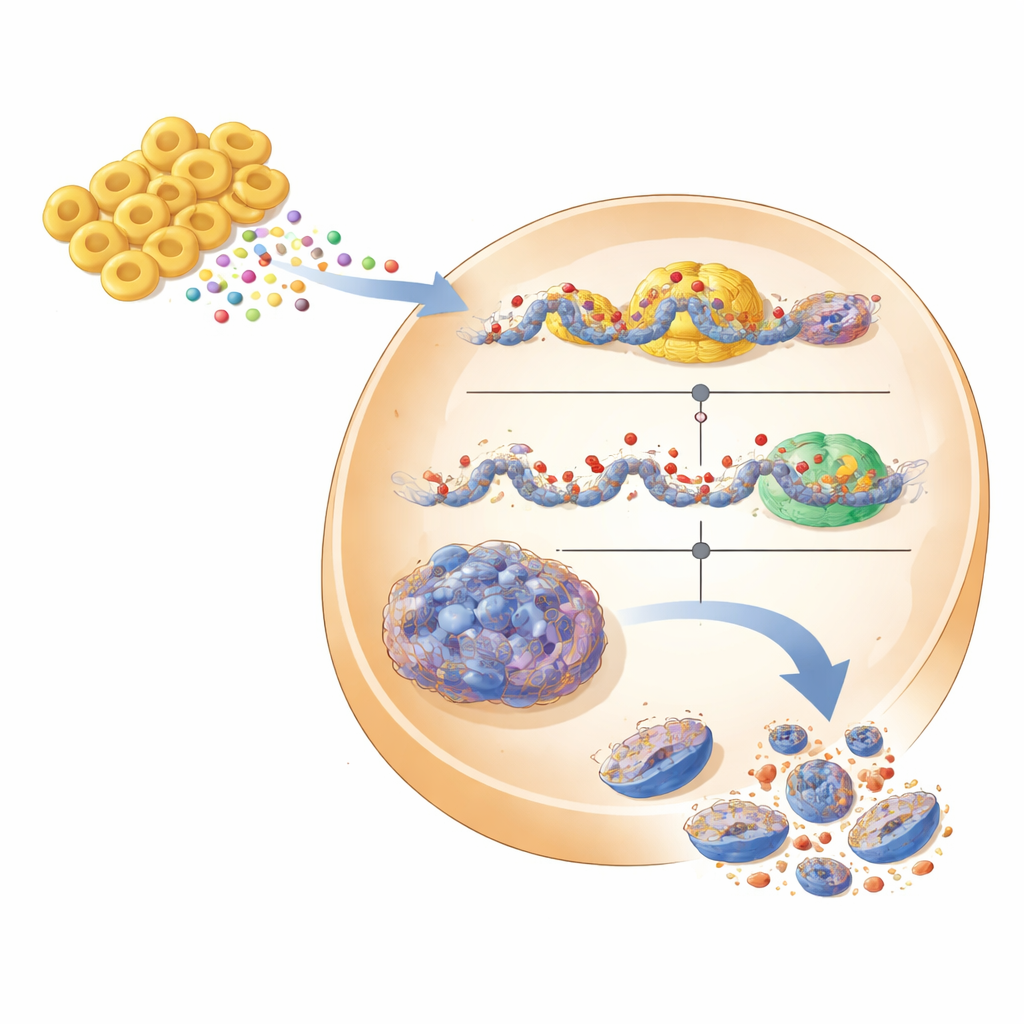
De los modelos de laboratorio hacia futuras terapias
Para acercarse a condiciones más realistas, el equipo probó sus ideas en esferoides tumorales tridimensionales, que imitan mejor los tumores sólidos, y en ratones con injertos de cáncer renal humano. En los esferoides, disminuir EHMT2, tratar con el inhibidor o añadir el sobrenadante de Fb7-311 provocó que las esferas tumorales compactas se desintegraran, acompañado de un aumento de DDIT3 y señales de muerte celular más intensas. En ratones, el inhibidor de EHMT2 redujo el tamaño de los tumores sin pérdida de peso evidente ni toxicidad mayor, y los tumores tratados mostraron más DDIT3. Aunque quedan muchos obstáculos —como demostrar que Fb7-311 puede colonizar a los pacientes de forma segura, que produce los mismos metabolitos en el intestino humano y que estos alcanzan el riñón intactos—, el trabajo traza una vía convincente. Sitúa a EHMT2 como un objetivo molecular prometedor en el carcinoma de células renales y sugiere que un probiótico a medida o sus metabolitos purificados podrían algún día complementar los fármacos para activar los programas internos de muerte en los tumores renales.
Cita: Lee, J., Lee, J., Tae, I.H. et al. Gut microbiota modulation of epigenetic target EHMT2: Lacticaseibacillus rhamnosus Fb7-311 regulated renal cell carcinoma apoptosis and metastasis. Exp Mol Med 58, 739–754 (2026). https://doi.org/10.1038/s12276-026-01659-6
Palabras clave: carcinoma de células renales, terapia epigenética, microbioma intestinal, tratamiento oncológico con probióticos, indol-3-carbinol