Clear Sky Science · pl
Modulacja przez mikrobiotę jelitową epigenetycznego celu EHMT2: Lacticaseibacillus rhamnosus Fb7-311 regulował apoptozę i przerzuty raka nerkowokomórkowego
Dlaczego twoje jelita mogą mieć znaczenie dla raka nerki
Naukowcy odkrywają zaskakujące powiązania między bakteriami żyjącymi w naszych jelitach a nowotworami w odległych narządach. W tym badaniu zbadano, jak konkretny mikroorganizm jelitowy i molekularny „wyłącznik” wewnątrz komórek raka nerki współdziałają, aby kontrolować, czy guzy rosną, czy ulegają samozniszczeniu. Zrozumienie tego połączenia może otworzyć drogę do nowych terapii łączących precyzyjne leki z celowo dobranymi probiotykami.
Śmiertelny rak nerki, który potrzebuje nowych opcji
Rak nerkowokomórkowy jest najczęstszą postacią raka nerki i często bywa śmiertelny, gdy rozszerzy się poza nerkę. Chirurgia, radioterapia, terapie immunologiczne i leki ukierunkowane pomagają niektórym pacjentom, ale wielu wciąż stoi w obliczu niekorzystnego rokowania, szczególnie gdy choroba już dała przerzuty. Autorzy skupili się na białku wewnątrz komórek, zwanym EHMT2, które pomaga ciasniej upakować DNA i wyciszać wybrane geny. Analizując duże publiczne zbiory danych o raku oraz próbki tkanek od pacjentów, stwierdzili, że guzy nerkowe wytwarzają znacznie więcej EHMT2 niż normalna tkanka nerkowa, a pacjenci z wyższym poziomem tego białka mają zwykle krótsze przeżycie.
Przełączanie wewnętrznego wyłącznika śmierci w komórkach guza
Aby sprawdzić, co EHMT2 faktycznie robi w raku nerki, zespół obniżył jego poziom w dwóch ludzkich liniach komórek raka nerkowego, używając narzędzi genetycznych oraz małocząsteczkowego inhibitora znanego jako BIX-01294. W obu przypadkach blokada EHMT2 spowalniała wzrost komórek, uruchamiała samobójczą śmierć komórkową (apoptozę) i zmniejszała zdolność komórek nowotworowych do przemieszczania się i inwazji — zachowania powiązane z przerzutami. Naukowcy powiązali te efekty z innym białkiem, DDIT3, które normalnie utrzymywane jest na niskim poziomie, ale może skierować komórki ku zaprogramowanej śmierci, gdy zostanie aktywowane pod wpływem stresu. Pokazali, że EHMT2 chemicznie znakował opakowanie DNA w rejonie genu DDIT3 w sposób utrzymujący go w stanie wyciszenia; kiedy EHMT2 jest usunięte lub zahamowane, te znaki znikają, poziom DDIT3 rośnie, a komórki nowotworowe zostają popchnięte ku samozagładzie.
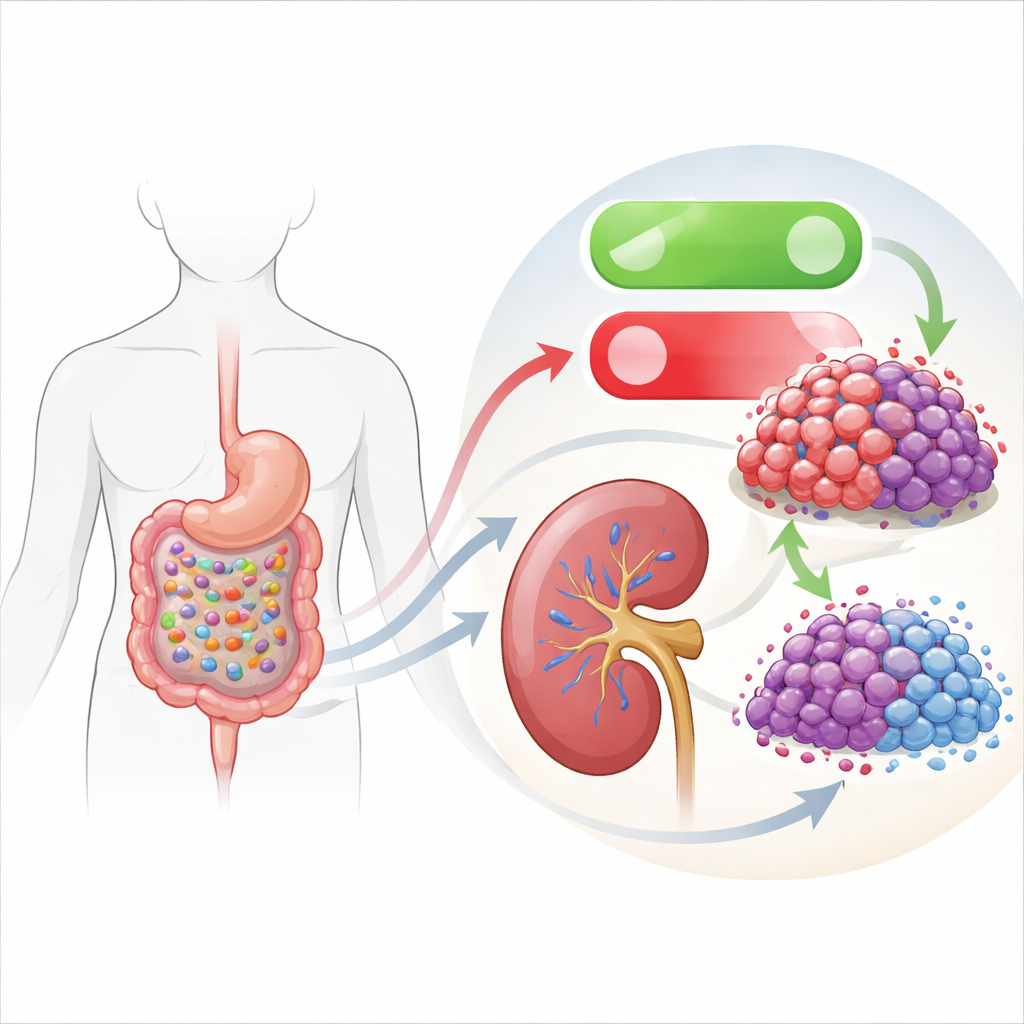
Jak bakteria jelitowa naśladuje lek precyzyjny
Najbardziej intrygująca część pracy łączy ten wewnętrzny wyłącznik śmierci z mikrobiotą jelitową. Zespół przesiał pożywki hodowlane od różnych bakterii jelitowych i odkrył, że płyn z szczepu Lacticaseibacillus rhamnosus Fb7-311 silnie spowalnia wzrost komórek raka nerki. Gdy komórki nowotworowe były wystawione na działanie tego supernatantu bakteryjnego, wykazywały ten sam wzorzec co przy bezpośredniej inhibicji EHMT2: niższe EHMT2, wyższe DDIT3, więcej biochemicznych oznak apoptozy oraz mniejsza migracja i inwazja. Autorzy potwierdzili, że chemiczne znaki w rejonie genu DDIT3 zostały zmniejszone, co wskazuje, że produkty bakteryjne pośrednio rozluźniają kontrolę EHMT2 nad tym kluczowym genem promującym śmierć.
Skupienie się na molekule mikrobiologicznej walczącej z rakiem
Aby ustalić, co w hodowli bakteryjnej było odpowiedzialne za efekt, badacze przeprowadzili szczegółowe profilowanie chemiczne supernatantu i porównali je z wcześniejszymi badaniami nad metabolitami o działaniu przeciwnowotworowym. Zawęzili listę do sześciu kandydatów i przetestowali je indywidualnie na komórkach raka nerki. Jeden związek, indol-3-karbinol — molekuła już znana z warzyw kapustnych i niektórych ścieżek mikrobiologicznych — wyróżnił się. Nie tylko hamował wzrost komórek, ale również obniżał poziomy EHMT2 i podwyższał DDIT3, odtwarzając podstawowy wzorzec molekularny wywoływany przez bakterię. Sugeruje to, że indol-3-karbinol produkowany przez Fb7-311 może być kluczowym przekaźnikiem, który przez zmiany epigenetyczne przeprogramowuje komórki guza w kierunku śmierci.
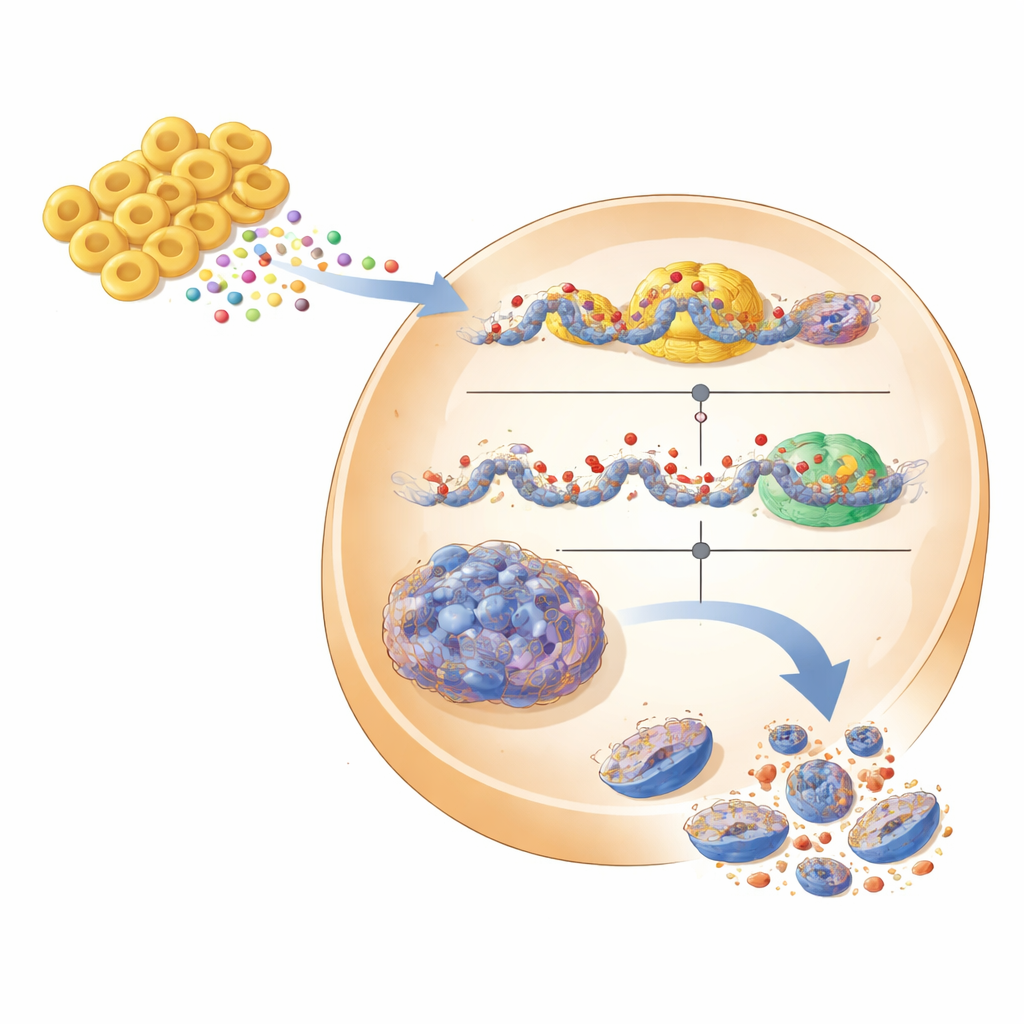
Od modeli laboratoryjnych ku przyszłym terapiom
Aby zbliżyć się do warunków rzeczywistych, zespół przetestował swoje hipotezy w trójwymiarowych sferoidach nowotworowych, które lepiej naśladują guzy lite, oraz u myszy z przeszczepami ludzkiego raka nerki. W sferoidach zmniejszenie EHMT2, leczenie inhibitorem lub dodanie supernatantu Fb7-311 spowodowały rozpad zwartych kul nowotworowych, któremu towarzyszyły wyższe poziomy DDIT3 i silniejsze sygnały śmierci komórkowej. U myszy inhibitor EHMT2 zmniejszał guzy bez widocznej utraty masy ciała czy większej toksyczności, a leczone guzy wykazywały więcej DDIT3. Choć pozostaje wiele przeszkód — jak udowodnienie, że Fb7-311 może bezpiecznie skolonizować pacjentów, że produkuje te same metabolity w ludzkim jelicie i że docierają one do nerki w nienaruszonej formie — praca wyznacza przekonującą ścieżkę. Pozycjonuje EHMT2 jako obiecujący cel molekularny w raku nerkowokomórkowym i sugeruje, że dopasowany probiotyk lub jego oczyszczone metabolity mogłyby pewnego dnia uzupełniać leki, aby uruchamiać wbudowane programy śmierci w guzach nerkowych.
Cytowanie: Lee, J., Lee, J., Tae, I.H. et al. Gut microbiota modulation of epigenetic target EHMT2: Lacticaseibacillus rhamnosus Fb7-311 regulated renal cell carcinoma apoptosis and metastasis. Exp Mol Med 58, 739–754 (2026). https://doi.org/10.1038/s12276-026-01659-6
Słowa kluczowe: rak nerkowokomórkowy, terapia epigenetyczna, mikrobiom jelitowy, probiotyczne leczenie raka, indol-3-karbinol