Clear Sky Science · tr
Eşzamanlı mekânsal transkriptomik ve morfoloji profillemesi: mikroglianın yaşla nasıl değiştiğini keşfetme araçları
Yaşlandıkça Beyin Bağışıklık Hücrelerinin Önemi
Yaşlandıkça beynimiz sadece nöronlarını kaybetmez; onları çevreleyen destek ve bağışıklık hücreleri de bellek, ruh hali ve hastalıklara yatkınlığı etkileyebilecek ince değişiklikler geçirir. Bu çalışma, beynin yerel bağışıklık hücreleri olan mikrogliaları ele alıyor ve görünüşte basit bir soruyu soruyor: bu hücrelerin ince dallanma yapısı ve genetik mesajlarının hücre içindeki konumlanması yaşla nasıl değişiyor? Güçlü görüntüleme ve gen-okuma araçlarını birleştirerek yazarlar, belirli moleküllerin mikroglia içinde nerede bulunduğunun hücrenin şekli ve davranışını etkileyebileceğini ve bu mekânsal düzenin yaşam boyunca yeniden şekillendiğini gösteriyor.
Yaşlanan Beynin İçine Bakmak
Bu soruları incelemek için araştırmacılar, genç yetişkin farelerin (insan karşılığında erken yetişkinlik) ve çok yaşlı farelerin beyin dilimlerini incelediler. Yüzlerce farklı RNA molekülünü—genlerin çalışan kopyalarını—neredeyse tek molekül çözünürlüğünde tespit etmek için MERFISH adlı görüntüleme yöntemini kullanırken, eşzamanlı olarak mikrogliaları boyadılar, böylece her hücrenin dış hattı ve dallanma deseni yakalanabildi. Bu yöntem, yedi beyin bölgesinde 3.900’den fazla bireysel mikroglianın haritalanmasına imkan verdi; her hücrenin ayrıntılı şeklini gen etkinliğiyle ve transkriptlerin kalın merkezi gövdesi ile ince, ağaç benzeri uzantıları içindeki kesin konumlarıyla ilişkilendirdiler. 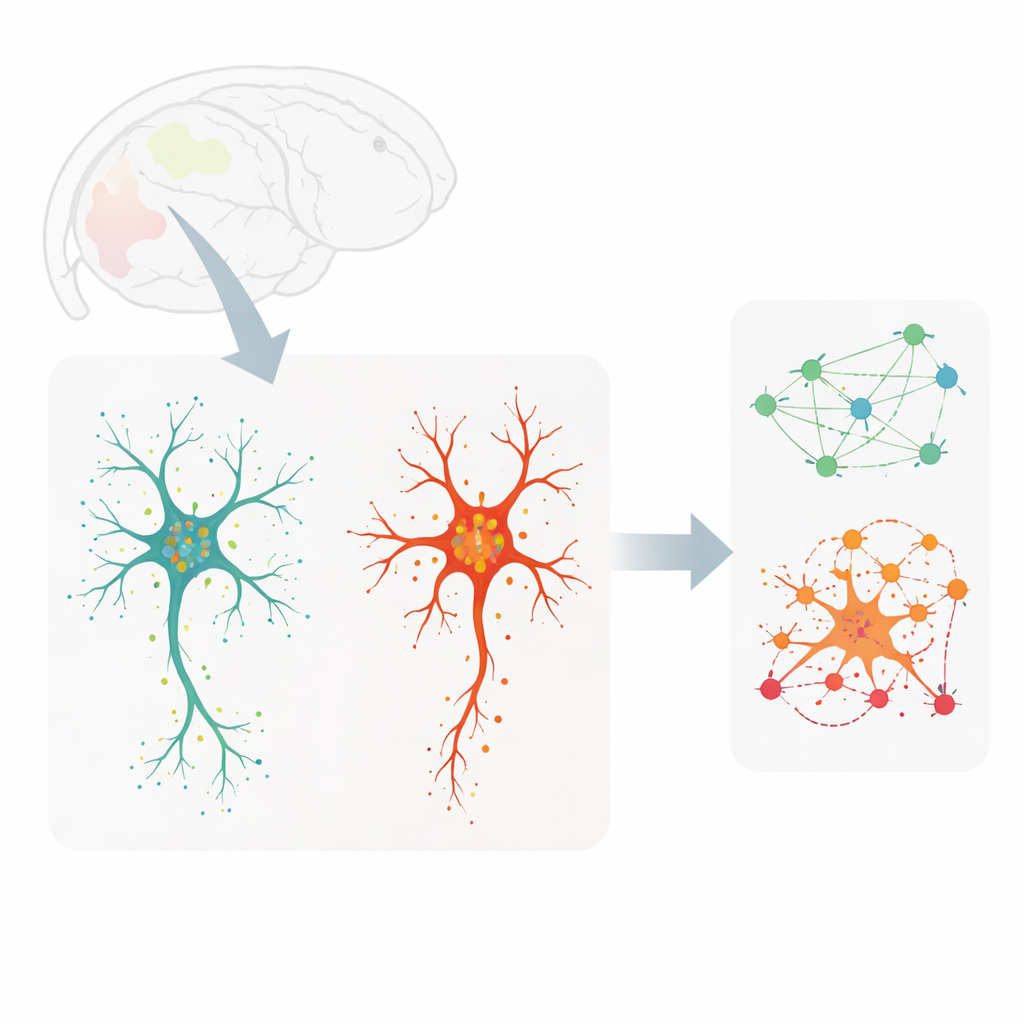
Şekiller ve Durumlar Her Zaman Uyumlu Değil
Geleneksel olarak mikroglialar iki geniş sınıfa ayrılır: beyni sessizce tarayan çok dallı (ramifiye) hücreler ve “aktif” ya da hastalıkla ilişkili olduğu düşünülen daha yuvarlak, amöboid hücreler. Yeni haritalar bu öyküyü karmaşıklaştırıyor. Ekip mikrogliaları gen ekspresyon profillerine göre kümelediğinde üç ana grup buldu: homeostatik, geçişte olan ve hastalıkla ilişkili-benzeri hücreler. Ayrı olarak, hücreleri yalnızca şekle göre—bir sinir ağı ve onlarca geometrik ölçüm kullanarak—kümelediklerinde, en az dallı olandan en çok dallı olana doğru kesintisiz bir spektrum ortaya çıktı. İkisini karşılaştırmak şaşırtıcı bir uyumsuzluğu ortaya koydu. Bazı hastalıkla ilişkili-benzeri hücreler geniş dallanmalarını korurken, bazı görünüşte “dinlenen” hücreler daha amöboid görünüyordu. Bu da bir mikroglial hücrenin ne yaptığını yalnızca dış hatlarından güvenilir şekilde çıkaramayacağımız anlamına geliyor.
Dallanmayla Eşleşen Genetik Mesajlar
Daha derine inmek için yazarlar belirli genlerin mikroglial geometriyle nasıl ilişkili olduğunu incelediler. Hücre alanı, dal uçlarının sayısı ve dallanma desenlerinin karmaşıklığı gibi özelliklerle güçlü şekilde korele olan gen setlerini tanımladılar. Özellikle, glutamat nörotransmitterini işleyen birkaç gen, taşınma geni Slc1a2 dahil, çok dallı hücrelerde daha aktifti ve RNA molekülleri uzantılar boyunca uzanıyordu. İç veziküller ve madde yutumu ile ilişkilendirilen gövdeye bağlı diğer genler ise soma boyutu ve kompaktlığıyla ilişki gösterdi. Transkriptleri merkezi gövde veya uzantılarla zenginleşenlere odaklanarak, ekibin süreçlere lokalize genlerin özellikle bilgilendirici olduğunu gösterdi: yalnızca bunları kullanarak bir makine öğrenmesi modeli dallı ile amöboid mikrogliaları iyi bir doğrulukla ayırt edebiliyordu. 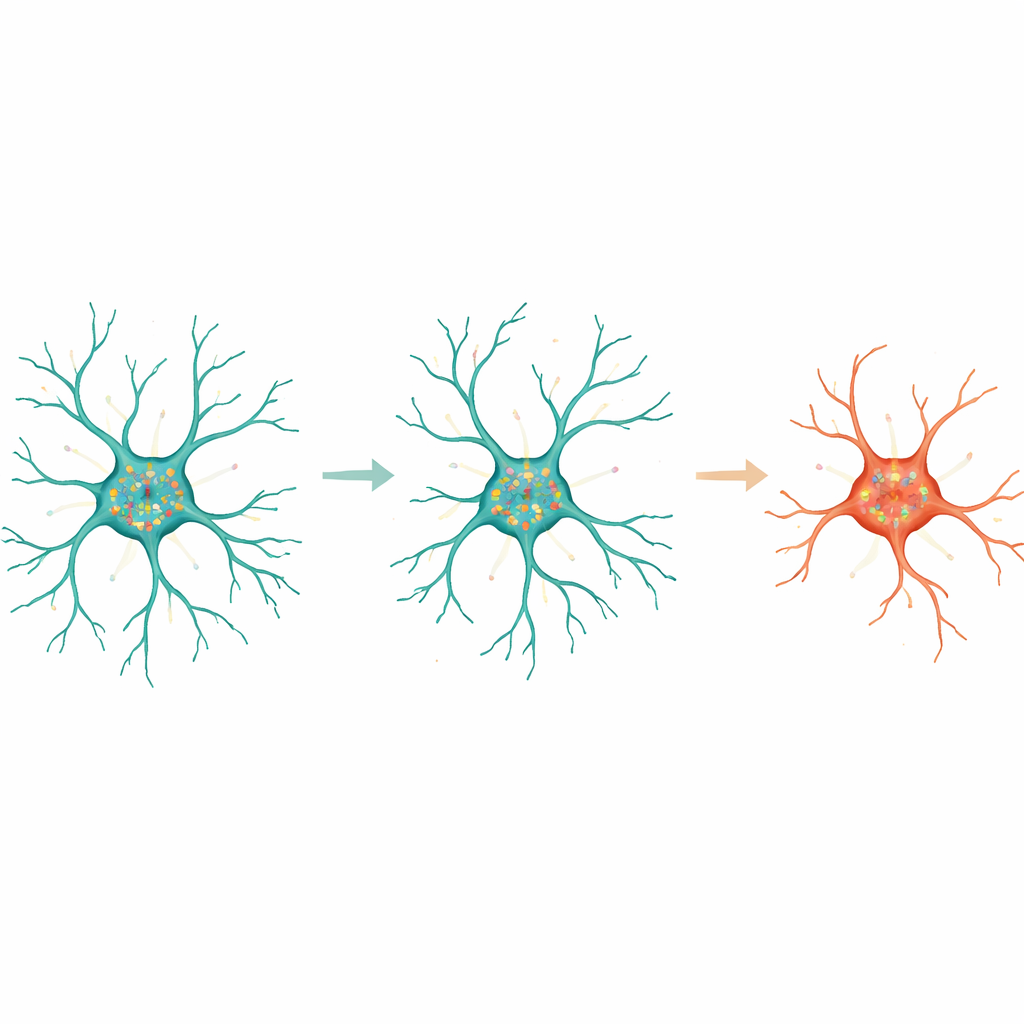
Yaşlanma İç Organizasyonu Nasıl Yeniden Düzenliyor
Yaşın eklediği bir başka unsur daha vardı. Genç farelerin ramifiye mikroglialarında birçok gen ya soma ya da uzantılar için belirgin tercih gösteriyordu ve transkriptleri genellikle enerji yönetimi veya sinaps budaması gibi eşgüdümlü işlevleri düşündüren desenler içinde kümeleniyordu. Yaşlı farelerde güçlü şekilde bölümlenmiş genlerin sayısı azaldı ve birbirine yakın duran transkript ağları daha seyrek ve vurgu bakımından farklı hale geldi. Genç hücrelerde somada sıkı şekilde birlikte lokalize RNA’lar sitokin üretimi ve metabolik kontrolle ilişkilendiriliyken, yaşlı hücrelerde göç ve hücresel artıkların uzaklaştırılmasına kaydı. Uzantılarda, genç mikroglialar yerel protein yönetimi ve sinaps rafinasyonu ile ilişkili ağlar gösterirken, yaşlı mikroglialar madde alımı ve parçalanmasına doğru eğilim gösterdi. Yaşla birlikte bu basitleşmeye rağmen, Slc1a2 ve Pink1 dahil süreçlere lokalize çekirdek bir gen grubu, bir hücrenin ne kadar dallı olacağını tahmin etmede hâlâ anahtar kaldı.
Bu, Beyin Sağlığı İçin Ne Anlama Geliyor
Bir araya getirildiğinde bu çalışma, mikroglia içindeki RNA moleküllerinin iç coğrafyasının rastgele olmadığını gösteriyor: bu coğrafya hücrelerin nasıl şekillendiğini ve ne yaptıklarını tanımlamaya yardımcı oluyor ve beyin yaşlandıkça yeniden şekilleniyor. “Aktive olmuş” mikroglianın mutlaka yuvarlak ve küt göründüğü klasik tablo artık geçerli değil; bunun yerine işlev, şekil ve moleküler durum kısmen birbirinden ayrılabiliyor. Genel okuyucu için ana mesaj, beyin bağışıklık hücrelerinin ders kitaplarındaki portrelerinden çok daha çeşitli ve uyarlanabilir olduğudur. Mesajların nerede konumlandığı ve kiminle kümelendiği gibi iç lojistiklerinin yaşla nasıl değiştiğini öğrenerek, bilim insanları nihayetinde mikrogliaları yaşlanan beyni dejenerasyon ve hastalıklardan daha iyi koruyan hallere yönlendirebilecek yollar bulabilirler.
Atıf: Henze, D.E., Tsai, A.P., Wyss-Coray, T. et al. Simultaneous spatial transcriptomics and morphology profiling as tools to explore how microglia change with age. Nat Aging 6, 869–885 (2026). https://doi.org/10.1038/s43587-026-01089-z
Anahtar kelimeler: mikroglia, beyin yaşlanması, mekânsal transkriptomik, hücre morfolojisi, nöroenflamasyon