Clear Sky Science · ja
空間トランスクリプトミクスと形態解析を同時に行うことで、マイクログリアが加齢とともにどう変わるかを探る手法
加齢に伴い脳の免疫細胞が重要である理由
年を重ねると脳は単にニューロンを失うだけではなく、それらを取り巻く支持細胞や免疫細胞も微妙に変化し、記憶や気分、病気への脆弱性に影響を与えます。本研究は脳に常在する免疫細胞であるマイクログリアに注目し、一見単純な問いを立てます:これらの細胞の精緻な構造と遺伝情報の細胞内での配置は、加齢とともにどのように変わるのか?強力なイメージングと遺伝子検出の手法を組み合わせることで、著者らは重要な分子がマイクログリアのどこに存在するかがその形態や挙動に影響を与え、こうした空間的配置が寿命にわたって再編されることを示しています。
老化する脳の内部を覗く
この問いを調べるために、研究者たちは若年成人マウス(人間でいう早期成人期に相当)と非常に高齢のマウスの脳スライスを解析しました。MERFISHと呼ばれるイメージング手法を用い、数百種類のRNA分子(遺伝子の動作コピー)をほぼ単一分子分解能で検出すると同時に、マイクログリアを染色して各細胞の輪郭や枝分かれパターンを捉えました。これにより、7つの脳領域にわたって3,900を超える個々のマイクログリアをマッピングし、各細胞の詳細な形状を遺伝子活動や太い中央体部(ソーマ)と細い樹状突起状のプロセス内での転写産物の正確な位置と結びつけました。 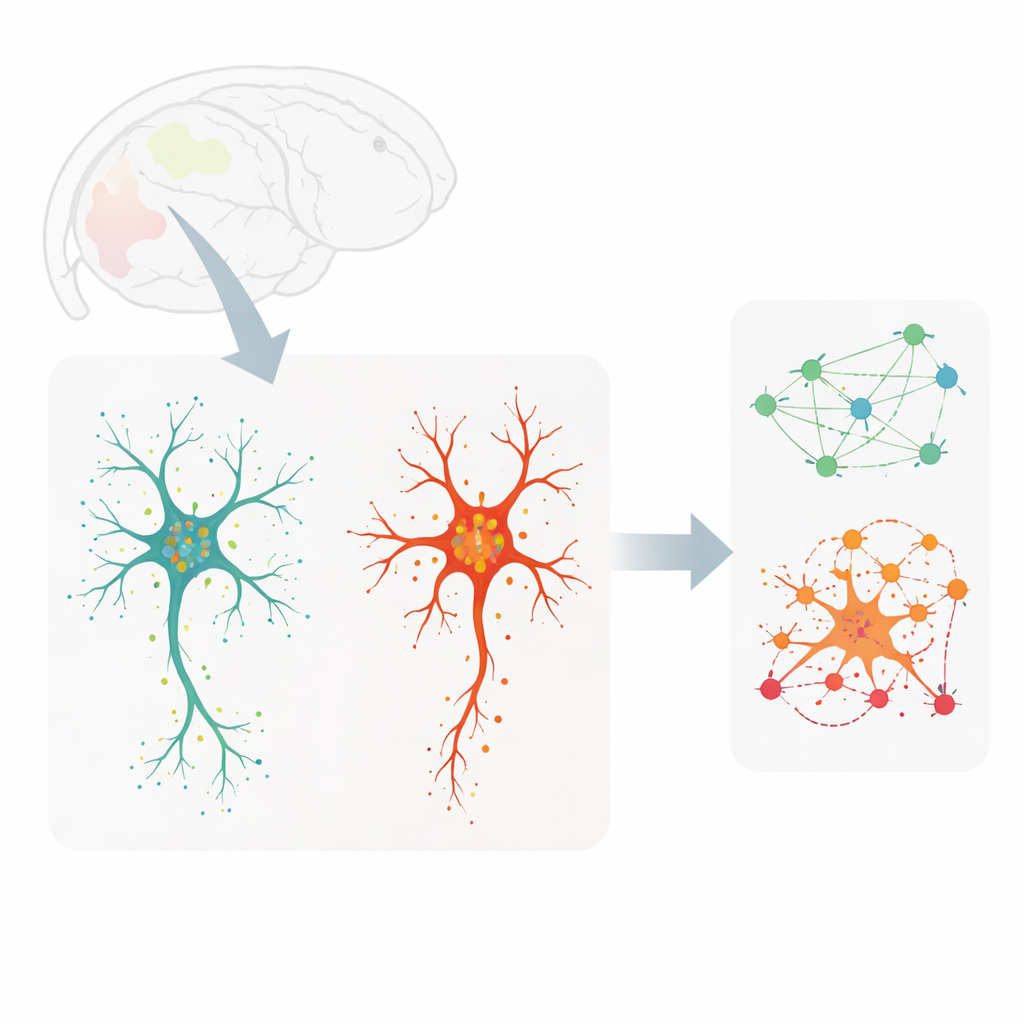
形と状態は常に一致するわけではない
従来、マイクログリアは大きく二つに分けられてきました:多くの枝を持ち静かに脳を見張る扇状(ramified)な細胞と、「活性化」または疾患関連状態にあると考えられるより丸くアメーバ状の細胞です。新しいマップはこの単純な図式を複雑にします。チームが遺伝子発現プロファイルでマイクログリアをクラスタリングしたところ、ホメオスタティック(恒常性維持)、移行期、疾患関連様の3つの主なグループが見つかりました。一方、ニューラルネットワークと数十の幾何学的指標だけで形態に基づいて細胞をクラスタリングすると、枝の少ないものから多いものへの滑らかな連続体が明らかになりました。この二つを比較すると、驚くべき不一致がありました。疾患関連様の遺伝子発現を示す細胞の中には広範な枝分かれを保つものがあり、逆に一見「休止」しているように見える細胞がよりアメーバ状である場合もありました。つまり、輪郭だけからマイクログリアの機能を正確に推測することはできない、ということです。
枝分かれと相関する遺伝子メッセージ
より詳しく調べるため、著者らは特定の遺伝子がマイクログリアの幾何学とどのように関連するかを解析しました。細胞面積、枝先の数、枝分かれの複雑さと強く相関する遺伝子群を同定しました。注目すべきは、グルタミン酸という神経伝達物質の取り扱いに関わる複数の遺伝子で、トランスポーター遺伝子Slc1a2を含め、高度に枝分かれした細胞でより活発であり、RNA分子がプロセスに沿って伸びていることが観察された点です。一方、細胞体に結びつく遺伝子、たとえば内部の小胞や物質の取り込みに関連する遺伝子はソーマの大きさや緻密さと関連していました。中央体またはプロセスに濃縮された転写産物に着目することで、特にプロセス局在の遺伝子が情報量の高いことが示されました:これらのみを用いると、機械学習モデルは枝分かれしたマイクログリアとアメーバ状のものを高い精度で識別できました。 
加齢が内部構造をどう再配置するか
加齢はさらに別のひねりを加えました。若いマウスの扇状マイクログリアでは、多くの遺伝子がソーマかプロセスのいずれかを明瞭に好み、その転写産物はエネルギー利用の管理やシナプスの刈り込みなど協調的な機能を示唆するパターンでしばしば集まっていました。高齢マウスでは、強く区画化された遺伝子の数が減り、互いに近接して存在する転写産物のネットワークはまばらで、重点も変化しました。若い細胞ではソーマに密に共局在するRNAはサイトカイン産生や代謝制御に結び付く傾向がありましたが、高齢細胞では移動や細胞残骸の除去にシフトしました。プロセス内では、若いマイクログリアは局所的なタンパク質処理やシナプスの微調整に結びつくネットワークを示したのに対し、高齢マイクログリアは取り込みと分解に傾きました。こうした加齢に伴う単純化にもかかわらず、Slc1a2やPink1を含むプロセス局在の遺伝子のコア群は、細胞がどれほど枝分かれするかの重要な予測因子として残っていました。
脳の健康にとっての意味
総じて、本研究はマイクログリア内部におけるRNA分子の地理がランダムではなく、それが細胞の形や機能を定義する助けとなり、脳が老いるにつれて再編されることを示しています。「活性化した」マイクログリアが必ず丸く短いという古典的な図式はもはや成り立たず、機能・形態・分子状態は部分的に切り離されうるという理解が必要です。一般読者に向けた主要なメッセージは、脳の免疫細胞は教科書的な絵よりもはるかに多様で適応性が高いということです。どこにメッセージが置かれ、どのようにクラスタを作るかといった内部のロジスティクスが加齢とともにどう変わるかを学ぶことで、科学者たちは最終的にマイクログリアを老化した脳を変性や疾患からよりよく守るような状態へと誘導する方法を見つけられるかもしれません。
引用: Henze, D.E., Tsai, A.P., Wyss-Coray, T. et al. Simultaneous spatial transcriptomics and morphology profiling as tools to explore how microglia change with age. Nat Aging 6, 869–885 (2026). https://doi.org/10.1038/s43587-026-01089-z
キーワード: マイクログリア, 脳の老化, 空間トランスクリプトミクス, 細胞形態, 神経炎症