Clear Sky Science · sv
Samtidig rumslig transkriptomik och morfologisk profilering som verktyg för att undersöka hur mikroglia förändras med åldern
Varför hjärnans immunceller spelar roll när vi blir äldre
När vi åldras förlorar hjärnan inte bara neuroner; stödjande och immunceller runt dem förändras också på subtila sätt som kan påverka minne, humör och sårbarhet för sjukdom. Denna studie undersöker mikroglia — hjärnans egna immunceller — och ställer en förrädiskt enkel fråga: hur förändras dessa cellers finmaskiga förgreningar och hur deras genetiska budskap är fördelade inuti dem med åldern? Genom att kombinera kraftfull avbildning och genavläsning visar författarna att var viktiga molekyler befinner sig i en mikroglia kan påverka dess form och beteende, och att denna rumsliga organisation omformas över livsloppet.
Inblick i den åldrande hjärnan
För att undersöka dessa frågor granskade forskarna hjärnskivor från unga vuxna möss (ungefär motsvarande tidig vuxen ålder hos människor) och mycket gamla möss. De använde en avbildningsmetod kallad MERFISH för att upptäcka hundratals olika RNA-molekyler — geners arbetsexemplar — på nästan enskild-molekylnivå, samtidigt som mikroglia färgades så att varje cells kontur och förgreningsmönster kunde fångas. Detta gjorde det möjligt för dem att kartlägga mer än 3 900 individuella mikroglia över sju hjärnregioner, koppla varje cells detaljerade form till dess genaktivitet och till de exakta platserna för transkripten inom dess tjocka centrala kropp och dess tunna, trädliknande utskott. 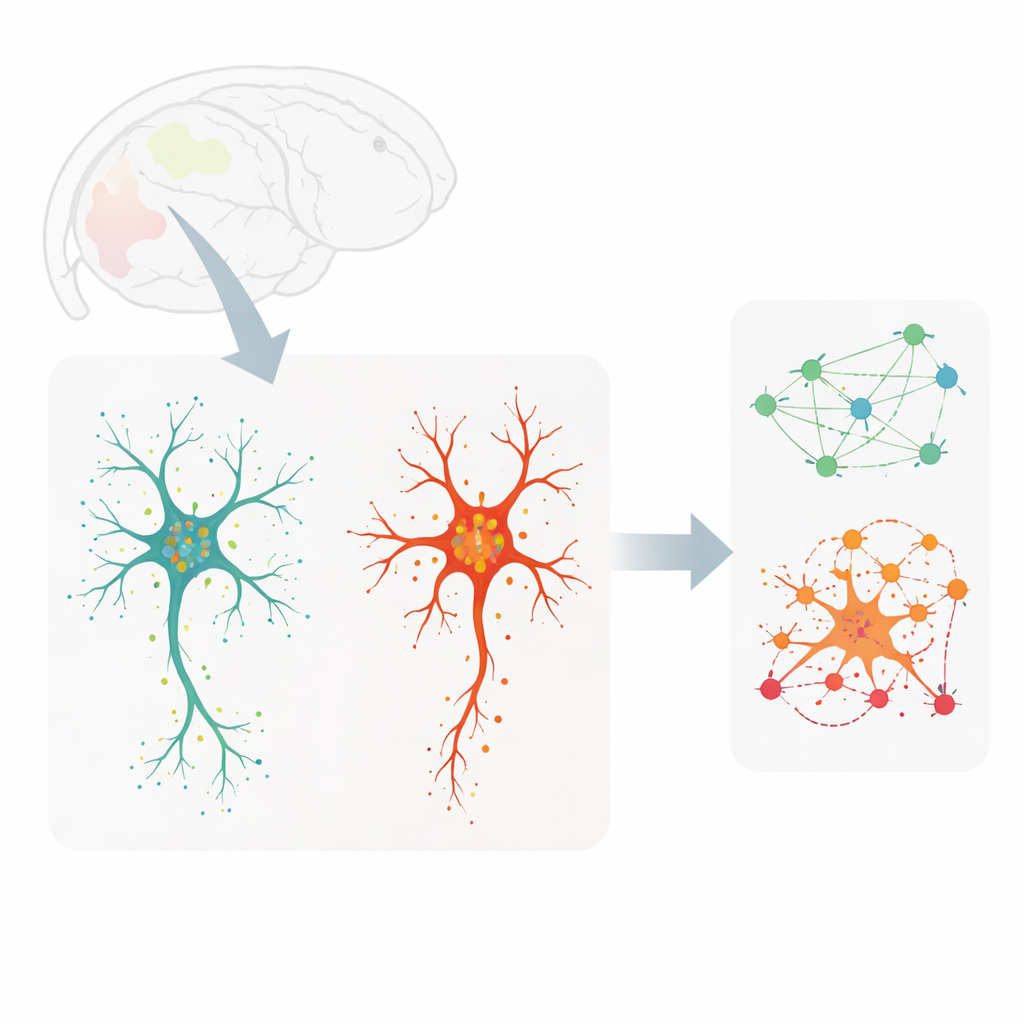
Form och tillstånd stämmer inte alltid överens
Traditionellt har mikroglia delats in i två breda kategorier: ramifierade celler med många grenar som tyst övervakar hjärnan, och rundare, amöboida celler som antas vara i ett "aktiverat" eller sjukdomsassocierat tillstånd. De nya kartorna komplicerar den bilden. När teamet klustrade mikroglia efter deras genuttrycksprofiler fann de tre huvudgrupper: homeostatiska, övergångs- och sjukdomsassocierade-liknande celler. Separat, när de klustrade celler enbart efter form med hjälp av ett neuralt nätverk och flera dussin geometriska mått, avslöjade de ett jämnt spektrum från minst till mest förgrenat. Jämförelse av de två visade en överraskande diskrepans. Vissa sjukdomsassocierade-liknande celler behöll omfattande förgreningar, medan vissa till synes "vila" celler var mer amöboida. Det betyder att man inte pålitligt kan utläsa vad en mikroglial cell gör enbart från dess kontur.
Genetiska budskap som följer förgrening
För att gå djupare undersökte författarna hur specifika gener relaterade till mikroglial geometri. De identifierade genuppsättningar vars aktivitet korrelerade starkt med egenskaper som cellarea, antalet grenändar och komplexiteten i förgreningsmönstren. Noterbart var att flera gener som är involverade i hantering av neurotransmittorn glutamat, inklusive transportergenet Slc1a2, var mer aktiva i starkt förgrenade celler och visade RNA-molekyler som sträckte sig längs utskotten. Andra gener kopplade till cellkroppen, såsom de som associeras med interna vesiklar och upptag av material, följde soma-storlek och kompakthet. Genom att fokusera på transkript som var berikade antingen i den centrala kroppen eller i utskotten visade teamet att processlokaliserade gener var särskilt informativa: med enbart dessa kunde en maskininlärningsmodell skilja förgrenade från amöboida mikroglia med god noggrannhet. 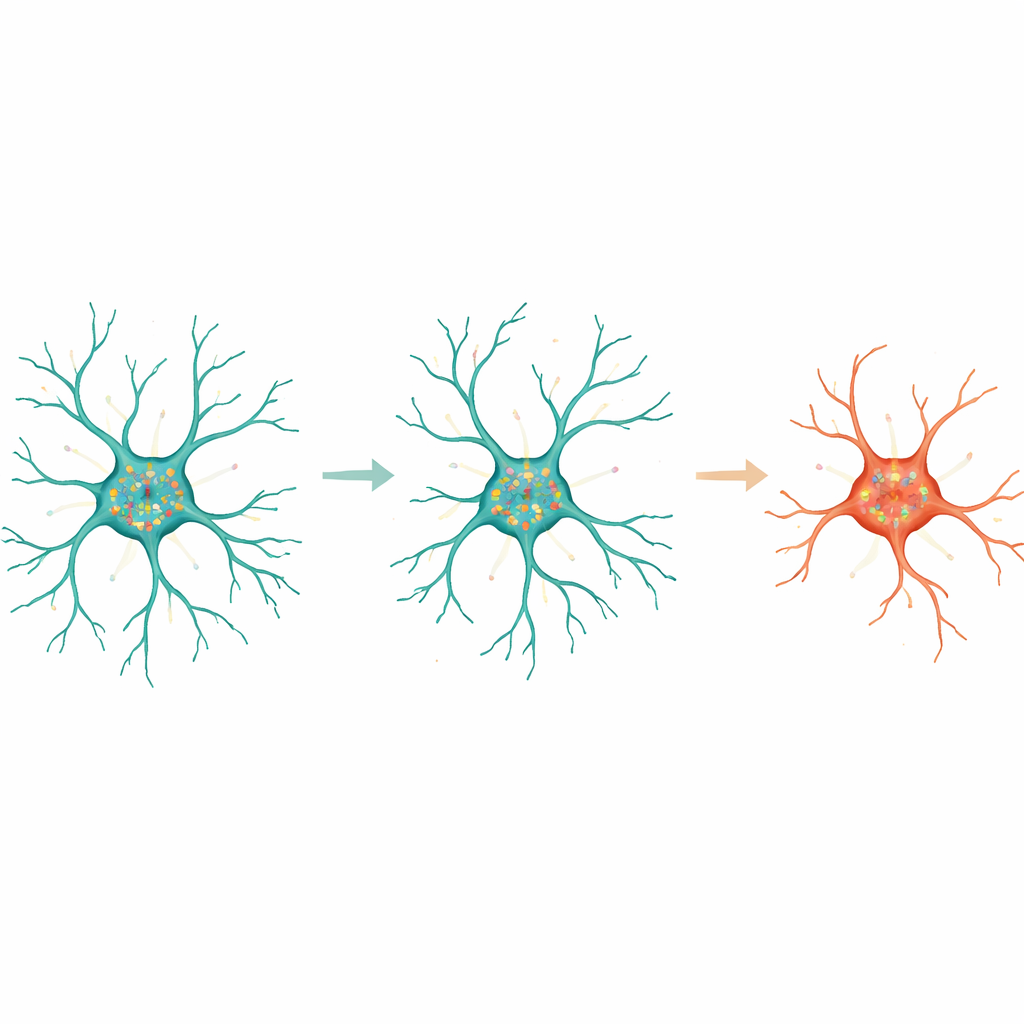
Hur åldrande omarrangerar intern organisation
Åldern lade till ytterligare en vändning. I ramifierade mikroglia från unga möss visade många gener tydliga preferenser för antingen soma eller utskott, och deras transkript klustrade ofta tillsammans i mönster som antydde koordinerade funktioner, såsom hantering av energi eller beskärning av synapser. Hos åldrade möss minskade antalet starkt compartmentaliserade gener, och nätverken av transkript som låg nära varandra blev glesare och förändrade tonvikt. I unga celler tenderade tätt kolokaliserade RNA i soma att kopplas till cytokinproduktion och metabolisk kontroll, medan de i äldre celler skiftade mot migration och borttagning av cellulärt skräp. I utskotten visade unga mikroglia nätverk knutna till lokal proteinhantering och synapsjustering, medan åldrande mikroglia lutade mot upptag och nedbrytning av material. Trots denna förenkling med åldern förblev en kärngrupp av processlokaliserade gener, inklusive Slc1a2 och Pink1, nyckelprediktorer för hur förgrenad en cell skulle vara.
Vad detta betyder för hjärnhälsa
Sammantaget visar arbetet att den inre geografien för RNA-molekyler i mikroglia inte är slumpmässig: den hjälper till att definiera hur dessa celler är formade och vad de gör, och den omformas när hjärnan blir äldre. Den klassiska bilden att "aktiverade" mikroglia måste vara runda och knubbiga håller inte längre; i stället kan funktion, form och molekylärt tillstånd delvis vara okopplade. För en allmän läsare är huvudbudskapet att hjärnans immunceller är mycket mer varierade och anpassningsbara än deras läroboksframställningar antyder. Genom att förstå hur deras interna logistik — var budskap placeras och med vilka de klustrar — förändras med åldern kan forskare så småningom hitta sätt att styra mikroglia mot tillstånd som bättre skyddar den åldrande hjärnan från degeneration och sjukdom.
Citering: Henze, D.E., Tsai, A.P., Wyss-Coray, T. et al. Simultaneous spatial transcriptomics and morphology profiling as tools to explore how microglia change with age. Nat Aging 6, 869–885 (2026). https://doi.org/10.1038/s43587-026-01089-z
Nyckelord: mikroglia, hjärnans åldrande, rumslig transkriptomik, cellmorfologi, neuroinflammation