Clear Sky Science · it
Transcriptomica spaziale simultanea e profili morfologici come strumenti per esplorare come i microglia cambiano con l’età
Perché le cellule immunitarie cerebrali contano con l’avanzare dell’età
Con l’età, il cervello non perde soltanto neuroni; anche le cellule di supporto e immunitarie che li circondano cambiano in modi sottili che possono influenzare memoria, umore e vulnerabilità alle malattie. Questo studio si concentra sui microglia — le cellule immunitarie residenti del cervello — e pone una domanda apparentemente semplice: come cambia con l’età l’organizzazione fine di queste cellule e la posizione dei loro messaggi genetici al loro interno? Combinando potenti strumenti di imaging e lettura genica, gli autori mostrano che la collocazione di molecole chiave all’interno di un microglio può influenzarne forma e comportamento, e che questa organizzazione spaziale viene rimodellata nel corso della vita.
Uno sguardo all’interno del cervello invecchiato
Per esplorare queste questioni, i ricercatori hanno esaminato sezioni cerebrali di topi in giovane età adulta (all’incirca l’inizio dell’età adulta nell’uomo) e di topi molto anziani. Hanno utilizzato un metodo di imaging chiamato MERFISH per rilevare centinaia di diverse molecole di RNA — le copie operative dei geni — a risoluzione quasi mono-molecolare, mentre contemporaneamente coloravano i microglia in modo che il contorno e il pattern di diramazione di ciascuna cellula potessero essere catturati. Questo ha permesso di mappare oltre 3.900 microglia individuali in sette regioni cerebrali, collegando la forma dettagliata di ogni cellula alla sua attività genica e alle posizioni esatte dei trascritti all’interno del suo corpo centrale spesso e dei suoi sottili processi arboriformi. 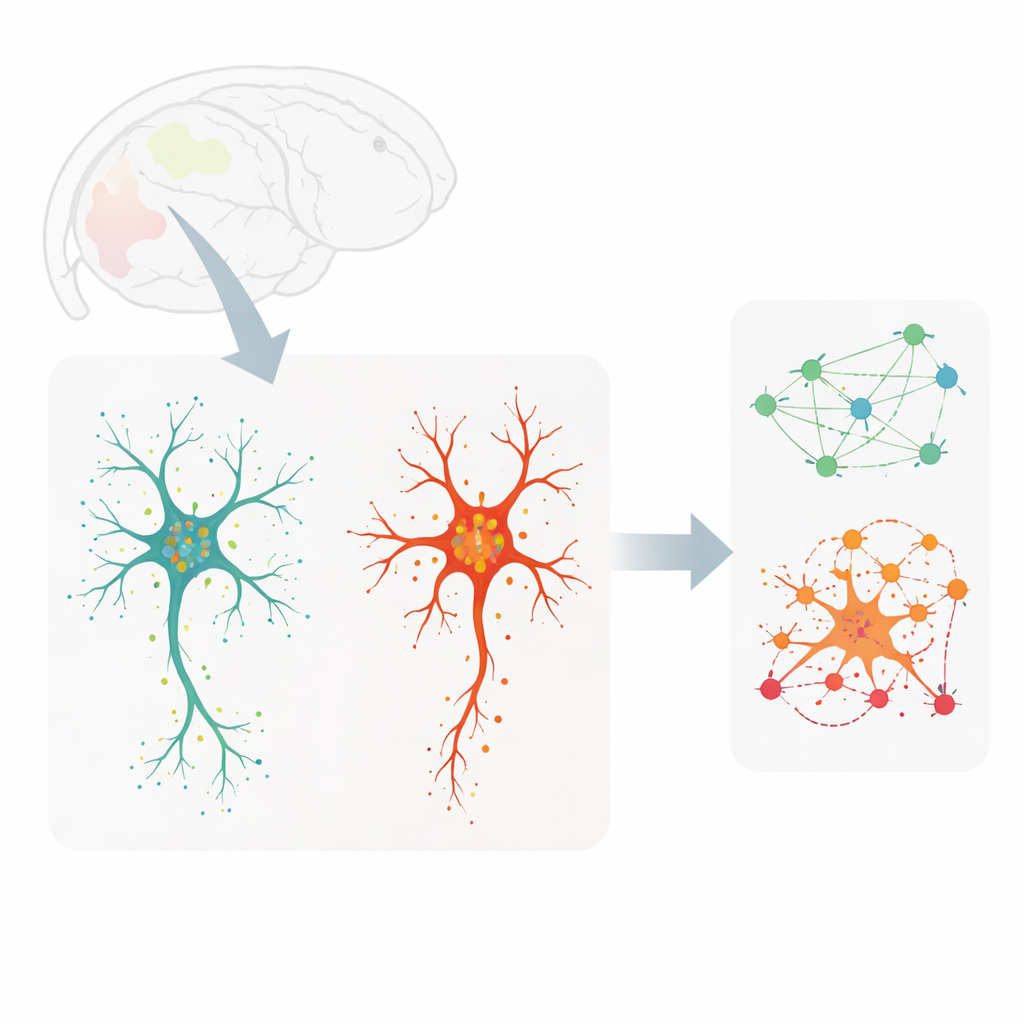
Forme e stati non sempre coincidono
Tradizionalmente i microglia sono stati divisi in due grandi categorie: cellule ramificate con molti rami che sorvegliano silenziosamente il cervello, e cellule più tondeggianti, ameboidi, considerate in uno stato «attivato» o associato alla malattia. Le nuove mappe complicano questa visione. Quando il team ha raggruppato i microglia in base ai loro profili di espressione genica, ha trovato tre gruppi principali: cellule omeostatiche, in transizione e simili a quelle associate alla malattia. Separatamente, raggruppando le cellule unicamente per forma tramite una rete neurale e dozzine di misure geometriche, hanno scoperto uno spettro continuo dal meno al più ramificato. Il confronto dei due insiemi ha rivelato una sorprendente discrepanza. Alcune cellule simili a quelle associate alla malattia mantenevano ampia ramificazione, mentre altre cellule apparentemente «a riposo» erano più ameboidi. Ciò significa che non si può inferire in modo affidabile cosa stia facendo un microglio solo dal suo profilo esterno.
Messaggi genetici che si associano alla ramificazione
Per approfondire, gli autori hanno esaminato come geni specifici si relazionassero alla geometria microgliale. Hanno identificato set di geni la cui attività correlava fortemente con caratteristiche come l’area cellulare, il numero di punte dei rami e la complessità dei pattern di diramazione. Notoriamente, diversi geni coinvolti nella gestione del neurotrasmettitore glutammato, incluso il gene trasportatore Slc1a2, risultavano più attivi nelle cellule altamente ramificate e mostravano molecole di RNA estese lungo i processi. Altri geni legati al corpo cellulare, come quelli associati a vescicole interne e all’ingestione di materiale, si correlavano con la dimensione e la compattezza del soma. Focalizzandosi sui trascritti arricchiti o nel corpo centrale o nei processi, il team ha dimostrato che i geni localizzati nei processi erano particolarmente informativi: usando soltanto questi, un modello di machine learning riusciva a distinguere con buona accuratezza microglia ramificati da quelli ameboidi. 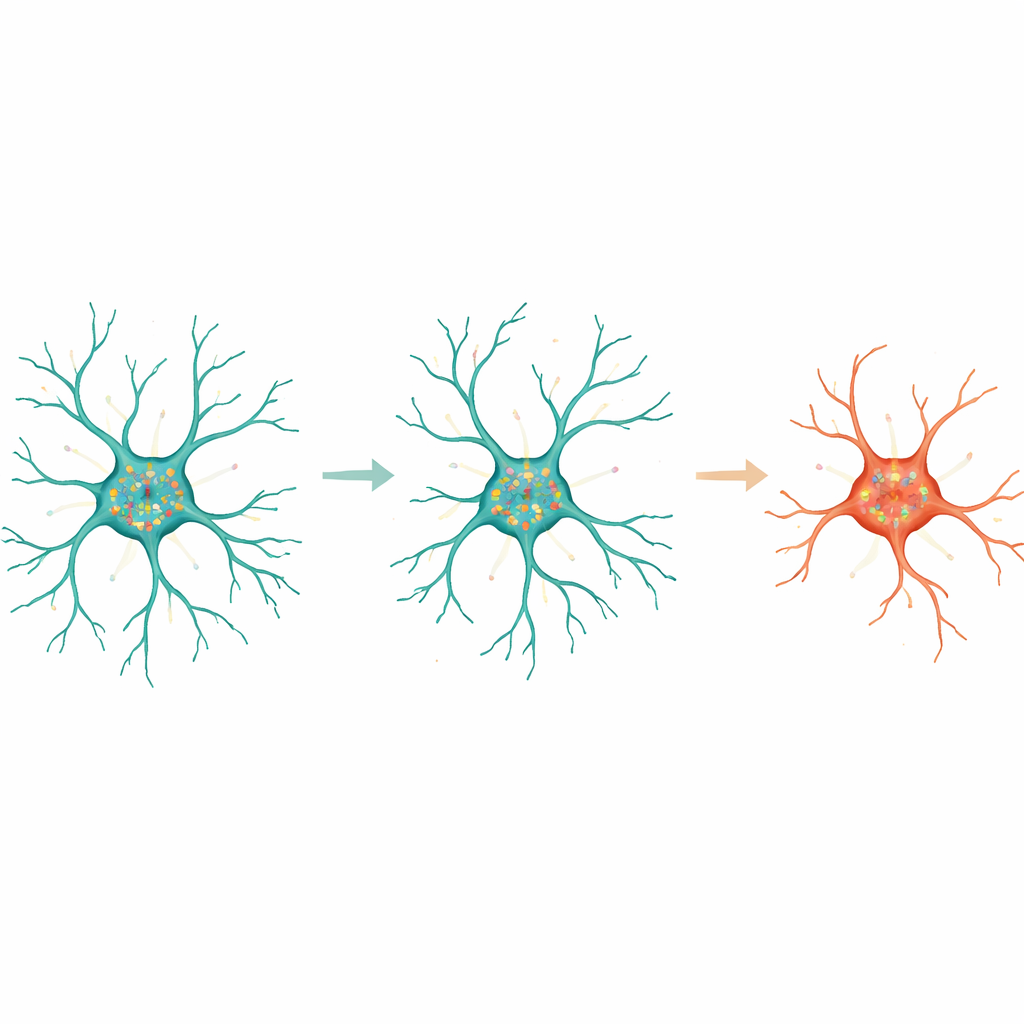
Come l’età riorganizza l’organizzazione interna
L’età ha aggiunto un ulteriore elemento. Nei microglia ramificati dei topi giovani, molti geni mostravano preferenze chiare per il soma o per i processi, e i loro trascritti spesso si raggruppavano in pattern che suggerivano funzioni coordinate, come la gestione dell’energia o il potatura delle sinapsi. Nei topi anziani, il numero di geni fortemente compartimentalizzati è diminuito e le reti di trascritti che si trovavano vicine l’una all’altra sono diventate più rade e con un’enfasi diversa. Nelle cellule giovani, gli RNA strettamente co-localizzati nel soma tendevano a essere collegati alla produzione di citochine e al controllo metabolico, mentre nelle cellule più vecchie si spostavano verso la migrazione e la rimozione di detriti cellulari. Nei processi, i microglia giovani mostravano reti legate alla gestione locale delle proteine e al raffinamento delle sinapsi, mentre i microglia anziani inclinavano verso l’assorbimento e la degradazione di materiale. Nonostante questa semplificazione con l’età, un gruppo centrale di geni localizzati nei processi, tra cui Slc1a2 e Pink1, è rimasto predittore chiave del grado di ramificazione di una cellula.
Cosa significa per la salute del cervello
Nel complesso, il lavoro mostra che la geografia interna delle molecole di RNA all’interno dei microglia non è casuale: contribuisce a definire forma e funzioni di queste cellule ed è rimodellata con l’invecchiamento cerebrale. L’immagine classica secondo cui i microglia «attivati» devono essere necessariamente tondeggianti e tozzi non regge più; invece, funzione, forma e stato molecolare possono essere parzialmente disaccoppiati. Per il lettore non specialista, il messaggio chiave è che le cellule immunitarie cerebrali sono molto più diverse e adattabili di quanto suggeriscano i ritratti da manuale. Capire come la loro logistica interna — dove vengono collocati i messaggi e con chi si raggruppano — cambi con l’età potrebbe un giorno aiutare gli scienziati a orientare i microglia verso stati che proteggano meglio il cervello invecchiante dalla degenerazione e dalle malattie.
Citazione: Henze, D.E., Tsai, A.P., Wyss-Coray, T. et al. Simultaneous spatial transcriptomics and morphology profiling as tools to explore how microglia change with age. Nat Aging 6, 869–885 (2026). https://doi.org/10.1038/s43587-026-01089-z
Parole chiave: microglia, invecchiamento cerebrale, transcriptomica spaziale, morfologia cellulare, neuroinfiammazione