Clear Sky Science · es
Transcriptómica espacial simultánea y perfilado morfológico como herramientas para explorar cómo cambian las microglias con la edad
Por qué importan las células inmunitarias del cerebro a medida que envejecemos
A medida que envejecemos, nuestro cerebro no solo pierde neuronas; las células de soporte e inmunitarias que las rodean también cambian de maneras sutiles que pueden moldear la memoria, el estado de ánimo y la vulnerabilidad a enfermedades. Este estudio se centra en las microglias —las células inmunitarias residentes del cerebro— y plantea una pregunta aparentemente sencilla: ¿cómo cambia la fina organización de estas células, y la localización de sus mensajes genéticos, con la edad? Al combinar potentes técnicas de imagen y lectura genética, los autores muestran que la posición de moléculas clave dentro de una microglía puede influir en su forma y comportamiento, y que esta organización espacial se remodela a lo largo de la vida.
Mirando dentro del cerebro envejecido
Para explorar estas cuestiones, los investigadores examinaron cortes cerebrales de ratones adultos jóvenes (aproximadamente la adultez temprana en términos humanos) y de ratones muy viejos. Emplearon un método de imagen llamado MERFISH para detectar cientos de moléculas de ARN diferentes —las copias operativas de los genes— a resolución cercana a la de una sola molécula, mientras teñían simultáneamente las microglias para capturar el contorno y el patrón ramificado de cada célula. Esto les permitió mapear más de 3.900 microglias individuales en siete regiones cerebrales, vinculando la forma detallada de cada célula con su actividad génica y con las localizaciones exactas de los transcriptos dentro de su cuerpo central grueso y sus procesos delgados y arbóreos. 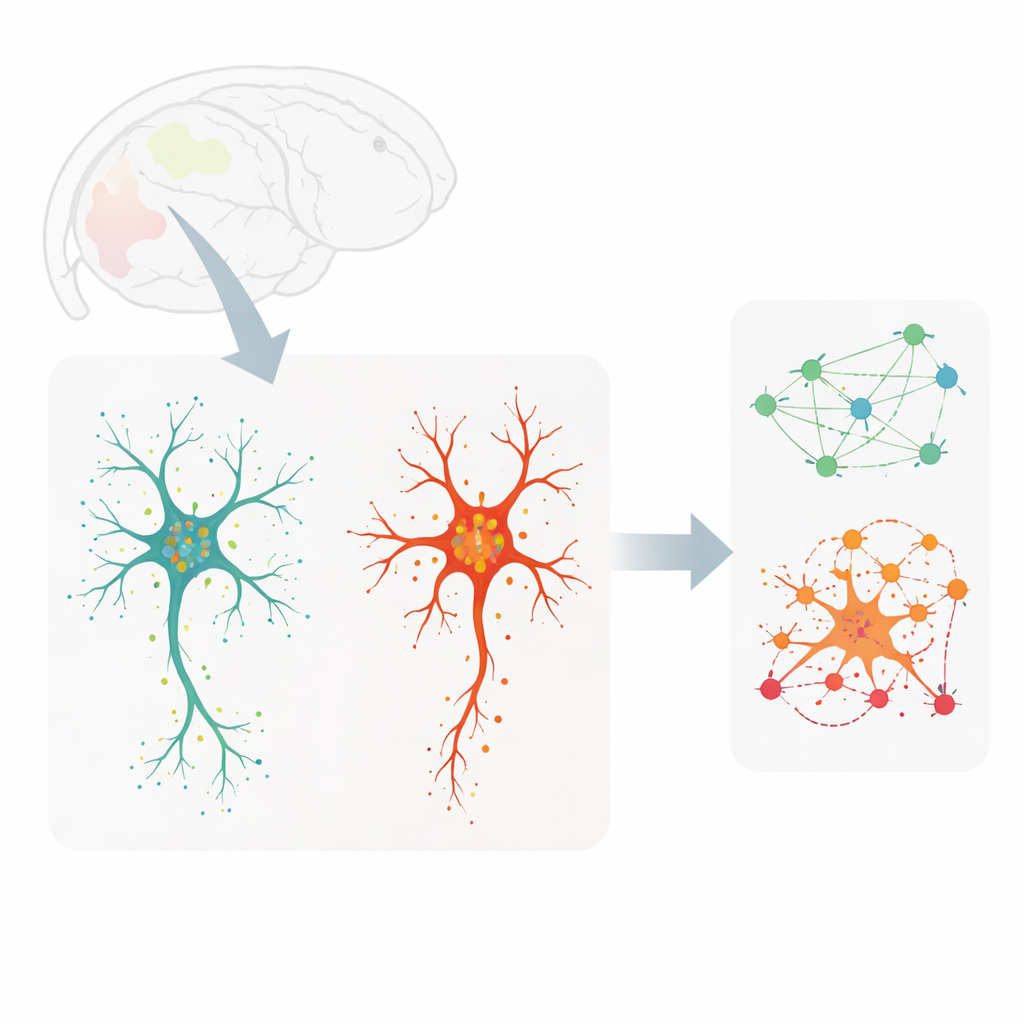
La forma y el estado no siempre coinciden
Tradicionalmente, las microglias se han dividido en dos grandes categorías: células ramificadas con muchas ramas que vigilan el cerebro de forma tranquila, y células más redondeadas, ameboides, que se consideran en un estado “activado” o asociado a la enfermedad. Los nuevos mapas complican esa visión. Cuando el equipo agrupó las microglias según sus perfiles de expresión génica, encontró tres grupos principales: homeostáticas, en transición y con similitud a células asociadas a la enfermedad. Por separado, al agrupar las células solo por forma utilizando una red neuronal y docenas de mediciones geométricas, descubrieron un espectro continuo desde las menos hasta las más ramificadas. Al comparar ambos enfoques surgió una discrepancia sorprendente. Algunas células tipo enfermedad mantenían un ramificado extenso, mientras que algunas células aparentemente “reposadas” eran más ameboides. Esto significa que no se puede inferir de forma fiable la función de una microglía solo por su contorno.
Mensajes genéticos que acompañan a la ramificación
Para profundizar, los autores examinaron cómo genes específicos se relacionaban con la geometría microglial. Identificaron conjuntos de genes cuya actividad correlacionaba fuertemente con características como el área celular, el número de extremos de las ramas y la complejidad de los patrones de ramificación. En particular, varios genes implicados en el manejo del neurotransmisor glutamato, incluido el gen transportador Slc1a2, mostraron mayor actividad en células altamente ramificadas y presentaron moléculas de ARN que se extendían a lo largo de los procesos. Otros genes vinculados al cuerpo celular, como los asociados a vesículas internas y a la ingestión de material, se relacionaron con el tamaño y la compactación del soma. Al centrarse en los transcriptos enriquecidos ya sea en el cuerpo central o en los procesos, el equipo demostró que los genes localizados en los procesos eran especialmente informativos: usando solo estos, un modelo de aprendizaje automático pudo distinguir microglias ramificadas de ameboides con buena precisión. 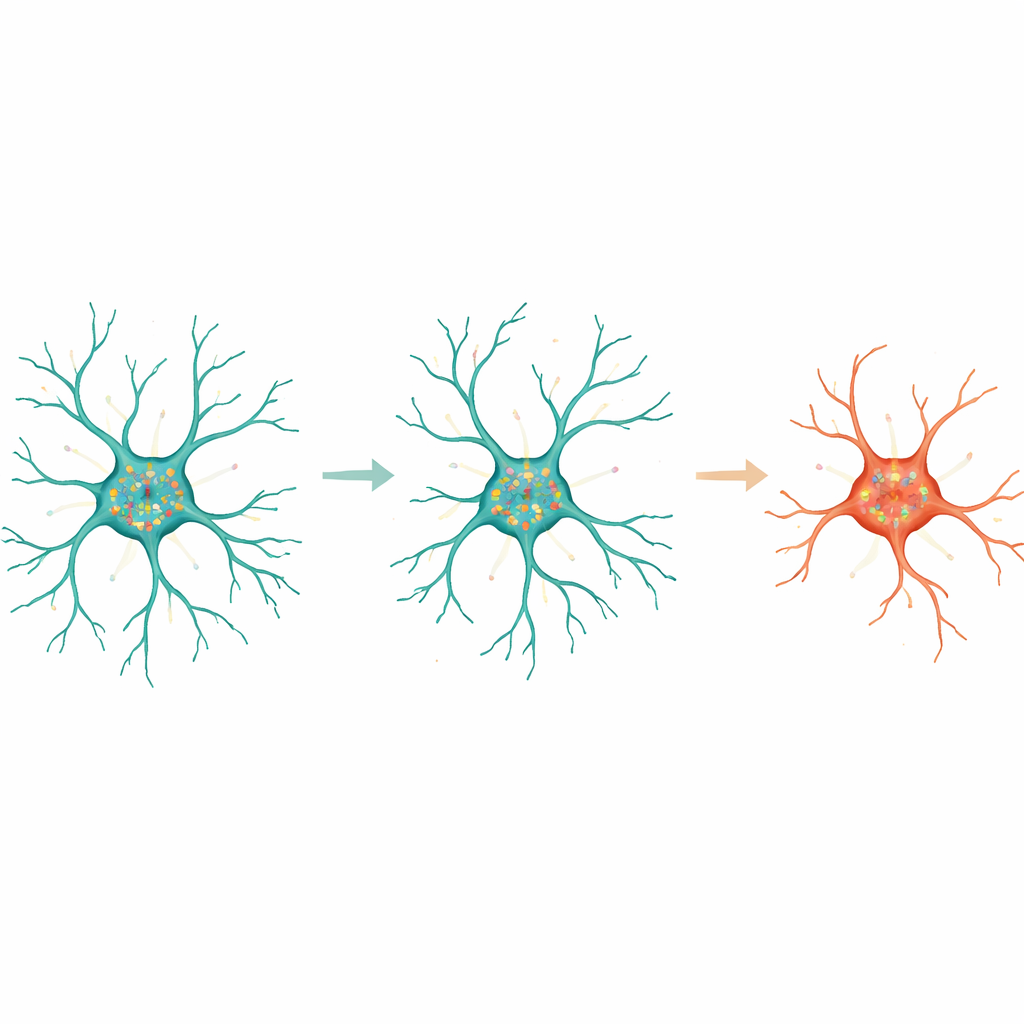
Cómo el envejecimiento reorganiza la organización interna
La edad añadió otra vuelta de tuerca. En las microglias ramificadas de ratones jóvenes, muchos genes mostraban claras preferencias por el soma o por los procesos, y sus transcriptos a menudo se agrupaban en patrones que sugerían funciones coordinadas, como gestionar el uso de energía o podar sinapsis. En ratones envejecidos, el número de genes fuertemente compartimentados disminuyó, y las redes de transcriptos que se situaban cerca unas de otras se hicieron más escasas y cambiaron de énfasis. En células jóvenes, los ARN estrechamente colocalizados en el soma tendían a vincularse con la producción de citocinas y el control metabólico, mientras que en células mayores se desplazaban hacia la migración y la eliminación de desechos celulares. En los procesos, las microglias jóvenes mostraban redes relacionadas con el manejo local de proteínas y el refinamiento sináptico, mientras que las microglias envejecidas se inclinaban hacia la captación y degradación de material. A pesar de esta simplificación con la edad, un grupo central de genes localizados en los procesos, incluyendo Slc1a2 y Pink1, siguió siendo predictivo de cuán ramificada sería una célula.
Qué significa esto para la salud cerebral
En conjunto, el trabajo muestra que la geografía interna de las moléculas de ARN dentro de las microglias no es aleatoria: ayuda a definir cómo se moldean estas células y qué hacen, y se remodela a medida que el cerebro envejece. La imagen clásica de que las microglias “activadas” deben ser redondeadas y toscas ya no se sostiene; en cambio, la función, la forma y el estado molecular pueden estar parcialmente desvinculados. Para el lector general, el mensaje clave es que las células inmunitarias cerebrales son mucho más diversas y adaptables de lo que sugieren los retratos de libro de texto. Al aprender cómo su logística interna —dónde se colocan los mensajes y con quién se agrupan— cambia con la edad, los científicos podrían eventualmente encontrar formas de orientar a las microglias hacia estados que protejan mejor al cerebro envejecido frente a la degeneración y la enfermedad.
Cita: Henze, D.E., Tsai, A.P., Wyss-Coray, T. et al. Simultaneous spatial transcriptomics and morphology profiling as tools to explore how microglia change with age. Nat Aging 6, 869–885 (2026). https://doi.org/10.1038/s43587-026-01089-z
Palabras clave: microglía, envejecimiento cerebral, transcriptómica espacial, morfología celular, neuroinflamación