Clear Sky Science · pl
Jednoczesne przestrzenne transkryptomika i profilowanie morfologii jako narzędzia do badania, jak mikroglej zmienia się z wiekiem
Dlaczego komórki odpornościowe mózgu mają znaczenie w miarę naszego starzenia się
W miarę starzenia się mózgu nie tracimy tylko neuronów; komórki wspierające i układu odpornościowego wokół nich również ulegają subtelnym zmianom, które mogą wpływać na pamięć, nastrój i podatność na choroby. W tym badaniu przyglądamy się mikroglejowi — rezydentnym komórkom odpornościowym mózgu — i zadajemy pozornie proste pytanie: jak zmienia się drobne okablowanie tych komórek i rozmieszczenie ich komunikatów genetycznych wraz z wiekiem? Łącząc zaawansowane techniki obrazowania i czytania genów, autorzy pokazują, że to, gdzie kluczowe cząsteczki znajdują się wewnątrz komórki mikroglejowej, może wpływać na jej kształt i zachowanie, i że ta przestrzenna organizacja jest przebudowywana w ciągu życia.
Wgląd w starzejący się mózg
Aby zbadać te zagadnienia, badacze przeanalizowali plasterki mózgu pochodzące od młodych dorosłych myszy (odpowiednik wczesnej dorosłości u ludzi) oraz od bardzo starych myszy. Wykorzystali metodę obrazowania MERFISH do wykrycia setek różnych cząsteczek RNA — czynnych kopii genów — z prawie pojedynczą rozdzielczością molekularną, jednocześnie barwiąc mikroglej tak, by można było uchwycić obrys każdej komórki i wzór jej rozgałęzień. Pozwoliło to na zmapowanie ponad 3900 pojedynczych mikroglejów w siedmiu regionach mózgu, łącząc szczegółowy kształt każdej komórki z jej aktywnością genową oraz z dokładnymi lokalizacjami transkryptów w grubej centralnej części ciała i cienkich, drzewiastych wypustkach. 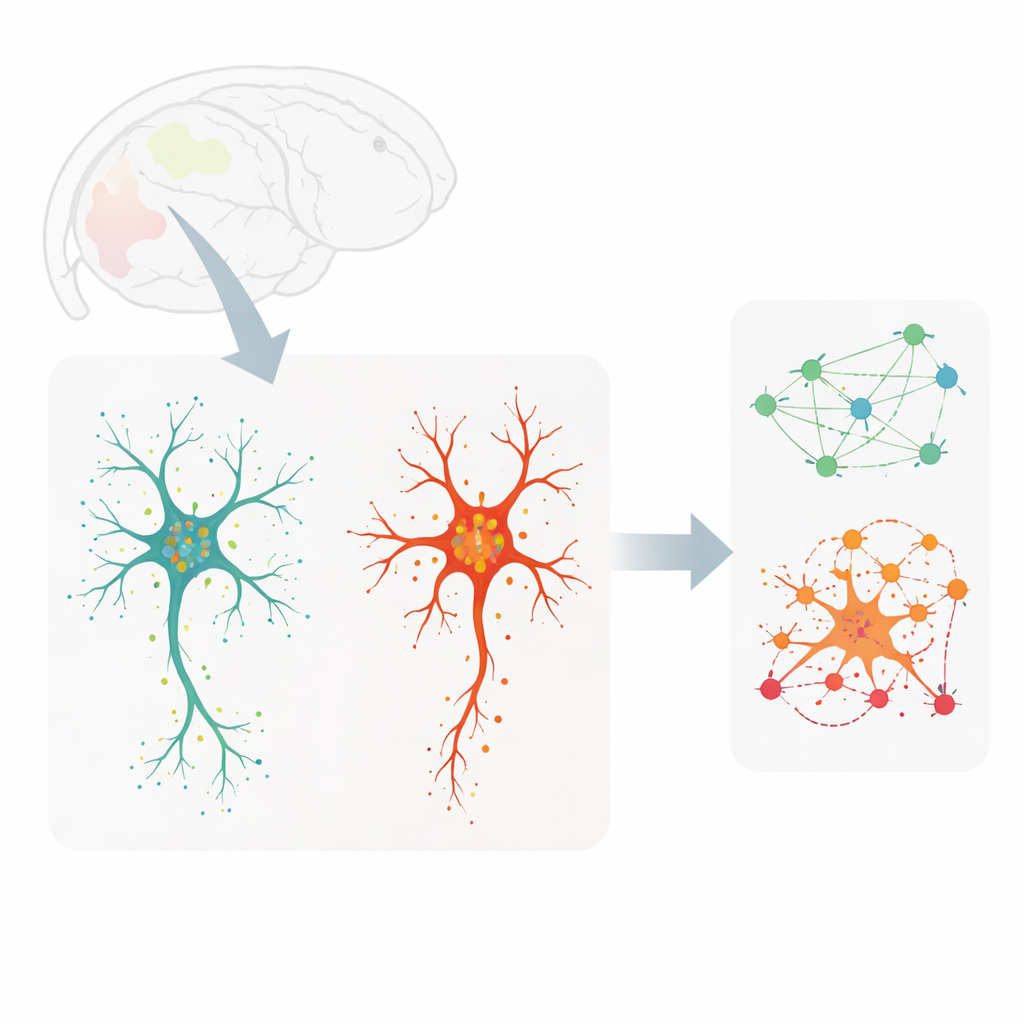
Kształty i stany nie zawsze idą w parze
Tradycyjnie mikroglej dzielono na dwa główne typy: rozgałęzione komórki z wieloma wypustkami, które biernie patrolują mózg, oraz bardziej okrągłe, ameboidalne komórki uważane za „aktywowane” lub związane z chorobą. Nowe mapy komplikują tę opowieść. Gdy zespół grupował mikrogleje według profili ekspresji genów, wyróżnili trzy główne grupy: komórki homeostatyczne, przejściowe i podobne do komórek związanych z chorobą. Osobno, gdy grupowali komórki wyłącznie według kształtu przy użyciu sieci neuronowej i kilkudziesięciu miar geometrycznych, odkryli płynne spektrum od najmniej do najbardziej rozgałęzionych. Porównanie obu podziałów ujawniło zaskakującą rozbieżność. Niektóre komórki przypominające te związane z chorobą zachowały rozległe rozgałęzienia, podczas gdy niektóre pozornie „spoczywające” komórki były bardziej ameboidalne. Oznacza to, że nie można wiarygodnie wnioskować, co robi komórka mikroglejowa, patrząc tylko na jej zarys.
Komunikaty genetyczne związane z rozgałęzieniem
Aby zagłębić się bardziej, autorzy zbadali, jak konkretne geny korelują z geometrią mikrogleju. Zidentyfikowali zestawy genów, których aktywność silnie korelowała z cechami takimi jak powierzchnia komórki, liczba końcówek gałązek i złożoność wzorów rozgałęzień. Co warte uwagi, kilka genów zaangażowanych w obsługę neurotransmitera glutaminianu, w tym gen kodujący transporter Slc1a2, było bardziej aktywnych w silnie rozgałęzionych komórkach i wykazywało cząsteczki RNA rozciągające się wzdłuż wypustek. Inne geny związane z ciałem komórkowym, takie jak te powiązane z wewnętrznymi pęcherzykami i trawieniem materiału, korelowały z rozmiarem i zwartością somy. Skupiając się na transkryptach wzbogaconych albo w centralnym ciele, albo we wypustkach, zespół wykazał, że geny lokalizowane w wypustkach były szczególnie informatywne: używając tylko tych, model uczenia maszynowego mógł z dobrą dokładnością odróżnić mikroglej rozgałęziony od ameboidalnego. 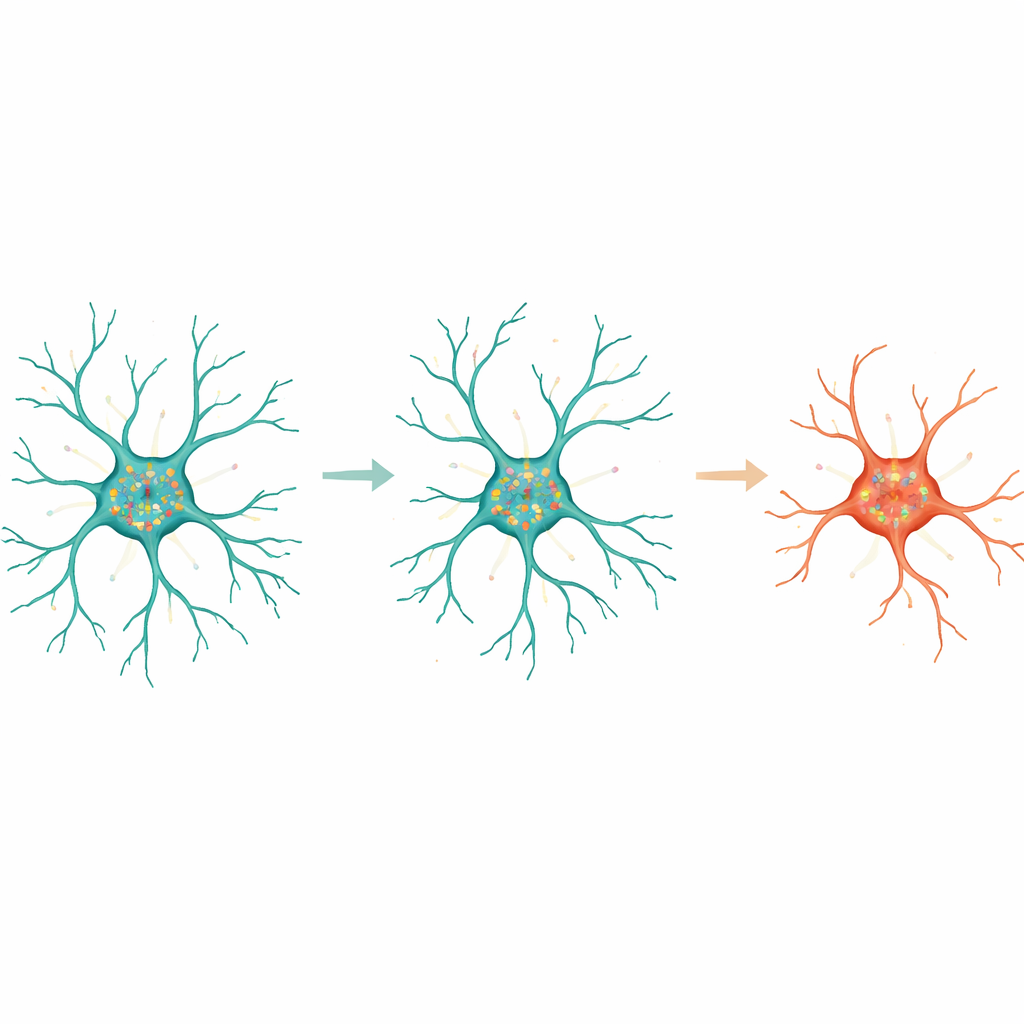
Jak starzenie się przebudowuje wewnętrzną organizację
Wiek dodał kolejny zwrot akcji. W rozgałęzionych mikroglejach młodych myszy wiele genów wykazywało wyraźne preferencje dla somy lub wypustek, a ich transkrypty często skupiały się razem w wzory sugerujące skoordynowane funkcje, takie jak zarządzanie zużyciem energii czy przycinanie synaps. U starszych myszy liczba silnie skompartamentalizowanych genów spadła, a sieci transkryptów znajdujących się blisko siebie stały się rzadsze i zmieniły nacisk funkcjonalny. W młodych komórkach ściśle współlokalizowane RNA w somie miały tendencję do bycia powiązanymi z produkcją cytokin i kontrolą metaboliczną, podczas gdy w starszych komórkach przesunęły się w kierunku migracji i usuwania szczątków komórkowych. W wypustkach młodych mikroglejów sieci powiązane były z lokalnym przetwarzaniem białek i rafinacją synaps, natomiast w mikroglejach starszych dominowało przejmowanie i rozkład materiału. Pomimo tej uproszczonej organizacji z wiekiem, rdzeniowa grupa genów lokalizowanych w wypustkach, w tym Slc1a2 i Pink1, pozostała kluczowym predyktorem stopnia rozgałęzienia komórki.
Co to znaczy dla zdrowia mózgu
Podsumowując, praca pokazuje, że wewnętrzna geografia cząsteczek RNA w mikrogleju nie jest przypadkowa: pomaga definiować, jak te komórki są ukształtowane i co robią, i jest przekształcana w miarę starzenia się mózgu. Klasyczny obraz, że „aktywowany” mikroglej musi być okrągły i krępy, przestaje być prawdziwy; zamiast tego funkcja, kształt i stan molekularny mogą być częściowo rozłączone. Dla czytelnika niebędącego specjalistą kluczowy przekaz jest taki, że komórki odpornościowe mózgu są znacznie bardziej zróżnicowane i elastyczne niż sugerują podręcznikowe portrety. Poznając, jak ich wewnętrzna logistyka — gdzie umieszczane są komunikaty i z kim się grupują — zmienia się z wiekiem, naukowcy mogą w końcu znaleźć sposoby na skłonienie mikrogleju do stanów, które lepiej chronią starzejący się mózg przed degeneracją i chorobami.
Cytowanie: Henze, D.E., Tsai, A.P., Wyss-Coray, T. et al. Simultaneous spatial transcriptomics and morphology profiling as tools to explore how microglia change with age. Nat Aging 6, 869–885 (2026). https://doi.org/10.1038/s43587-026-01089-z
Słowa kluczowe: mikroglej, starzenie się mózgu, przestrzenna transkryptomika, morfologia komórkowa, nezapalenie nerwowe