Clear Sky Science · tr
Triazol indolinon ligandinin vanadil iyonlarıyla kontrollü redoks aktivitesi ve koordinasyon davranışı
Bu çalışma neden önemli
Temiz su, daha güvenli ilaçlar ve daha akıllı sensörler, metal iyonlarını istenildiğinde tutup bırakabilen küçük kimyasal yardımcı moleküllere dayanır. Bu çalışma, H2TIS adını taşıyan, özel tasarlanmış bir organik bileşiği inceliyor ve çevreleyen sıvının asiditesini veya bazikliğini değiştirerek bu molekülün davranışının nasıl hassas şekilde ayarlanabileceğini gösteriyor. Bu molekülün elektron alışverişini ve teknolojik ve biyolojik açıdan önemli bir metal olan vanadyumla bağlanmasını anlayarak araştırmacılar, daha iyi katalizörler, kirlilik algılayıcıları ve gelişmiş batarya veya sensör malzemeleri tasarlamaya bir adım daha yaklaşıyor.
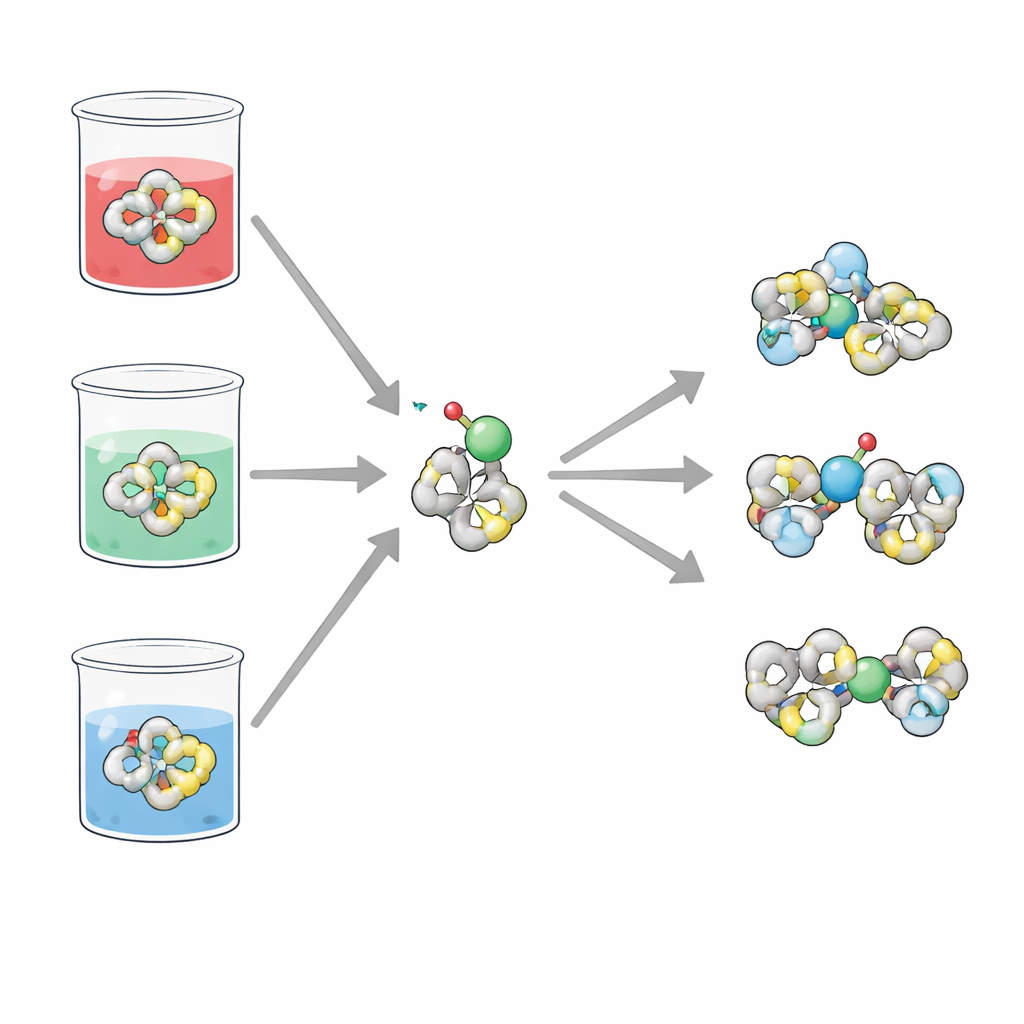
Şekil değiştiren bir yardımcı molekül
H2TIS, birden fazla halka yapısı ve elektron çifti verebilen kimyasal gruplardan oluşan kompakt bir organik moleküldür. Bu “donör” noktalar arasında kükürt, azot ve oksijen atomları bulunur; bunlar birlikte H2TIS’i metal iyonlarını kavramak için mükemmel bir aday yapar. Ekip, bu ligandın elektron kazandığında veya kaybettiğinde (redoks aktivitesi) nasıl davrandığına ve vanadilde (suda yaygın bir vanadyum formu) nasıl bağlandığına odaklandı. Bu süreçler çözeltinin asidik, nötr veya bazik olmasına güçlü biçimde bağlı olduğundan, araştırmacılar H2TIS’i bu koşulları taklit eden üç basit tuz çözeltisinde inceledi.
Elektronların küçük voltaj taramalarıyla izlenmesi
H2TIS’in elektron taşıma davranışını takip etmek için bilim insanları, bir karbon elektrotunda voltajın ileri geri tarandığı ve ortaya çıkan akımın ölçüldüğü döngüsel voltametri tekniğini kullandı. Asidik çözeltide, molekülün karbonil grubuna elektron eklendiğinde bir akım tepe noktası gözlendi; bu işlem, karbon‑oksijen çift bağını daha indirgenmiş bir forma dönüştürüyordu. Ters yönde tarama yapıldığında, ligandın kükürt içeren bölümünde oksidasyonla bağlantılı başka bir tepe belirdi. Bu tepelerin konumları ve biçimleri ile bunların konsantrasyon ve tarama hızına göre değişimleri, hem elektron transferi hem de bunu izleyen kimyasal adımların dahil olduğunu ve sürecin çözelti içindeki proton varlığına bağlı olduğunu gösterdi.
Çevreleyen sıvı hikâyeyi nasıl değiştiriyor
Aynı ligand nötr çözelti içinde test edildiğinde, karbonil grubu daha dengeli bir anahtar gibi davrandı ve neredeyse birbirinin ayna görüntüsü olan bir tepe çifti gösterdi. Bu desen, ileri ve geri elektron transferlerinin makul ölçüde eşlendiği yarı‑tersinir bir redoks çifti olduğunu, sistemin daha kararlı ve öngörülebilir hale geldiğini işaret etti. Ancak güçlü bazik çözeltide ligand farklı bir kişilik sergiledi: kükürt grubu protonunu kaybedip daha reaktif hale geldi ve geri yönde eşleşen bir indirgeme sinyali olmaksızın yalnızca tek bir oksidasyon tepesi gösterdi. Veriler, bu koşullar altında oksitlendiğinde kükürt bölgelerinin birbirine bağlanıp disülfit köprülü dimerler oluşturduğunu, bunun kolayca geri dönmediğini öne sürüyor; bu da basit bir pH değişiminin tüm reaksiyon yolunu nasıl yeniden yönlendirebileceğini vurguluyor.
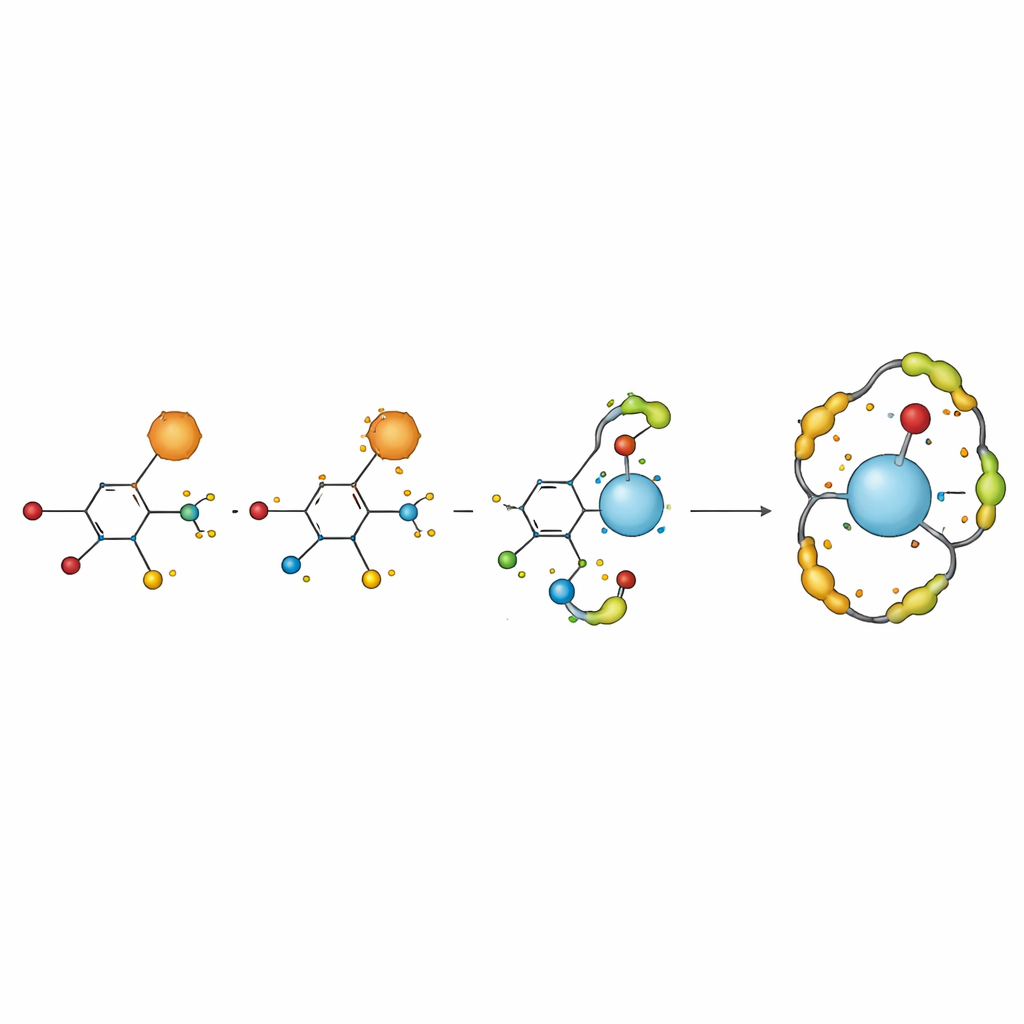
Vanadyumla iş birliği
Bir sonraki adım, H2TIS’in nötre yakın tuz çözeltisinde vanadil iyonlarıyla nasıl etkileştiğini görmekti. Tek başına vanadil iyonu, elektrottaki elektron transferi ile suda hızlı yan reaksiyonlar arasında bir dengeyi yansıtan yalnızca kısmen tersinir bir redoks paterni gösterir. Ligand eklendiğinde voltametri eğrileri kaydı ve daraldı, tepe akımları değişti; bu, metal ile ligandın yeni kompleksler oluşturduğuna dair açık işaretlerdi. Bu kaymaları yerleşik elektrokimyasal eşitliklerle analiz ederek araştırmacılar çözeltide iki ana yapıya kanıt buldu: bir vanadil iyonunun bir H2TIS molekülüne bağlandığı bir tür ve aynı metal merkezinin iki ligand birimiyle çevrelendiği başka bir tür. Bu kompleksler serbest metal iyonuna kıyasla iyileşmiş elektrokimyasal kararlılık gösterdi.
Işıkla kompleks şekillerinin doğrulanması
Elektriksel ölçümleri desteklemek için ekip basit ışık‑soğurma deneylerine başvurdu. Vanadil iyonları ve H2TIS’i farklı oranlarda, toplam miktarı sabit tutarak karıştırdılar ve çözeltilerin belirli bir renkte ışığı ne kadar güçlü emdiğini izlediler. Emilim, metal‑ligand oranlarının bir‑eşi ve bir‑e‑iki kompozisyonlarına karşılık gelen bileşimlerde en yüksek değerlere ulaştı; bu, elektrokimyasal bulgularla örtüştü. Bu verilerden stabilite sabitleri ve ilişkili enerji değişimleri hesaplandı; bunlar kompleks oluşumunun test edilen koşullar altında kendiliğinden ve enerjik olarak elverişli olduğunu gösterdi. Birlikte, voltaj ve spektroskopik sonuçlar suda sağlam vanadil–H2TIS komplekslerinin tutarlı bir resmini çizdi.
Gerçek dünya uygulamaları için anlamı
Uygulama açısından bu çalışma, tek bir ustaca tasarlanmış organik molekülün konulduğu çözeltinin özelliklerine bağlı olarak çok farklı davranabileceğini; tersinir ve tersinmez elektron yolları arasında geçiş yapabileceğini ve vanadyum gibi redoks‑aktif bir metal ile kararlı kompleksler oluşturabileceğini gösteriyor. Yazarlar H2TIS’in asidik, nötr ve bazik ortamlara nasıl yanıt verdiğini ve vanadil iyonlarını ne kadar sıkı bağladığını haritalandırarak, karmaşık ortamlarda metalleri algılamak veya dönüştürmek üzere tasarlanacak gelecekteki malzemeler için tasarım kuralları sunuyor. Bu ayarlanabilir redoks ve bağlanma özellikleri, H2TIS‑temelli sistemleri yeni nesil elektrokimyasal sensörler, katalitik süreçler ve çevresel temizlik teknolojileri için umut verici adaylar haline getiriyor.
Atıf: Mannaa, A.H., Gomaa, E.A., Zaky, R.R. et al. Medium controlled redox activity and coordination behavior of a triazole indolinone ligand with vanadyl lons. Sci Rep 16, 11370 (2026). https://doi.org/10.1038/s41598-026-44306-w
Anahtar kelimeler: vanadyum kompleksleri, elektrokimyasal algılama, redoks kimyası, metal–ligand etkileşimleri, çevresel kataliz