Clear Sky Science · es
Actividad redox controlada de manera media y comportamiento de coordinación de un ligando triazol indolinona con iones vanadilo
Por qué importa este estudio
Agua limpia, medicamentos más seguros y sensores más inteligentes dependen de pequeños auxiliares químicos capaces de captar y liberar iones metálicos a demanda. Este trabajo explora uno de esos auxiliares, una molécula orgánica diseñada llamada H2TIS, y muestra cómo su comportamiento puede ajustarse finamente simplemente cambiando la acidez o basicidad del líquido que la rodea. Al entender cómo esta molécula intercambia electrones y se une al vanadio, un metal de importancia tecnológica y biológica, los investigadores avanzan hacia el diseño de mejores catalizadores, detectores de contaminación y materiales avanzados para baterías o sensores.
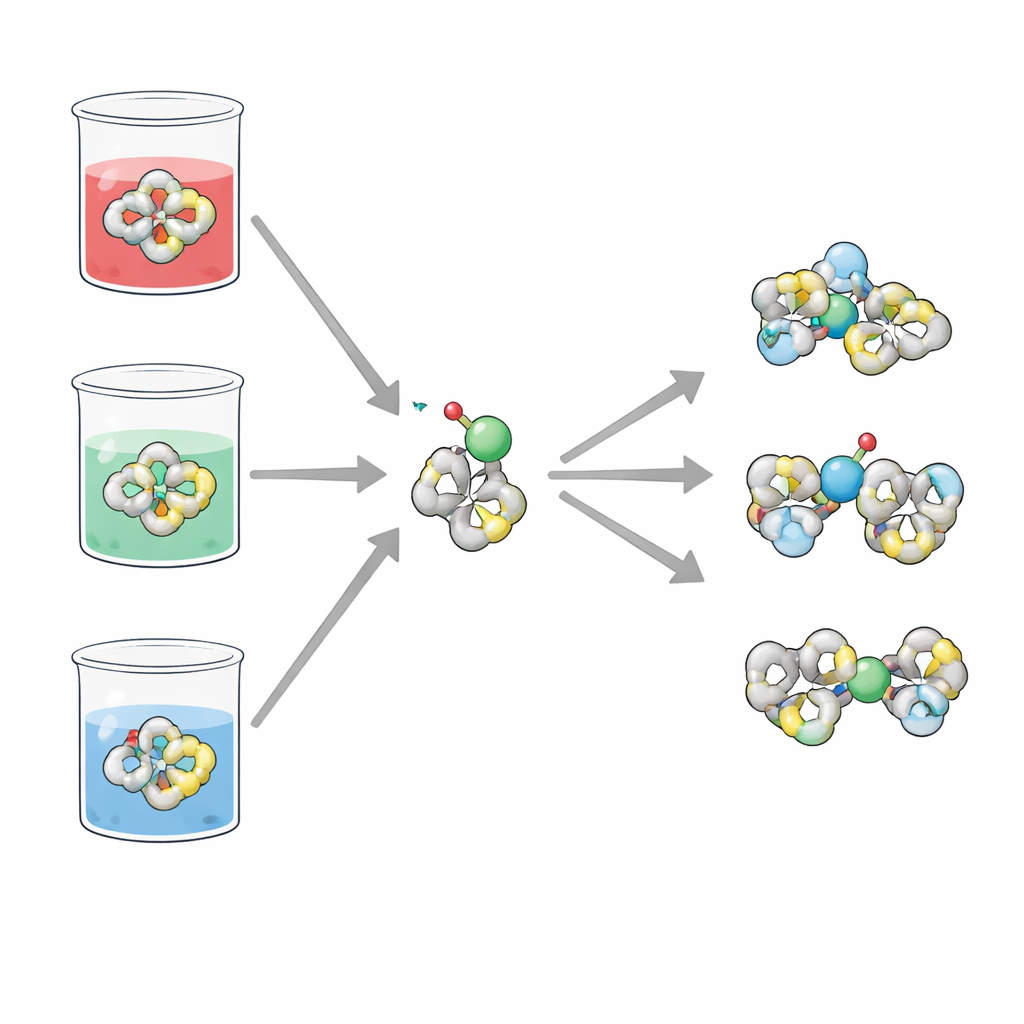
Una molécula auxiliar que cambia de forma
H2TIS es una molécula orgánica compacta construida a partir de varios anillos y grupos químicos que pueden donar pares de electrones. Estos puntos donantes incluyen átomos de azufre, nitrógeno y oxígeno, que en conjunto convierten a H2TIS en una excelente candidata para atrapar iones metálicos. El equipo se centró en cómo actúa este ligando cuando gana o pierde electrones (su actividad redox) y en cómo se coordina con iones vanadilo, una forma común de vanadio en agua. Dado que estos procesos dependen fuertemente de si la solución es ácida, neutra o básica, los investigadores examinaron H2TIS en tres soluciones salinas simples que imitan esas condiciones.
Observando el movimiento de electrones con barridos de voltaje
Para seguir el comportamiento de transferencia electrónica de H2TIS, los científicos usaron voltametría cíclica, una técnica en la que la tensión en un electrodo de carbono se barre hacia adelante y hacia atrás mientras se mide la corriente resultante. En solución ácida, observaron un pico de corriente cuando se añadían electrones al grupo carbonilo de la molécula, convirtiendo efectivamente un doble enlace carbono–oxígeno en una forma más reducida. Al barrer en la dirección opuesta, apareció otro pico ligado a la oxidación en la porción del ligando que contiene azufre. Las posiciones y formas de estos picos, y cómo cambiaban con la concentración y la velocidad de escaneo, indicaron que intervenían tanto transferencias electrónicas como pasos químicos subsiguientes, y que el proceso dependía de la presencia de protones en la solución.
Cómo el líquido circundante cambia la historia
Cuando el mismo ligando se probó en solución neutra, su grupo carbonilo se comportó más como un interruptor bien equilibrado, mostrando un par de picos que casi se reflejaban entre sí. Este patrón señalaba un par redox casi reversible, donde las transferencias de electrones en avance y retroceso están razonablemente igualadas, lo que hace al sistema más estable y predecible. En solución fuertemente básica, sin embargo, el ligando cambió de personalidad: el grupo de azufre perdió su protón, se volvió más reactivo y mostró solo un único pico de oxidación sin una señal de reducción coincidente en el retorno. Los datos sugieren que, una vez oxidado en estas condiciones, los sitios de azufre se enlazan entre sí formando dímeros con puente disulfuro, que no se revierten fácilmente, lo que subraya cómo un simple cambio de pH puede redirigir toda la vía de reacción.
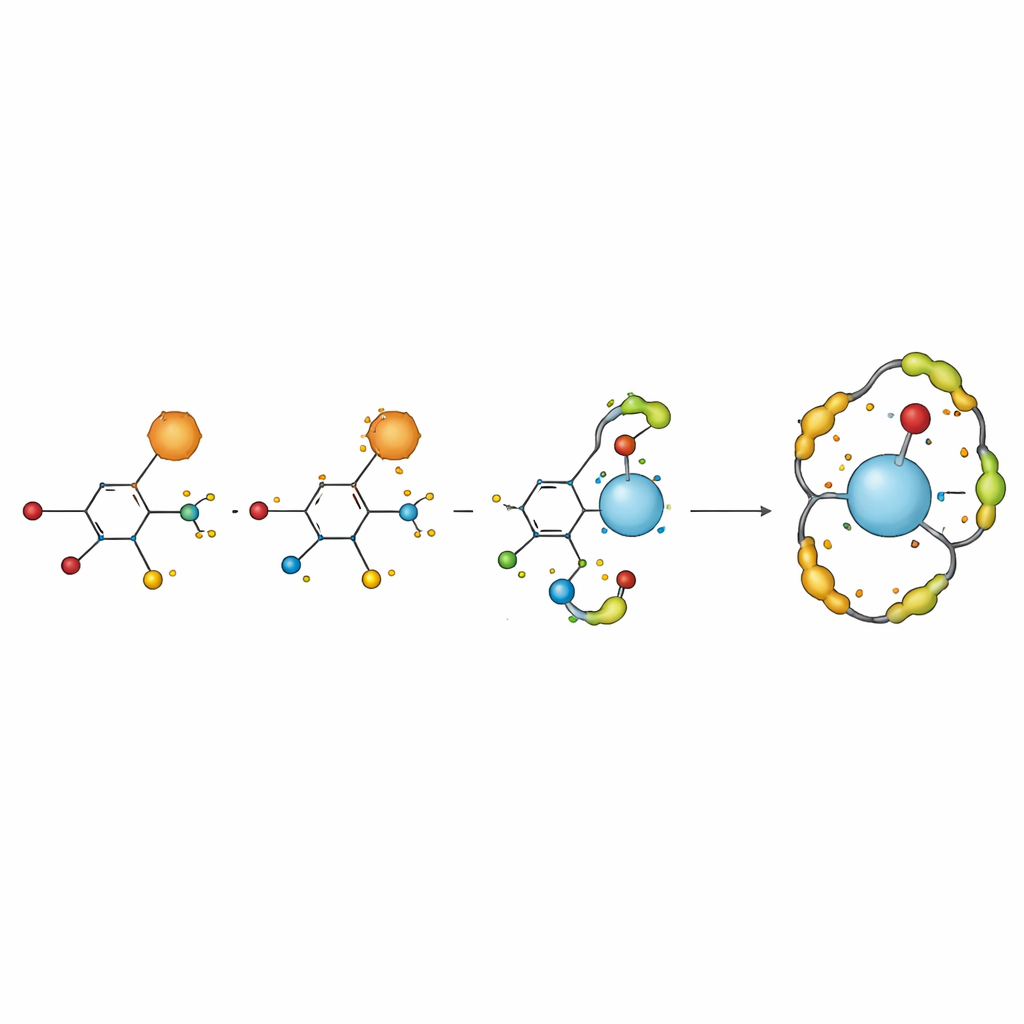
Alianzas con vanadio
El siguiente paso fue ver cómo interactúa H2TIS con iones vanadilo en una solución salina casi neutra. Por sí solo, el ion vanadilo presenta un patrón redox que es solo parcialmente reversible, reflejando un equilibrio entre la transferencia de electrones en el electrodo y reacciones secundarias rápidas en agua. Cuando se añadió el ligando, las curvas voltamétricas se desplazaron y estrecharon, y las corrientes de pico cambiaron, señales claras de que el metal y el ligando estaban formando nuevos complejos. Al analizar estos desplazamientos con ecuaciones electroquímicas establecidas, los investigadores encontraron evidencia de dos estructuras principales en solución: un ion vanadilo unido a una molécula de H2TIS, y otra en la que el mismo centro metálico está rodeado por dos unidades ligando. Estos complejos mostraron una mayor estabilidad electroquímica en comparación con el ion metálico libre.
Confirmando las formas de los complejos con luz
Para respaldar las mediciones eléctricas, el equipo recurrió a experimentos sencillos de absorción de luz. Mezclaron iones vanadilo y H2TIS en distintas proporciones manteniendo constante la cantidad total, y monitorizaron la intensidad con la que las soluciones absorbían luz a un color específico. La absorción alcanzó sus valores máximos en composiciones correspondientes a relaciones metal:ligando de uno a uno y de uno a dos, coincidiendo con los hallazgos electroquímicos. A partir de estos datos calcularon constantes de estabilidad y los cambios energéticos asociados, demostrando que la formación de los complejos es espontánea y termodinámicamente favorable en las condiciones probadas. En conjunto, los resultados voltamétricos y espectroscópicos dibujan un panorama coherente de complejos vanadilo–H2TIS robustos en agua.
Qué significa todo esto para usos reales
En términos prácticos, este estudio muestra que una única molécula orgánica inteligentemente diseñada puede comportarse de manera muy distinta según la solución en la que se encuentre, alternando entre vías electrónicas reversibles e irreversibles y formando complejos estables con un metal redox‑activo como el vanadio. Al cartografiar cómo H2TIS responde a medios ácidos, neutros y básicos y con qué afinidad se une a iones vanadilo, los autores ofrecen reglas de diseño para materiales futuros que necesiten detectar o transformar metales en entornos complejos. Esas propiedades redox y de unión ajustables hacen que los sistemas basados en H2TIS sean candidatos prometedores para sensores electroquímicos de nueva generación, procesos catalíticos y tecnologías de limpieza ambiental.
Cita: Mannaa, A.H., Gomaa, E.A., Zaky, R.R. et al. Medium controlled redox activity and coordination behavior of a triazole indolinone ligand with vanadyl lons. Sci Rep 16, 11370 (2026). https://doi.org/10.1038/s41598-026-44306-w
Palabras clave: complejos de vanadio, detección electroquímica, química redox, interacciones metal–ligando, catálisis ambiental