Clear Sky Science · nl
Beheersbare redoxactiviteit en coördinatiegedrag van een triazool‑indolinoneligand met vanadyloxide‑ionen
Waarom deze studie ertoe doet
Zuiver water, veiligere geneesmiddelen en slimme sensoren vertrouwen allemaal op kleine chemische hulpmiddelen die metaalionen op commando kunnen binden en loslaten. Deze studie onderzoekt zo’n hulpstof, een op maat gemaakt organisch molecuul genaamd H2TIS, en laat zien hoe het gedrag ervan fijn kan worden afgesteld door eenvoudigweg de zuurgraad of basische aard van de omliggende vloeistof te veranderen. Door te begrijpen hoe dit molecuul elektronen uitwisselt en bindt aan vanadium — een technologisch en biologisch belangrijk metaal — komen onderzoekers dichter bij het ontwerpen van betere katalysatoren, detectoren voor vervuiling en geavanceerde batterij‑ of sensormaterialen.
Een hulpstof die van gedaante verandert
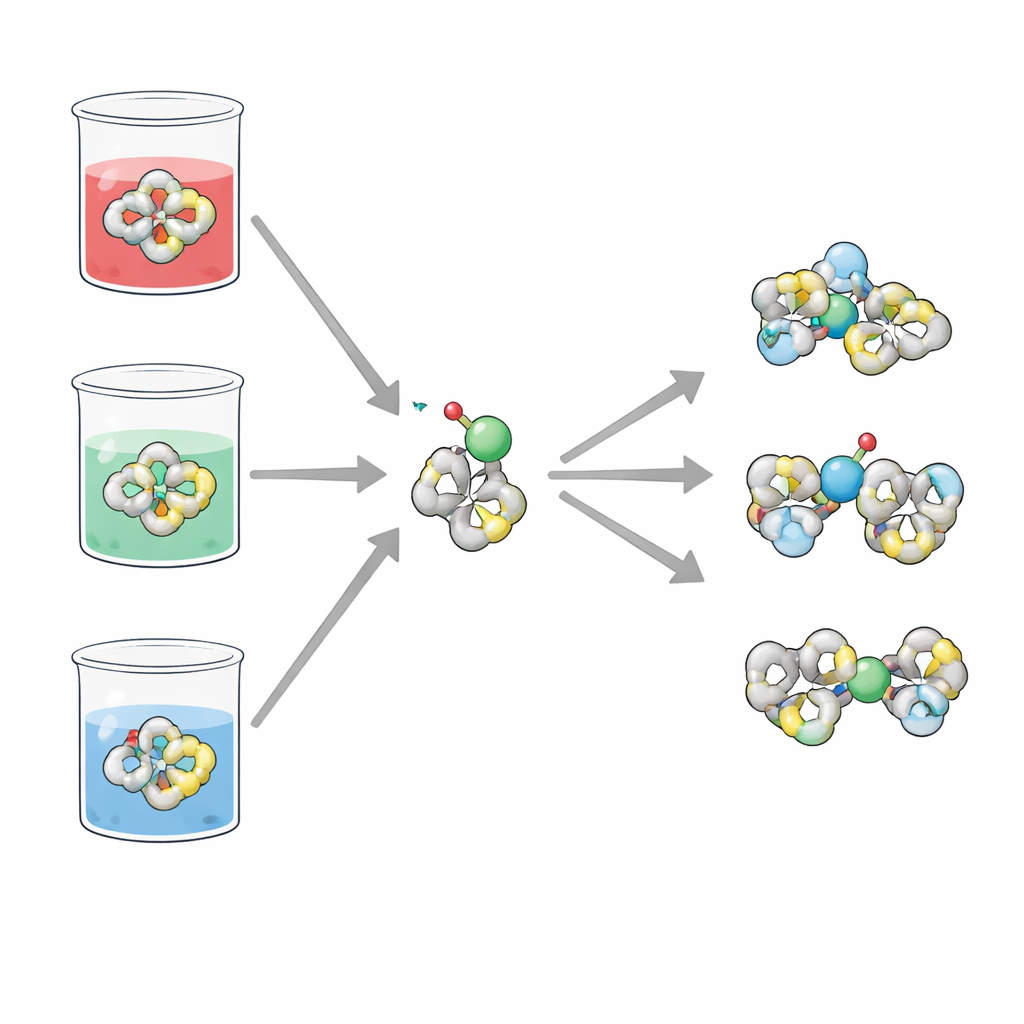
H2TIS is een compact organisch molecuul opgebouwd uit meerdere ringstructuren en chemische groepen die elektronenparen kunnen doneren. Deze “donor”plaatsen omvatten zwavel-, stikstof‑ en zuurstofatomen, die H2TIS samen tot een uitstekende kandidaat maken om metaalionen vast te pakken. Het team richtte zich op het gedrag van deze ligand wanneer hij elektronen wint of verliest (de redoxactiviteit) en hoe hij zich hecht aan vanadyloxide‑ionen, een veelvoorkomende vorm van vanadium in water. Omdat deze processen sterk afhangen van of de oplossing zuur, neutraal of basisch is, onderzochten de onderzoekers H2TIS in drie eenvoudige zoutoplossingen die deze omstandigheden nabootsen.
Het volgen van elektronen met kleine spanningsscans
Om het elektronenverplaatsende gedrag van H2TIS te volgen, gebruikten de wetenschappers cyclische voltammetrie, een techniek waarbij de spanning op een koolstofelektrode heen en weer wordt geveegd terwijl de resulterende stroom wordt gemeten. In zure oplossing observeerden ze een stroompiek wanneer elektronen werden toegevoegd aan de carbonylgroep van het molecuul, waardoor effectief een koolstof‑zuurstof dubbele binding werd gereduceerd. Bij het omgekeerd vegen verscheen een andere piek, gekoppeld aan oxidatie in het zwavelhoudende deel van de ligand. De posities en vormen van deze pieken, en hoe ze veranderden met concentratie en scansnelheid, toonden aan dat zowel elektronenoverdracht als daaropvolgende chemische stappen betrokken waren, en dat het proces afhankelijk was van de aanwezigheid van protonen in de oplossing.
Hoe de omliggende vloeistof het verhaal verandert
Wanneer dezelfde ligand werd getest in neutrale oplossing, gedroeg de carbonylgroep zich meer als een goed in balans zijnde schakelaar, met een paar pieken die bijna elkaars spiegelbeeld waren. Dit patroon duidde op een quasi‑reversibele redoxkoppel, waarbij de voorwaartse en teruggaande elektronenoverdrachten redelijk goed op elkaar afgestemd zijn, wat het systeem stabieler en voorspelbaarder maakt. In sterk basische oplossing veranderde de ligand echter van karakter: de zwavelgroep verloor een proton, werd reactiever en toonde slechts een enkele oxidatiepiek zonder bijbehorende reductiesignaal bij de terugweg. De gegevens suggereren dat, eenmaal geoxideerd onder deze omstandigheden, de zwavelplaatsen aan elkaar koppelen om disulfide‑verbonden dimeren te vormen die zich niet gemakkelijk terugzetten, wat benadrukt hoe een eenvoudige pH‑verandering de hele reactieroute kan omleiden.
Samenwerking met vanadium
De volgende stap was te onderzoeken hoe H2TIS interacteert met vanadyloxide‑ionen in bijna neutrale zoutoplossing. Het vanadyloxide‑ion op zichzelf vertoont een redoxpatroon dat slechts gedeeltelijk reversibel is, wat een balans weerspiegelt tussen elektronenoverdracht aan de elektrode en snelle nevenreacties in water. Wanneer de ligand werd toegevoegd, verschoven en versmalden de voltammetriecurven en veranderden de piekstromen — duidelijke aanwijzingen dat het metaal en de ligand nieuwe complexen vormden. Door deze verschuivingen te analyseren met gevestigde elektrochemische vergelijkingen vonden de onderzoekers bewijs voor twee hoofdstructuren in oplossing: één vanadyloxide‑ion gebonden aan één H2TIS‑molecuul, en een andere waarin hetzelfde metaalcentrum is omgeven door twee ligandeenheden. Deze complexen vertoonden verbeterde elektrochemische stabiliteit vergeleken met het vrije metaalion.
Vorm van complexen bevestigen met licht
Om de elektrische metingen te onderbouwen, voerden de onderzoekers eenvoudige absorptie‑spectroscopie‑experimenten uit. Ze mengden vanadyloxide‑ionen en H2TIS in verschillende verhoudingen terwijl de totale hoeveelheid constant bleef, en hielden bij hoe sterk de oplossingen licht op een specifieke kleur absorbeerden. De absorptie bereikte de hoogste waarden bij samenstellingen die overeenkomen met één‑op‑één en één‑op‑twee metaal‑tot‑ligandverhoudingen, wat overeenkomt met de elektrochemische bevindingen. Uit deze gegevens berekenden ze stabiliteitsconstanten en de bijbehorende energieveranderingen, waaruit bleek dat complexvorming spontaan en energetisch gunstig is onder de geteste omstandigheden. Samen schetsen de spannings‑ en spectroscopische resultaten een consistent beeld van robuuste vanadyloxide–H2TIS‑complexen in water.
Wat het betekent voor toepassingen in de echte wereld
In praktische termen laat deze studie zien dat één slim ontworpen organisch molecuul zich heel anders kan gedragen afhankelijk van de oplossing waarin het zich bevindt, wisselend tussen reversibele en irreversibele elektronenroutes en stabiele complexen vormend met een redoxactief metaal als vanadium. Door in kaart te brengen hoe H2TIS reageert in zure, neutrale en basische media en hoe sterk het vanadyloxide‑ionen bindt, bieden de auteurs ontwerprichtlijnen voor toekomstige materialen die metalen moeten detecteren of omzetten in complexe omgevingen. Zulke instelbare redox‑ en bindingseigenschappen maken H2TIS‑gebaseerde systemen veelbelovend voor de volgende generatie elektrochemische sensoren, katalytische processen en milieusaneringstechnologieën.
Bronvermelding: Mannaa, A.H., Gomaa, E.A., Zaky, R.R. et al. Medium controlled redox activity and coordination behavior of a triazole indolinone ligand with vanadyl lons. Sci Rep 16, 11370 (2026). https://doi.org/10.1038/s41598-026-44306-w
Trefwoorden: vanadiumcomplexen, elektrochemische detectie, redoxchemie, metaal–ligandinteracties, milieukatalyse