Clear Sky Science · pt
Atividade redox moderadamente controlada e comportamento de coordenação de um ligante triazol indolinona com íons vanadilo
Por que este estudo é importante
Água limpa, medicamentos mais seguros e sensores mais inteligentes dependem de pequenas moléculas que podem capturar e liberar íons metálicos sob demanda. Este estudo explora uma dessas moléculas auxiliares, um composto orgânico sob medida chamado H2TIS, e mostra como seu comportamento pode ser ajustado finamente simplesmente alterando a acidez ou basicidade do meio. Ao entender como essa molécula troca elétrons e se liga ao vanádio, um metal de relevância tecnológica e biológica, os pesquisadores avançam na direção de projetar catalisadores melhores, detectores de poluentes e materiais avançados para baterias ou sensores.
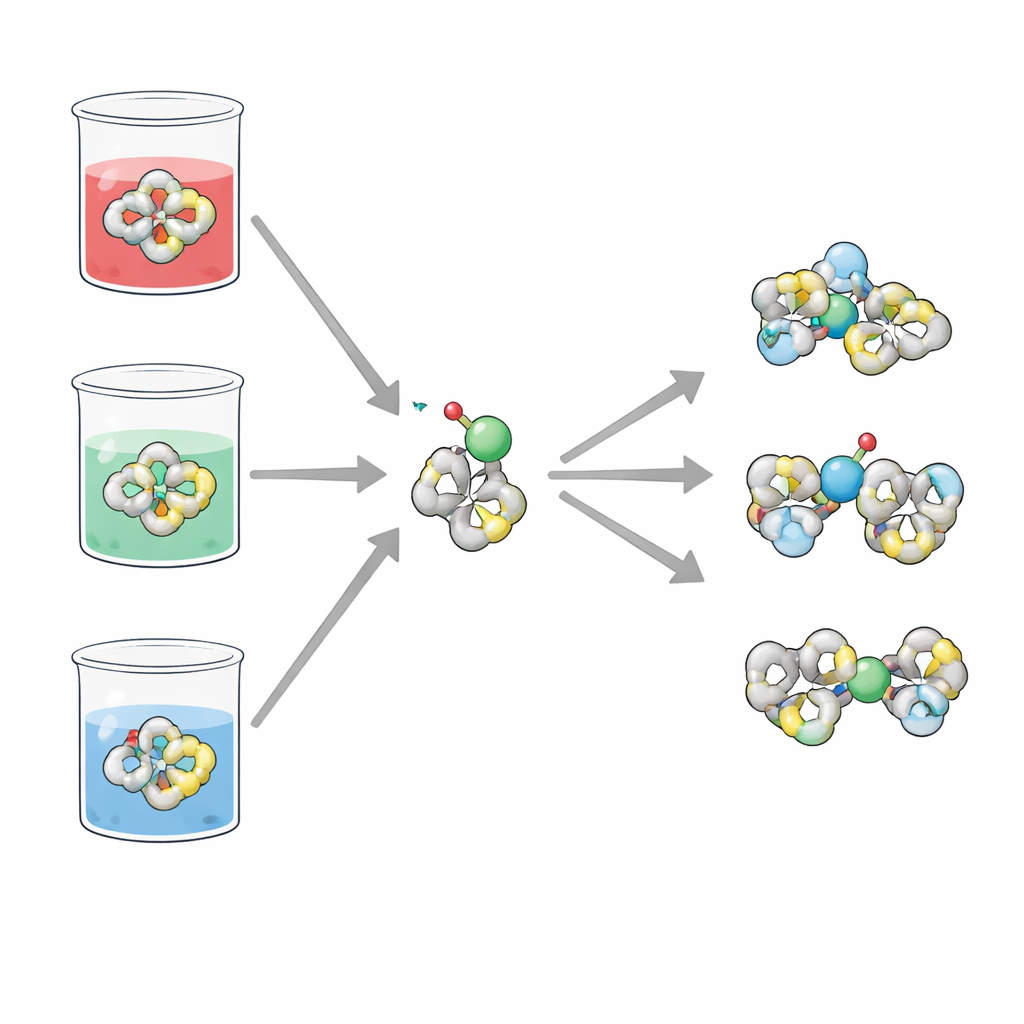
Uma molécula auxiliar que muda de forma
H2TIS é uma molécula orgânica compacta construída a partir de vários anéis e grupos químicos que podem doar pares de elétrons. Esses pontos doadores incluem átomos de enxofre, nitrogênio e oxigênio, que juntos tornam H2TIS uma excelente candidata para se ligar a íons metálicos. A equipe concentrou‑se em como esse ligante se comporta ao ganhar ou perder elétrons (sua atividade redox) e em como se liga a íons vanadilo, uma forma comum de vanádio em água. Como esses processos dependem fortemente de o meio ser ácido, neutro ou básico, os pesquisadores investigaram H2TIS em três soluções salinas simples que mimetizam essas condições.
Observando elétrons se moverem com varreduras de tensão
Para acompanhar o comportamento de movimentação de elétrons de H2TIS, os cientistas usaram voltametria cíclica, uma técnica em que a tensão em um eletrodo de carbono é varrida para frente e para trás enquanto a corrente resultante é medida. Em solução ácida, observaram um pico de corrente quando elétrons foram adicionados ao grupo carbonila da molécula, convertendo efetivamente uma ligação dupla carbono‑oxigênio em uma forma mais reduzida. Ao varrer na direção oposta, apareceu outro pico, ligado à oxidação na parte do ligante que contém enxofre. As posições e formas desses picos, e como mudavam com a concentração e a velocidade de varredura, mostraram que tanto a transferência de elétrons quanto passos químicos subsequentes estavam envolvidos, e que o processo dependia da presença de prótons na solução.
Como o líquido ao redor altera a história
Quando o mesmo ligante foi testado em solução neutra, seu grupo carbonila comportou‑se mais como um interruptor bem equilibrado, exibindo um par de picos quase espelhados. Esse padrão sinalizou um par redox quase reversível, em que as transferências de elétrons direta e reversa são razoavelmente equilibradas, tornando o sistema mais estável e previsível. Em solução fortemente básica, entretanto, o ligante mudou de personalidade: o grupo de enxofre perdeu seu próton, tornou‑se mais reativo e apresentou apenas um pico de oxidação sem sinal correspondente de redução no retorno. Os dados sugerem que, uma vez oxidado sob essas condições, os sítios de enxofre se ligam entre si para formar dímeros com pontes dissulfeto, que não regridem facilmente, ressaltando como uma simples mudança de pH pode redirecionar toda a via de reação.
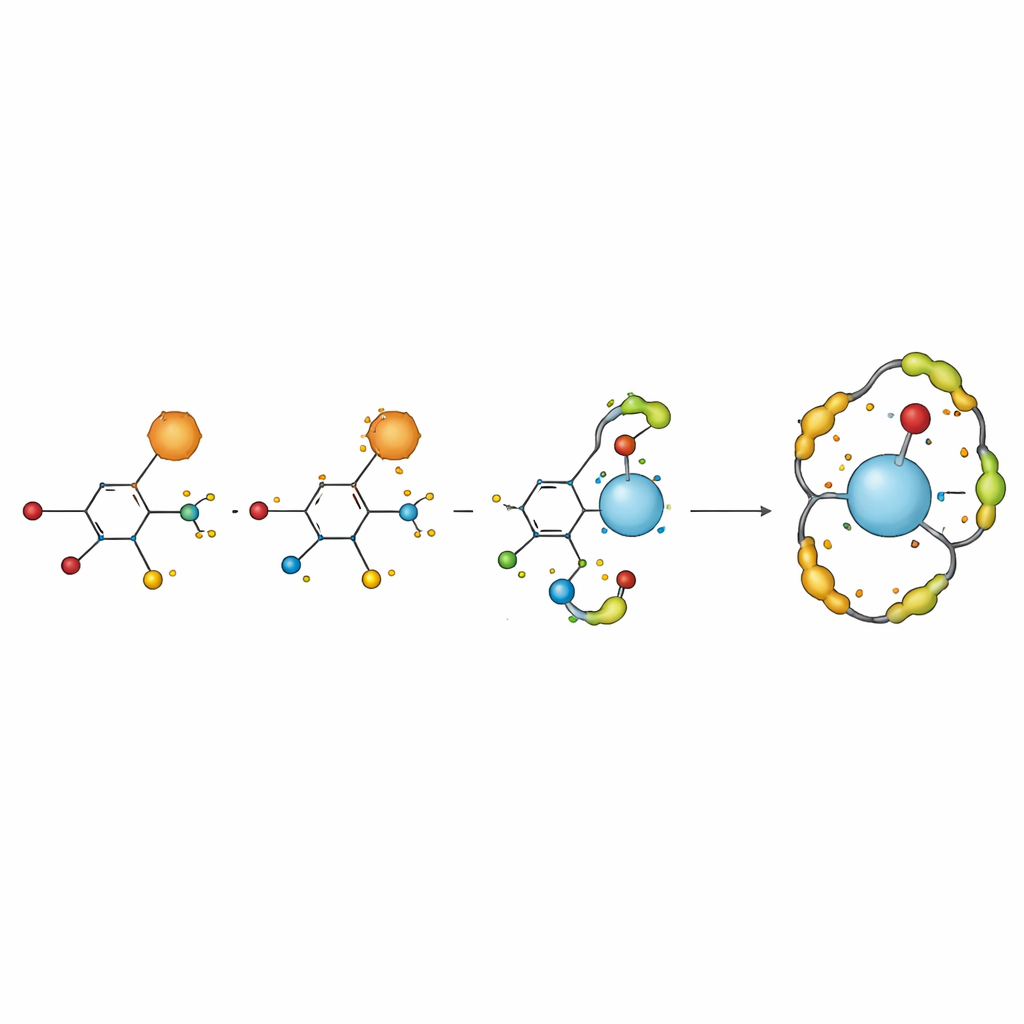
Fazendo equipe com o vanádio
O próximo passo foi ver como H2TIS interage com íons vanadilo em solução salina quase neutra. Por si só, o íon vanadilo mostra um padrão redox que é apenas parcialmente reversível, refletindo um equilíbrio entre transferência de elétrons no eletrodo e reações secundárias rápidas na água. Quando o ligante foi adicionado, as curvas de voltametria deslocaram‑se e afinaram‑se, e as correntes de pico mudaram — sinais claros de que o metal e o ligante estavam formando novos complexos. Ao analisar esses deslocamentos com equações eletroquímicas estabelecidas, os pesquisadores encontraram evidências para duas estruturas principais em solução: um íon vanadilo ligado a uma molécula de H2TIS e outra em que o mesmo centro metálico é envolvido por duas unidades do ligante. Esses complexos exibiram estabilidade eletroquímica melhorada em comparação com o íon metálico livre.
Confirmando as formas dos complexos com luz
Para respaldar as medidas elétricas, a equipe recorreu a experimentos simples de absorção de luz. Eles misturaram íons vanadilo e H2TIS em diferentes proporções mantendo a quantidade total constante e monitoraram quão fortemente as soluções absorviam luz em uma cor específica. A absorção atingiu seus valores máximos em composições correspondentes a razões metal:ligante de 1:1 e 1:2, coincidindo com os achados eletroquímicos. A partir desses dados, calcularam constantes de estabilidade e as mudanças de energia associadas, mostrando que a formação dos complexos é espontânea e energeticamente favorável nas condições testadas. Juntos, os resultados voltamétricos e espectroscópicos desenham um quadro consistente de complexos vanadilo–H2TIS robustos em água.
O que tudo isso significa para aplicações reais
Em termos práticos, este estudo mostra que uma única molécula orgânica inteligentemente projetada pode se comportar de maneiras muito diferentes dependendo do meio em que é colocada, alternando entre vias eletroquímicas reversíveis e irreversíveis e formando complexos estáveis com um metal redox‑ativo como o vanádio. Ao mapear como H2TIS responde a meios ácidos, neutros e básicos e quão firmemente se liga aos íons vanadilo, os autores fornecem regras de projeto para materiais futuros que precisam detectar ou transformar metais em ambientes complexos. Essas propriedades redox e de ligação ajustáveis tornam sistemas à base de H2TIS candidatos promissores para sensores eletroquímicos de nova geração, processos catalíticos e tecnologias de remediação ambiental.
Citação: Mannaa, A.H., Gomaa, E.A., Zaky, R.R. et al. Medium controlled redox activity and coordination behavior of a triazole indolinone ligand with vanadyl lons. Sci Rep 16, 11370 (2026). https://doi.org/10.1038/s41598-026-44306-w
Palavras-chave: complexos de vanádio, sensoriamento eletroquímico, química redox, interações metal–ligante, catálise ambiental