Clear Sky Science · sv
Medium kontrollerad redoxaktivitet och koordineringsbeteende hos en triazol‑indolinon ligand med vanadyljoner
Varför denna studie är viktig
Rent vatten, säkrare läkemedel och smartare sensorer bygger alla på små kemiska hjälpämnen som kan fånga och släppa metalljoner på kommando. Denna studie undersöker ett sådant hjälpämne, en skräddarsydd organisk förening kallad H2TIS, och visar hur dess beteende kan finjusteras enbart genom att ändra surhetsgraden i omgivande vätska. Genom att förstå hur denna molekyl utbyter elektroner och binder vanadin, ett tekniskt och biologiskt viktigt metall, kommer forskare närmare att designa bättre katalysatorer, detektorer för föroreningar samt avancerade batteri‑ och sensormaterial.
En formföränderlig hjälparmolekyl
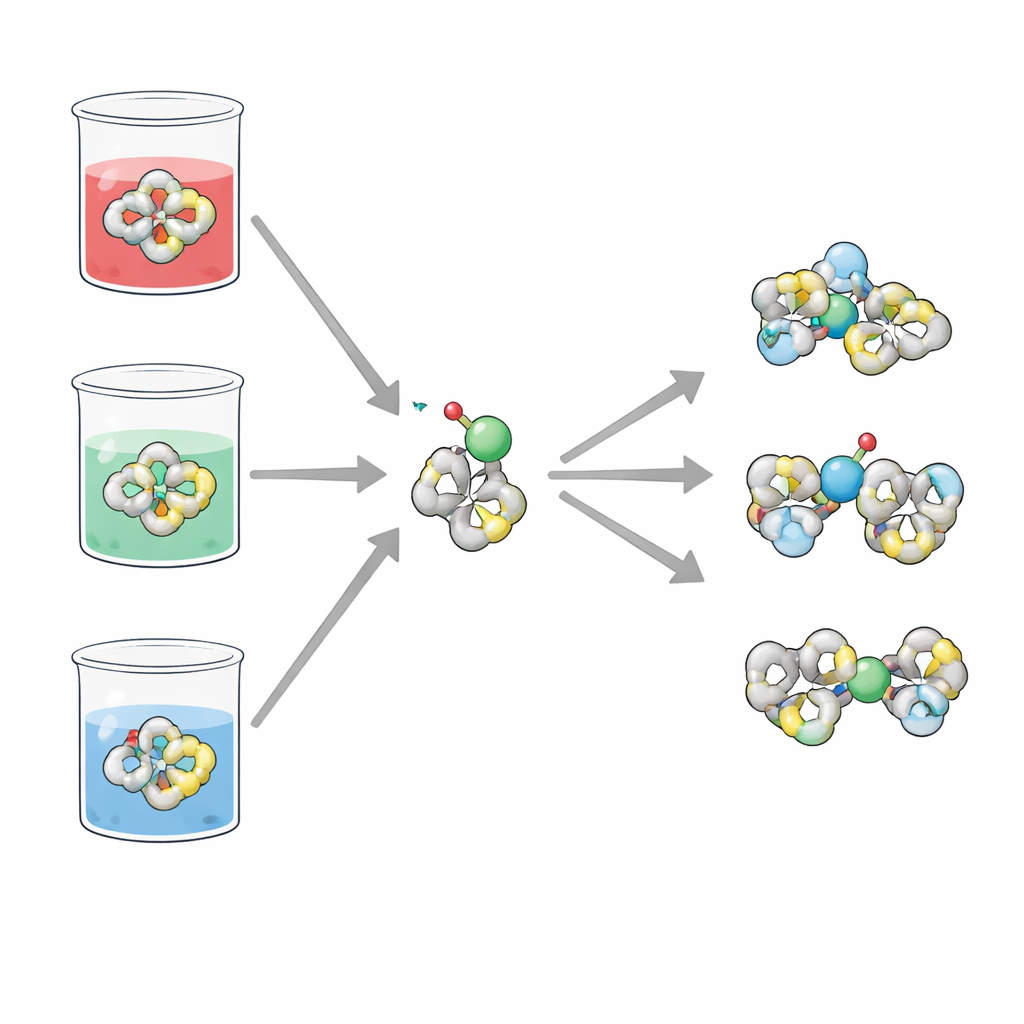
H2TIS är en kompakt organisk molekyl uppbyggd av flera ringstrukturer och kemiska grupper som kan donera elektronpar. Dessa ”donatorställen” inkluderar svavel, kväve och syreatomer, vilket tillsammans gör H2TIS till en utmärkt kandidat för att greppa metalljoner. Forskargruppen koncentrerade sig på hur denna ligand beter sig när den får eller förlorar elektroner (dess redoxaktivitet) och hur den fäster vid vanadyl‑joner, en vanlig form av vanadin i vatten. Eftersom dessa processer starkt påverkas av om lösningen är sur, neutral eller basisk, undersökte man H2TIS i tre enkla saltslösningar som efterliknar dessa förhållanden.
Att följa elektronrörelser med små spänningsvep
För att spåra H2TIS elektroniska beteende använde forskarna cyklisk voltammetri, en teknik där spänningen på en kollektrod sveps fram och tillbaka medan den resulterande strömmen mäts. I sur lösning observerade de en strömmaxima när elektroner tillfördes karbonylgruppen i molekylen, vilket i praktiken omvandlar en kol‑syre dubbelbindning till en mer reducerad form. Vid svep i motsatt riktning dök en annan topp upp, kopplad till oxidation i den svavelinnehållande delen av liganden. Topparnas lägen och former, och hur de ändrades med koncentration och svephastighet, visade att både elektronöverföring och efterföljande kemiska steg var inblandade, och att processen var beroende av protoner i lösningen.
Hur omgivande vätska ändrar förloppet
När samma ligand testades i neutral lösning uppträdde karbonylgruppen mer som en välbalanserad brytare, med ett par toppar som nästan speglade varandra. Detta mönster signalerade ett kvasi‑reversibelt redoxpar, där framåt‑ och bakåtgående elektronöverföringar är relativt väl matchade, vilket gör systemet mer stabilt och förutsägbart. I starkt basisk lösning ändrade liganden däremot karaktär: svavelgruppen förlorade sin proton, blev mer reaktiv och visade endast en enda oxidationsstopp med ingen motsvarande reduktionssignal på återvägen. Data tyder på att en gång oxiderade under dessa förhållanden länkar sig svavelställena ihop för att bilda disulfid‑bryggade dimerer som inte lätt återbildas, vilket belyser hur en enkel pH‑förändring kan styra hela reaktionsvägen.
Samarbete med vanadin
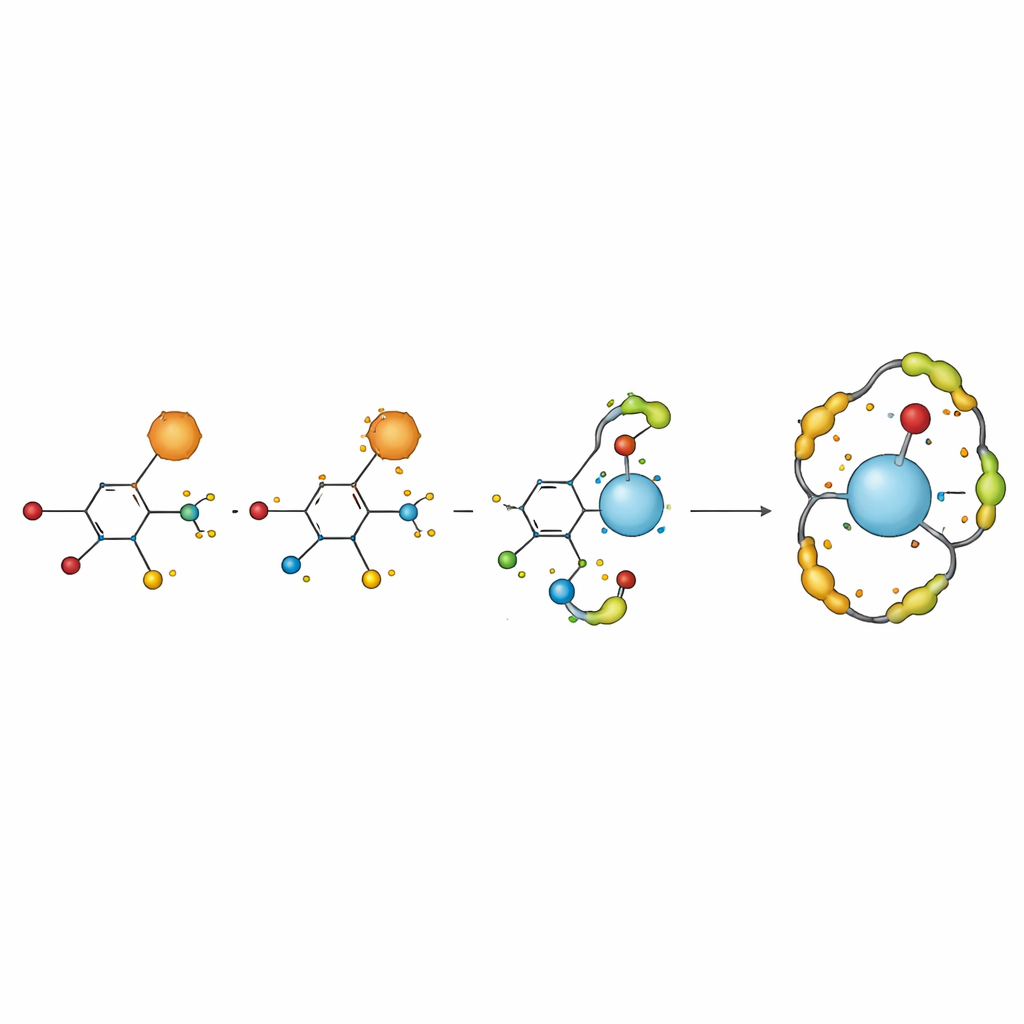
Nästa steg var att se hur H2TIS interagerar med vanadyl‑joner i nära‑neutral saltslösning. Själv visar vanadyljonen ett redoxmönster som bara delvis är reversibelt, vilket speglar en balans mellan elektronöverföring vid elektroden och snabba sidoreaktioner i vatten. När liganden tillsattes försköts och smalnade voltammetrikurvorna, och toppströmmarna förändrades — tydliga tecken på att metall och ligand bildade nya komplex. Genom att analysera dessa förskjutningar med etablerade elektrokemiska formler fann forskarna bevis för två huvudsakliga strukturer i lösning: en vanadyljon bunden till en H2TIS‑molekyl och en annan där samma metallcenter omsluts av två ligand‑enheter. Dessa komplex visade förbättrad elektrokemisk stabilitet jämfört med den fria metalljonen.
Bekräftelse av komplexens former med ljus
För att stödja de elektriska mätningarna använde teamet enkla ljusabsorptionsförsök. De blandade vanadyljoner och H2TIS i olika förhållanden samtidigt som totala mängden hölls konstant, och övervakade hur kraftigt lösningarna absorberade ljus vid en specifik färg. Absorptionen nådde högst värden vid sammansättningar som motsvarade ett‑till‑ett och ett‑till‑två metall‑till‑ligand‑kvoter, i linje med de elektrokemiska fynden. Från dessa data beräknade de stabilitetskonstanter och de associerade energiändringarna, vilket visade att komplexbildningen är spontan och energetiskt fördelaktig under de testade förhållandena. Tillsammans ger spännings‑ och spektroskopiska resultat en sammanhängande bild av robusta vanadyl–H2TIS‑komplex i vatten.
Vad det betyder för praktisk användning
I praktiska termer visar denna studie att en enda, genomtänkt organisk molekyl kan uppträda mycket olika beroende på vilken lösning den placeras i, växla mellan reversibla och irreversibla elektronvägar och bilda stabila komplex med en redoxaktiv metall som vanadin. Genom att kartlägga hur H2TIS reagerar i sura, neutrala och basiska medier och hur starkt den binder vanadyljoner, erbjuder författarna designregler för framtida material som behöver detektera eller omvandla metaller i komplexa miljöer. Sådana ställbara redox‑ och bindningsegenskaper gör H2TIS‑baserade system till lovande kandidater för nästa generations elektrokemiska sensorer, katalytiska processer och tekniker för miljörengöring.
Citering: Mannaa, A.H., Gomaa, E.A., Zaky, R.R. et al. Medium controlled redox activity and coordination behavior of a triazole indolinone ligand with vanadyl lons. Sci Rep 16, 11370 (2026). https://doi.org/10.1038/s41598-026-44306-w
Nyckelord: vanadiumkomplex, elektrokemisk detektion, redoxkemi, metall–ligand‑interaktioner, miljökatalys