Clear Sky Science · pl
Umiarkowana kontrola aktywności redoks i zachowania koordynacyjnego ligandu triazolowego indolinonowego z jonami wanadylu
Dlaczego to badanie ma znaczenie
Czysta woda, bezpieczniejsze leki i inteligentniejsze sensory opierają się na drobnych chemicznych pomocnikach, które potrafią przejmować i uwalniać jony metali na żądanie. W tym badaniu przyjrzano się jednemu z takich związków — zaprojektowanej cząsteczce organicznej H2TIS — i pokazano, jak jej zachowanie można precyzyjnie regulować przez zmianę kwasowości lub zasadowości otaczającego roztworu. Zrozumienie sposobu, w jaki ta cząsteczka wymienia elektrony i kompleksuje wanad — metal istotny technologicznie i biologicznie — przybliża naukowców do projektowania lepszych katalizatorów, detektorów zanieczyszczeń oraz zaawansowanych materiałów do baterii i sensorów.
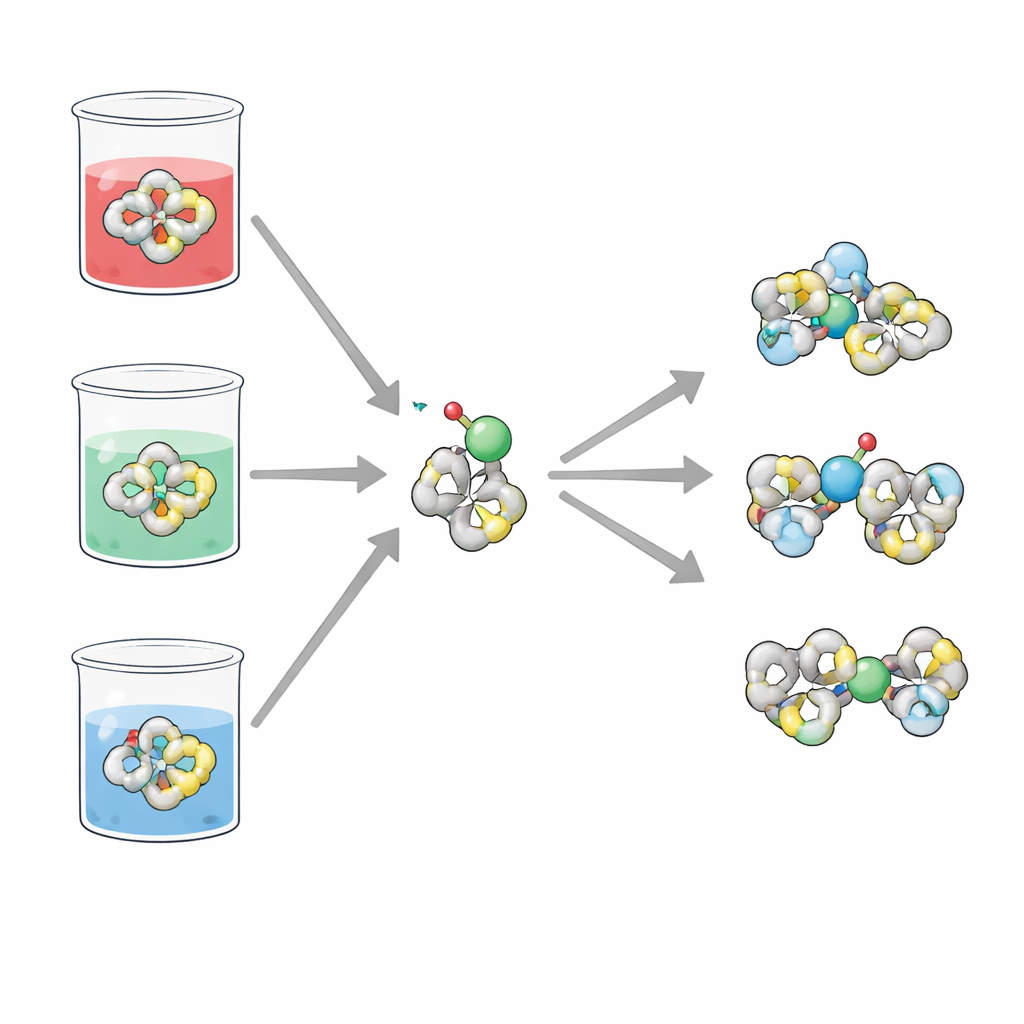
Pomocnik zmieniający kształt
H2TIS to zwarta cząsteczka organiczna zbudowana z kilku pierścieni i grup chemicznych zdolnych do oddawania par elektronów. Miejsca te — zawierające atomy siarki, azotu i tlenu — czynią H2TIS doskonałym kandydatem do chwycenia jonów metali. Zespół skupił się na tym, jak ligand zachowuje się przy przyjmowaniu lub oddawaniu elektronów (aktywność redoks) oraz jak wiąże się z jonami wanadylu, powszechną postacią wanadu w wodzie. Ponieważ te procesy silnie zależą od tego, czy roztwór jest kwaśny, obojętny czy zasadowy, badacze przeprowadzili pomiary H2TIS w trzech prostych roztworach solnych naśladujących te warunki.
Obserwowanie ruchu elektronów drobnymi zamiataniami napięcia
Aby śledzić zachowanie przenoszenia elektronów przez H2TIS, naukowcy zastosowali woltametrię cykliczną — technikę, w której napięcie na elektrodzie węglowej jest cyklicznie zmieniane, a mierzy się wynikający z tego prąd. W roztworze kwaśnym zaobserwowano pik prądu podczas dodawania elektronów do grupy karbonylowej cząsteczki, co odpowiednio redukowało wiązanie podwójne węgiel–tlen. Przy odwrotnym zamiataniu pojawił się inny pik związany z utlenianiem fragmentu ligandu zawierającego siarkę. Pozycje i kształty tych pików oraz ich zależność od stężenia i prędkości skanowania wskazywały, że oprócz transferu elektronów zachodzą także następujące kroki chemiczne, a cały proces zależy od obecności protonów w roztworze.
Jak otaczający płyn zmienia przebieg reakcji
W roztworze obojętnym ta sama grupa karbonylowa zachowywała się jak lepiej zrównoważony przełącznik, dając parę pików niemal lustrzanych. Wzór ten świadczył o quasi‑odwracalnej parze redoks, gdzie transfery elektronów w obu kierunkach są względnie dobrze dopasowane, co czyni system bardziej stabilnym i przewidywalnym. W silnie zasadowym roztworze ligand zmieniał jednak „osobowość”: grupa siarkowa traciła proton, stawała się bardziej reaktywna i wykazywała tylko pojedynczy pik utleniania bez odpowiadającego sygnału redukcji przy powrocie. Dane sugerują, że po utlenieniu w tych warunkach miejsca siarkowe łączą się w dimery z mostkami disiarczkowymi, które nie cofają się łatwo, co podkreśla, jak prosta zmiana pH może przekierować cały tor reakcji.
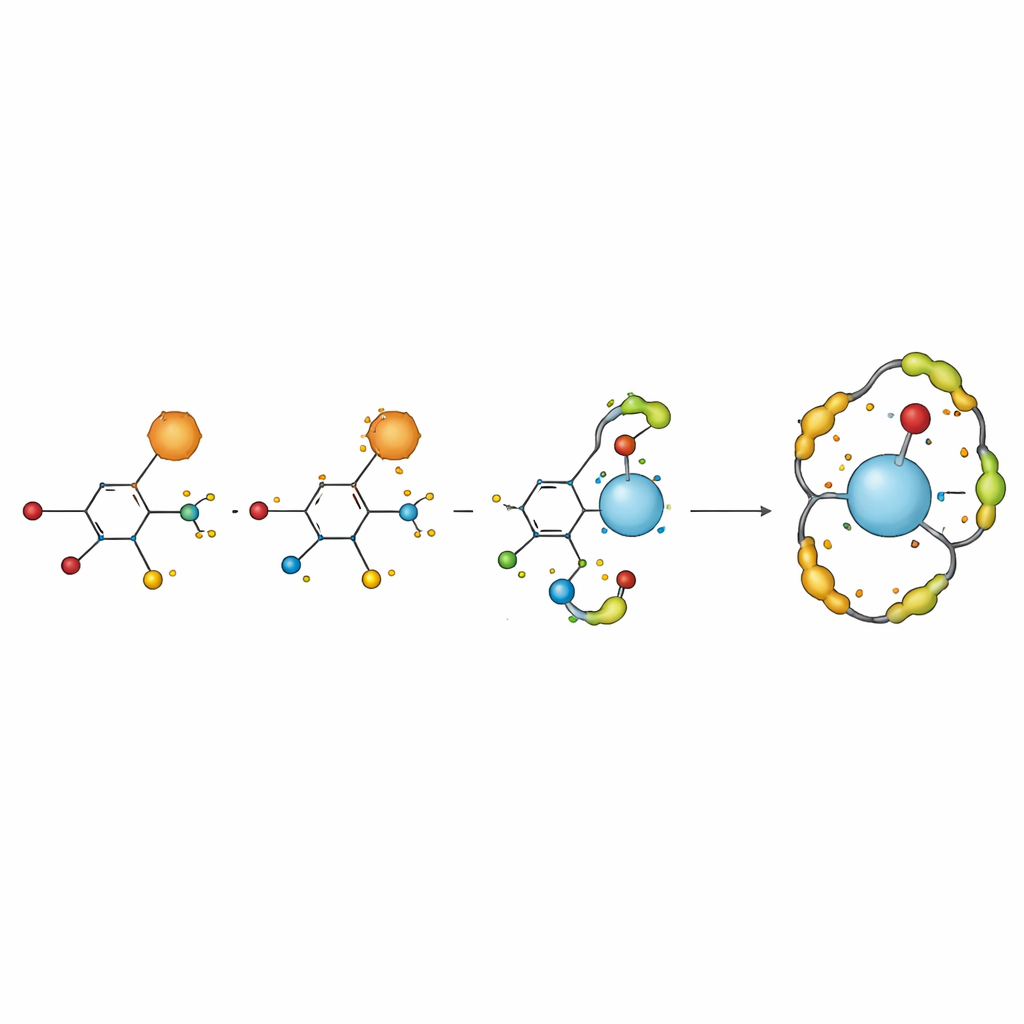
Współpraca z wanadem
Następnym krokiem było zbadanie, jak H2TIS oddziałuje z jonami wanadylu w warunkach zbliżonych do obojętnych. Sam jon wanadylowy wykazuje wzorzec redoks jedynie częściowo odwracalny, co odzwierciedla równowagę między transferem elektronów na elektrodzie a szybkimi reakcjami ubocznymi w wodzie. Po dodaniu ligandu krzywe woltametryczne przesunęły się i zawęziły, a prądy szczytowe zmieniły się — wyraźne sygnały tworzenia nowych kompleksów metalu z ligandem. Analizując te przesunięcia przy użyciu ustalonych równań elektrochemicznych, badacze znaleźli dowody na dwie główne struktury w roztworze: jeden jon wanadylu związany z jedną cząsteczką H2TIS oraz wariant, w którym to samo centrum metaliczne otoczone jest przez dwie jednostki ligandu. Te kompleksy wykazywały lepszą stabilność elektrochemiczną w porównaniu z wolnym jonem metalu.
Potwierdzanie kształtów kompleksów światłem
Aby uzupełnić pomiary elektryczne, zespół sięgnął po proste eksperymenty absorpcji światła. Mieszali jony wanadylu i H2TIS w różnych stosunkach, utrzymując stałą całkowitą ilość substancji, i monitorowali, jak silnie roztwory absorbowały światło przy określonym kolorze. Absorpcja osiągała maksima przy składach odpowiadających stosunkom metalu do ligandu 1:1 i 1:2, co zgadzało się z wynikami elektrochemicznymi. Na podstawie tych danych obliczono stałe stabilności i związane z nimi zmiany energetyczne, wykazując, że tworzenie kompleksów jest spontaniczne i termodynamicznie korzystne w badanych warunkach. Razem wyniki woltametryczne i spektroskopowe kreślą spójny obraz trwałych kompleksów wanadyl–H2TIS w wodzie.
Co to oznacza dla zastosowań praktycznych
W praktycznym ujęciu badanie pokazuje, że pojedyncza, sprytnie zaprojektowana cząsteczka organiczna może zachowywać się bardzo różnie w zależności od medium, w którym się znajduje — przełączając się między odwracalnymi i nieodwracalnymi torami elektronowymi i tworząc stabilne kompleksy z redoks‑czynnym metalem, takim jak wanad. Mapując reakcje H2TIS w warunkach kwaśnych, obojętnych i zasadowych oraz określając siłę wiązania z jonami wanadylu, autorzy dostarczają zasad projektowania przyszłych materiałów przeznaczonych do wykrywania lub przekształcania metali w złożonych środowiskach. Takie regulowane właściwości redoks i wiązania czynią systemy oparte na H2TIS obiecującymi kandydatami do następnej generacji sensorów elektrochemicznych, procesów katalitycznych i technologii oczyszczania środowiska.
Cytowanie: Mannaa, A.H., Gomaa, E.A., Zaky, R.R. et al. Medium controlled redox activity and coordination behavior of a triazole indolinone ligand with vanadyl lons. Sci Rep 16, 11370 (2026). https://doi.org/10.1038/s41598-026-44306-w
Słowa kluczowe: kompleksy wanadu, czujniki elektrochemiczne, chemia redoks, interakcje metal–ligand, kataliza środowiskowa