Clear Sky Science · de
Mäßig gesteuerte Redoxaktivität und Koordinationsverhalten eines Triazol‑Indolinon‑Liganden mit Vanadyl‑Ionen
Warum diese Studie wichtig ist
Sauberes Wasser, sichere Medikamente und intelligentere Sensoren beruhen alle auf winzigen chemischen Helfern, die Metallionen auf Abruf greifen und wieder freigeben können. Diese Studie untersucht einen solchen Helfer—ein maßgeschneidertes organisches Molekül namens H2TIS—und zeigt, wie sein Verhalten allein durch Änderung der Säure‑ oder Basizität der umgebenden Lösung feinabgestimmt werden kann. Indem die Forscher nachvollziehen, wie dieses Molekül Elektronen austauscht und an Vanadium bindet—einem technologisch und biologisch wichtigen Metall—kommen sie der Entwicklung besserer Katalysatoren, Verschmutzungsdetektoren und fortschrittlicher Batterie‑ oder Sensormaterialien näher.
Ein formwandelnder Helfer
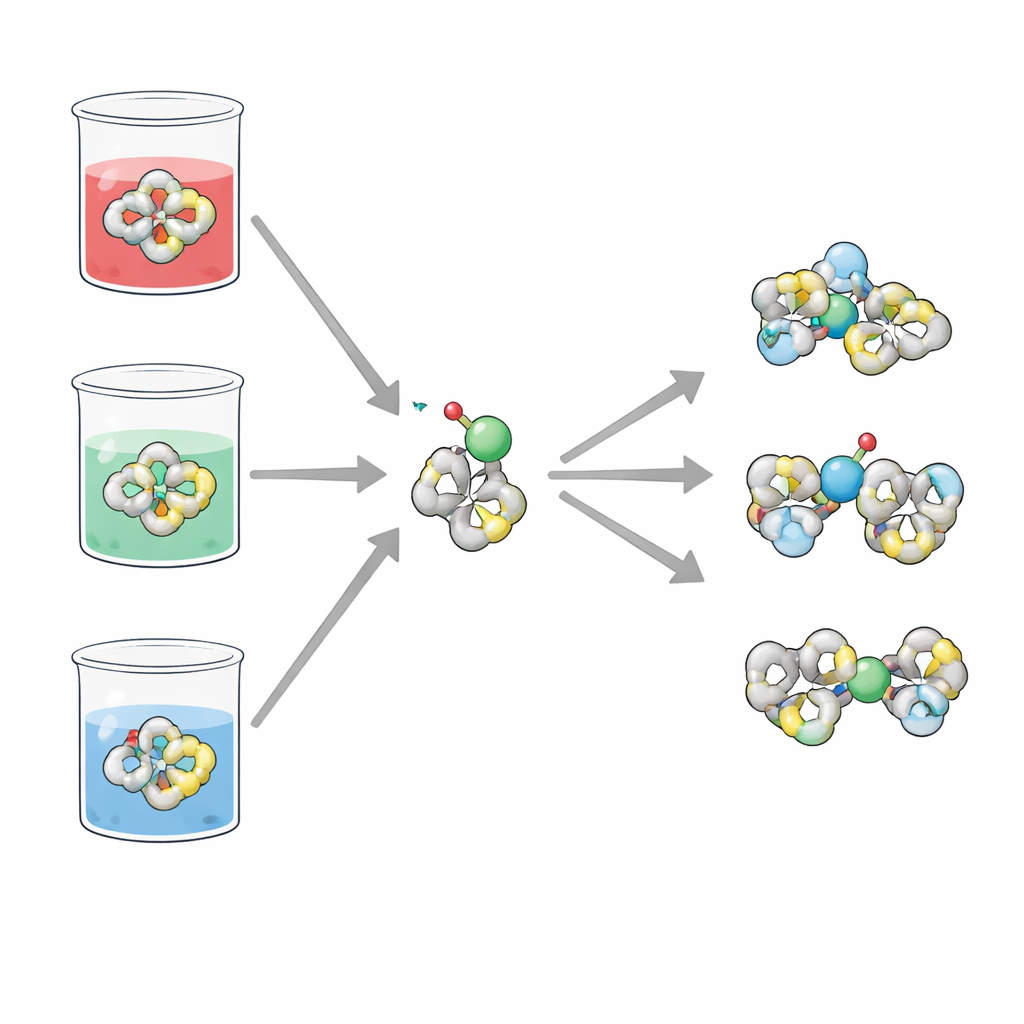
H2TIS ist ein kompaktes organisches Molekül, aufgebaut aus mehreren Ringsystemen und chemischen Gruppen, die Elektronenpaare abgeben können. Zu diesen „Donor“-Stellen gehören Schwefel‑, Stickstoff‑ und Sauerstoffatome, die zusammen H2TIS zu einem hervorragenden Kandidaten für das Fassgreifen von Metallionen machen. Das Team konzentrierte sich auf das Verhalten dieses Liganden beim Gewinnen oder Verlieren von Elektronen (seine Redoxaktivität) und darauf, wie er an Vanadyl‑Ionen bindet, eine häufige Vanadium‑Form in Wasser. Da diese Prozesse stark davon abhängen, ob die Lösung sauer, neutral oder basisch ist, untersuchten die Forschenden H2TIS in drei einfachen Salzlösungen, die diese Bedingungen nachahmen.
Elektronen beobachten mit kleinen Spannungssweeps
Um das elektronentransportierende Verhalten von H2TIS zu verfolgen, verwendeten die Wissenschaftler zyklische Voltammetrie, eine Technik, bei der die Spannung an einer Kohlenstoffelektrode hin und her gefahren wird, während der resultierende Strom gemessen wird. In saurer Lösung beobachteten sie einen Strompeak, wenn dem Carbonyl der Verbindung Elektronen hinzugefügt wurden, wodurch eine C=O‑Doppelbindung in eine stärker reduzierte Form überführt wurde. Beim Zurückfahren der Spannung erschien ein weiterer Peak, der mit der Oxidation am schwefelhaltigen Teil des Liganden verknüpft ist. Die Positionen und Formen dieser Peaks sowie deren Abhängigkeit von Konzentration und Scan‑Geschwindigkeit zeigten, dass sowohl Elektronentransfer als auch nachfolgende chemische Schritte beteiligt sind und dass der Prozess von der Anwesenheit von Protonen in der Lösung abhängt.
Wie das umgebende Lösungsmittel die Vorgänge verändert
Wurde derselbe Ligand in neutraler Lösung getestet, verhielt sich seine Carbonylgruppe eher wie ein gut ausbalancierter Schalter und zeigte ein Peak‑Paar, das sich nahezu spiegelte. Dieses Muster deutet auf ein quasi‑reversibles Redox‑Paar hin, bei dem Vorwärts‑ und Rückwärts‑Elektronentransfers einigermaßen gut aufeinander abgestimmt sind, wodurch das System stabiler und berechenbarer wird. In stark basischer Lösung änderte der Ligand jedoch sein Verhalten: die Schwefelgruppe verlor ihr Proton, wurde reaktiver und zeigte nur einen einzelnen Oxidationspeak ohne passende Reduktionssignale auf dem Rückweg. Die Daten sprechen dafür, dass unter diesen Bedingungen die oxidierten Schwefelzentren miteinander verknüpfen und Disulfid‑bridged Dimere bilden, die sich nicht leicht zurückbilden—ein Beispiel dafür, wie eine einfache pH‑Änderung den gesamten Reaktionsweg umleiten kann.
Zusammenarbeit mit Vanadium
Als nächstes untersuchten die Forschenden, wie H2TIS mit Vanadyl‑Ionen in nahezu neutraler Salzlösung interagiert. Das freie Vanadyl‑Ion zeigt ein Redoxverhalten, das nur teilweise reversibel ist, was ein Gleichgewicht zwischen Elektronentransfer an der Elektrode und schnellen Nebenreaktionen im Wasser widerspiegelt. Mit Zugabe des Liganden verschoben und verengten sich die Voltammetrie‑Kurven, und die Peakströme änderten sich—klare Hinweise darauf, dass Metall und Ligand neue Komplexe bilden. Durch Analyse dieser Verschiebungen mit etablierten elektrochemischen Gleichungen fanden die Autoren Hinweise auf zwei Hauptstrukturen in Lösung: ein Vanadyl‑Ion gebunden an ein H2TIS‑Molekül sowie eine Spezies, bei der dasselbe Metallzentrum von zwei Liganden umgeben ist. Diese Komplexe zeigten im Vergleich zum freien Metallion eine verbesserte elektrochemische Stabilität.
Komplexformen mit Licht bestätigen
Um die elektrischen Messungen zu untermauern, führten die Forscher einfache lichtabsorptionsexperimente durch. Sie mischten Vanadyl‑Ionen und H2TIS in verschiedenen Verhältnissen bei konstanter Gesamtmenge und überwachten, wie stark die Lösungen bei einer bestimmten Wellenlänge Licht absorbierten. Die Absorption erreichte ihre Maxima bei Zusammensetzungen, die mit eins‑zu‑eins‑ und eins‑zu‑zwei‑Metall‑zu‑Ligand‑Verhältnissen übereinstimmen—diese Ergebnisse stimmen mit den elektrochemischen Befunden überein. Aus diesen Daten berechneten sie Stabilitätskonstanten und die zugehörigen Energieänderungen und zeigten, dass die Komplexbildung unter den getesteten Bedingungen spontan und energetisch begünstigt ist. Zusammen ergeben die Spannungs‑ und spektroskopischen Ergebnisse ein konsistentes Bild robuster Vanadyl–H2TIS‑Komplexe in Wasser.
Was das für Anwendungen in der Praxis bedeutet
Praktisch betrachtet zeigt diese Studie, dass ein einzeln entworfenes organisches Molekül je nach Lösung sehr verschieden reagieren kann, zwischen reversiblen und irreversiblen Elektronenwegen umschaltet und stabile Komplexe mit einem redoxaktiven Metall wie Vanadium bildet. Indem die Autoren aufschlüsseln, wie H2TIS auf saure, neutrale und basische Medien reagiert und wie fest es Vanadyl‑Ionen bindet, liefern sie Gestaltungsprinzipien für zukünftige Materialien, die Metalle in komplexen Umgebungen erkennen oder umwandeln sollen. Solch abstimmbare Redox‑ und Bindungseigenschaften machen H2TIS‑basierte Systeme zu vielversprechenden Kandidaten für nächste‑Generation elektrochemischer Sensoren, katalytischer Verfahren und Technologien zur Umweltreinigung.
Zitation: Mannaa, A.H., Gomaa, E.A., Zaky, R.R. et al. Medium controlled redox activity and coordination behavior of a triazole indolinone ligand with vanadyl lons. Sci Rep 16, 11370 (2026). https://doi.org/10.1038/s41598-026-44306-w
Schlüsselwörter: Vanadiumkomplexe, elektrochemische Sensorik, Redoxchemie, Metall–Liganden‑Wechselwirkungen, umweltbezogene Katalyse